Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Cardiología
Print version ISSN 1409-4142
Rev. costarric. cardiol vol.7 n.1 San José Jan. 2005
Dr. Carlos Ciancaglini
La evaluación no invasiva de la vasculatura intracraneal ha sido dificultosa e inexacta, pese a ser un elemento diagnóstico y pronóstico fundamental para numerosas patologías neurológicas y básica en la decisión de conductas terapéuticas.
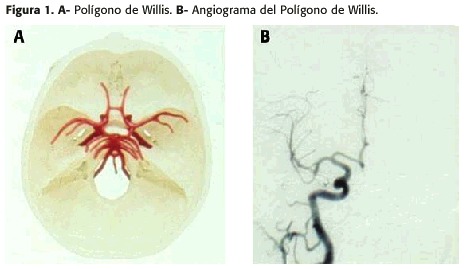
En 1982, Aaslid desarrolló el Doppler Transcraneal (DTC), realizando la insonorización del cráneo de su hija con una sonda ultrasónica de Doppler pulsado de baja frecuencia, capaz de penetrar el cráneo y evaluar la velocidad en los vasos del polígono de Willis (Figura 1). A partir de este momento, y gracias a un desarrollo vertiginoso, el DTC se ha transformado en una herramienta de bajo costo, muy útil desde el punto de vista clínico e investigativo, que permite evaluar en forma no invasiva la hemodinamia cerebral mediante un análisis objetivo, inmediato ("on line"), sin límite de tiempo y con la frecuencia de repetición que sea necesaria de las velocidades sanguíneas, que a su vez reflejan los cambios relativos del flujo cerebral regional (por ej. el monitoreo contínuo y en tiempo real del flujo sanguíneo cerebral durante cirugías neurovasculares, cardíacas y otras intervenciones vasculocerebrales).
Para estudiar cada una de las arterias y sus distintos segmentos se tienen en cuenta fundamentalmente cuatro elementos: la ubicación (ventana)y dirección del transductor en el cráneo; la profundidad del volumen de muestreo del Doppler pulsado y la dirección del flujo sanguíneo (hacia o alejándose de la sonda ultrasónica). Además, el sonido de cada una de las arterias es distintivo para el operador experimentado.
Indicaciones clínicas
Di agnóstico de enfermedad estenótica/oclusiva intracraneal.
Test auxiliar para la enfermedad oclusiva extracraneal cuando los tests diagnósticos extracraneales son dudosos.
Evaluación de los efectos hemodinámicos de la enfermedad oclusiva extracraneal sobre el flujo sanguíneo intracraneal (por ejemplo, de la oclusión de la carótida interna sobre las arterias cerebrales; robo subclavio).
Detección e identificación de las arterias aferentes o nutrientes ("feeders")en las malformaciones arteriovenosas.
Tests preoperatorio de compresión para evaluar la capacidad de colateralización del polígono de Willis.
Monitoreo intermitente y seguimiento:
Del vasoespasmo en la hemorragia subaracnoidea y en la migraña.
De la recanalización -espontánea o terapéuticamente inducida-de vasos ocluídos.
Del establecimiento de colaterales tras intervenciones de oclusión.
De la enfermedad oclusiva durante terapéutica anticoagulante.
De las nutrientes de malformaciones arteriovenosas durante el tratamiento con radioterapia.
Monitoreo contínuo durante:
Intervenciones neurorradiológicas (oclusiones con balón; embolizaciones).
Estudios farmacológicos a corto plazo con drogas vasoactivas.
Endarterectomía carotídea (shunt).
Cirugía cardíaca (¿encefalopatía isquémica?¿embolismo aéreo?).
Hipertensión intracraneal.
Evolución de la muerte cerebral.
Tests funcionales
Estimulación de los vasomotora cerebrales con CO2 u otras drogas vasoactivas.
Estimulación externa de la corteza visual.
Esta no es una lista completa, debido a que las aplicaciones de esta técnica, rápidamente evolutiva, siguen en desarrollo permanente.
Técnicas de examen
Prerrequisitos Generales
1)Debemos conocer perfectamente el estado de las arterias extracraneales.
2)El paciente debe descansar confortablemente para evitar fluctuaciones importantes en el nivel de CO2 y los artefactos causados por el movimiento.
Además, el examinador debe conocer 2 consideraciones anatómicas:
1) A menudo el número y accesibilidad de los forámenes intracraneales ("ventanas" ultrasónicas)que pueden ser penetrados con el haz ultrasónico son limitados y/o difíciles de identificar.
2) Las arterias de la base del cráneo varían marcadamente en cuanto a tamaño, curso y desarrollo y en función del sitio de acceso.
3) Hasta en un 20% de los pacientes es imposible penetrar el cráneo, especialmente en las mujeres añosas.
Instrumentos de doppler transcraneal (D. T. C.)
La primera consideración es una excelente relación señal-ruido. Por ello, los aparatos de D. T. C. tienen un ancho de banda más bajo, y, por lo tanto, un volumen de muestreo más grande y menos definido que la mayoría de los otros instrumentos de Doppler pulsado. Los equipos disponibles comercialmente usan Doppler pulsado con una frecuencia de emisión de 2- Mhz, con una profundidad del volumen de muestreo regulable (en pasos de 5 a 2mm)y con buena resolución direccional. Los siguientes son requerimientos adicionales:
1)Potencia de transmisión entre 10 y 100 mW/cm/seg.
2)Profundidad ajustable del volumen de muestreo.
3)P. R. F. (Frecuencia de repetición de pulsos)hasta 20 kHz.
4)Focalización del haz ultrasónico a una distancia entre 40 a 60mm; y
5)Análisis "on-line "de la velocidad media y de la velocidad sistólica pico, mediciones derivadas del espectro de las señales ultrasónicas.
Ventanas ultrasónicas
El paciente se explora en decúbito supino (vías transtemporal y transorbitaria)o sentado (vía suboccipital). Se describen cuatro enfoques para estudiar las arterias intracraneales:
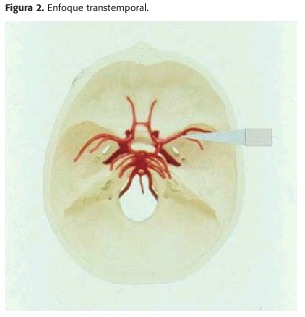
1)Enfoque TRANSTEMPORAL: (Figura 2).
Se coloca el transductor en la zona temporal, por encima del arco zigomático e inmediatamente por delante y levemente hacia arriba del trago del pabellón auricular. Generalmente es el sitio que más información brinda. En algunos pacientes se utiliza una segunda ventana (por encima y levemente hacia atrás de la anterior), especialmente para evaluar P2 de la Cerebral Posterior. En otros pacientes una tercera ventana transtemporal se ubica más frontalmente que las anteriores. Angulando el haz anteriormente (formando un ángulo de aproximadamente 6 °con respecto a la línea media sagital), se evalúan los segmentos M1 y M2 de la Arteria Cerebral Media, el segmento C1 del sifón carotídeo, el segmento A1 de la Arteria Cerebral Anterior y a menudo la A. Comunicante Anterior (Figura 3); la bifurcación de la Carótida Interna en Cerebral Anterior (A.C.A.) y Cerebral Media (A.C.M.)se ubica a 63+/-5 mm. Orientando posteriormente el haz con un ángulo de alrededor de 5° (y teniendo en cuenta que la bifurcación de la Arteria Basilar está a 78+/-5 mm)se evalúan el extremo distal de la Arteria Basilar y el segmento P1 de la Cerebral Posterior (siguiendo una línea cuya prolongación pasa 2 a 3 cm por detrás del orificio auditivo contralateral), el segmento P2 de esta misma arteria (dirigiendo el haz aún más posteriormente, en una línea cuya prolongación pasa a unos 5 cm por detrás del orificio auditivo contralateral)y las Comunicantes posteriores.
Arteria Cerebral Media (ACM): al evaluar el segmento M1 una compresión suave y rápida de la Carótida Primitiva homolateral (en su porción más proximal)confirma su localización (reducción de la velocidad sisto-diastólica).
Arteria Cerebral Anterior (ACA): comprende un segmento precomunicante (A1) - oblicuo hacia adelante, adentro y arriba, detectándose como una señal negativa a unos 65mm de profundidad - y un segmento poscomunicante (A2). La compresión de la carótida primitiva homolateral invierte el flujo sanguíneo en A1, mientras que la compresión contralateral lo aumenta. No obstante, cuando la Comunicante anterior no es funcional, estas maniobras compresivas inducen, respectivamente, una disminución de la señal y ausencia de cambios en la misma.
Arteria Comunicante Anterior (AcoA): para poder ubicarla se debe efectuar compresión de la Carótida Primitiva homolateral; se producen dos signos:
directo: registro nítido (o más fácilmente su audición, con una frecuencia más alta que la de cualquier arteria ubicada a esa profundidad,)a unos 70 o 75mm de profundidad, de una onda positiva (flujo dirigido hacia la Carótida Primitiva comprimida).
indirecto: inversión del sentido del flujo en la Cerebral Anterior homolateral.
Arteria comunicante Posterior (AcoP): de difícil detección por su dirección perpendicular al haz ultrasónico y flujo reducido. Se detecta como una señal de alta frecuencia ubicada entre la señal de la Carótida Interna y la Cerebral Posterior homolateral durante la compresión carotídea.
Arteria Cerebral Posterior (ACP): comprende un segmento precomunicante (P1)y un segmento postcomunicante (P2). P1 se orienta hacia adelante, abajo y afuera y con el transductor, orientado hacia atrás, adentro y ligeramente hacia arriba, se detecta como una señal positiva a 65mm de profundidad. A 75mm, la aparición de una segunda señal negativa indica la bifurcación del tronco Basilar (aparición de la Cerebral Posterior contralateral). La compresión de la Arteria Carótida Primitiva homolateral incrementa la velocidad P1 al desplazar flujo del sistema vertebrobasilar al carotídeo. En un 10-15% de los casos, la Cerebral Posterior nace de la Carótida Interna, y las maniobras fisiológicas no la ponen de manifiesto. La modificación de la señal Doppler al abrir y cerrar los ojos por estimulación de luz es un criterio para identificar la Cerebral Posterior.
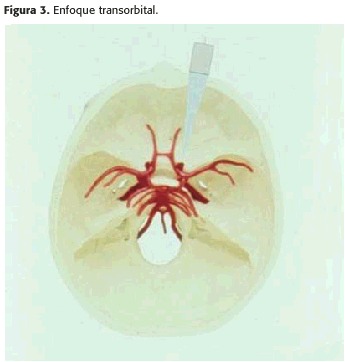
2)Enfoque TRANSORBITAL: (Figura 3).
Se estudian porciones de la circulación cerebral anterior colocando el transductor contra los párpados cerrados; se recomienda disminuir al 5% la potencia máxima (peligro potencial de opacificación del cristalino), que sólo se aumenta un 5-10 % si la señal es demasiado débil, pidiendo al paciente que mire hacia abajo, a la derecha y a la izquierda, utilizando incidencias supra o laterobulbares.
La A. Oftálmica (AO): se encuentra a profundidades de 45 a 50mm, mostrando una pulsatilidad característica de ascenso rápido y resistencia elevada (a diferencia de la Carótida Interna que posee flujo diastólico acentuado).
Sifón Carotídeo (SC): el segmento C3 (rodilla anterior del sifón carotídeo)se encuentra normalmente a los 60-65mm; a los 70 a 75mm de profundidad se encuentran los segmentos C2 (supraclinoideo)y C4 (intracavernoso)que muestran direcciones de flujo hacia afuera y hacia el transductor respectivamente, orientando el haz casi sagital (levemente oblicuado medialmente)y penetrando al cráneo por las fisuras infra o supraorbitarias. Si se coloca el transductor en el cuadrante superoexterno de la órbita y angulándolo en una dirección mucho más oblicua hacia la línea media, el haz penetra por el agujero óptico, tomando la porción supraclinoidea del sifón carotídeo contralateral.
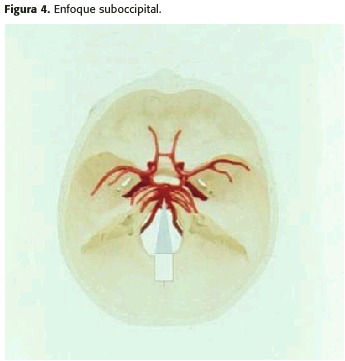
3)Enfoque SUBOCCIPITAL: (Figura 4).
Es esencial para el estudio de las arterias vertebrales y basilares en toda su extensión. El transductor se ubica exactamente entre el margen posterior del foramen magnum y la apófisis espinosa palpable del atlas, con el haz dirigido hacia el puente de la nariz. El paciente inclina la cabeza hacia adelante.
Arterias vertebrales (AV): La profundidad del volumen de muestreo se ubica en 65mm, y ambas arterias, derecha e izquierda, se siguen e inspeccionan individualmente, desde este punto hasta el foramen magnum, usando profundidades de muestreo progresivamente menores (de 50 a 35mm). A medida que la muestra se acerca a la superficie craneana el haz se angula cada vez más agudamente hacia el costado de la cabeza. Si la comunicante Posterior está permeable la compresión primero de la Carótida primitiva homolateral y luego de la contralateral, provoca un aumento de la señal vertebral en estudio.
Tronco Basilar (TB): Puede seguirse cefálicamente a partir del punto en el que las arterias vertebrales se unen. Su trayecto es oblicuo, hacia la derecha o izquierda, y hacia arriba y adelante. El extremo superior del tronco basilar se encuentra entre los 95 y 125 mm de profundidad. La señal es negativa (flujo que se aleja de la sonda). A veces, a 95 o 100 mm de profundidad se detecta una señal positiva que se modifica al comprimir la Carótida Primitiva y que se corresponde con el segmento P2 de la Cerebral Posterior.
4) Enfoque SUBMANDIBULAR.
Este enfoque completa el examen al permitir evaluar las porciones retromandibulares y extradurales mas dístales de la Carótida Interna (segmentos C5 y C6). Este exámen es un complemento muy útil de los estudios extracraneales, debido a que facilita la detección de disecciones de la Carótida Interna y sus oclusiones crónicas con abundante colateralización a través de la Arteria Carótida Externa. Con el transductor colocado en posición submandibular, el haz se dirige leve y posteriormente hacia la línea media. En general, la Carótida Interna puede seguirse desde una profundidad de 25mm hasta los 80-85 mm, donde se dobla medial y anteriormente para formar el sifón carotídeo (segmento C5).
Examen básico
Generalmente, lo más conveniente es comenzar con el enfoque transtemporal, identificando la ACM del lado estudiado a una profundidad de 50 a 55 mm, y luego "seguir "la red arterial homolateral, paso a paso, en varias direcciones. Es imprescindible confirmar el seguimiento de la ACM para asegurar su identificación, así como para otras arterias de la base del cráneo. Este "seguimiento " diagnóstico hace que podamos detectar el flujo ininterrumpidamente en el recorrido de la arteria estudiada, en pasos progresivos desde una profundidad superficial (35mm)a zonas más profundas (55mm)sin cambios en el perfil ni en la dirección del mismo. Cuando se sigue la ACM medialmente (65-70 mm); la presencia de un brusco cambio en la dirección del flujo (negativo o "escapando "del transductor)indica la detección del segmento A1 de la ACA. A esta profundidad las señales hacia el transductor generalmente provienen del sifón carotídeo en su unión con la ACM.
Angulando la sonda posteriormente desde este enfoque, se ubica el segmento P1 de la ACP, a profundidades de 65-70 mm. La ACP puede "rastrearse "hasta el tronco Basilar (75mm)y desde allí a la ACP contralateral (80-85mm). Los dos criterios de seguimiento o rasgos diagnósticos ultrasónicos más importantes para identificar las ACP sin tests compresivos son la presencia de flujo bilateral en la unión con el tronco Basilar y el cambio en la dirección del flujo con la ACP contralateral. Luego del enfoque transtemporal, se puede obtener información adicional desde las posiciones transorbital, suboccipital o submandibular.
Identificación de las arterias
Los criterios para la identificación de las arterias cerebrales son:
1) Profundidad de la muestra del Doppler pulsado.
2) Dirección del flujo sanguíneo a esa profundidad
3) Velocidad del flujo (velocidad media y velocidades de pico sístólica y telediástolica).
4) Posición del transductor (transtemporal, transorbital, submandibular o suboccipital).
5) Dirección del haz de ultrasonido(posterior, anterior, caudal, cefálico).
6) "Seguimiento "del vaso en estudio.
7) Respuesta a la compresión carotídea: en muchos individuos (especialmente en los ancianos)y en condiciones patológicas, los tests compresivos pueden ser necesarios para identificar ciertos segmentos arteriales. Estos tests se realizan con dos dedos sobre la A.C. Primitiva (comprimiendo en la zona inferolateral del cuello), o sobre las A. Vertebrales (a nivel de la apófisis mastoidea del occipital). Las maniobras compresivas generalmente no son necesarias para identificación vascular, pero sí son extremadamente útiles para evaluar vías colaterales. Las respuestas incluyen: a)ausencia de reacción; b)aumento de la velocidad de flujo; c)disminución de la velocidad; d)inversión del flujo; e)alternancia en la dirección del flujo (hacia y escapando del transductor)y f)cesación del flujo sanguíneo.
Mediciones de la velocidad sanguínea
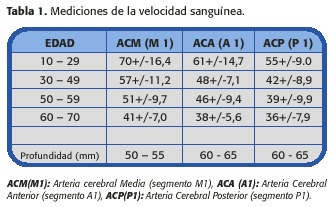
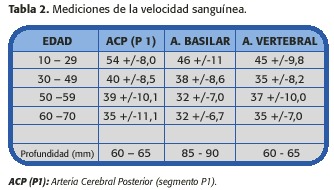
Las velocidades más altas se encuentran en la ACM o en la ACA. En personas normales las ACP y el tronco Basilar tienen valores más bajos. Existe discrepancia entre los valores de velocidades (en cuanto al cambio de frecuencia Doppler) y los volúmenes de flujo, lo que representaría un mecanismo compensatorio para mantener el flujo sanguíneo constante en vasos de diferente tamaño y así, las velocidades son más lentas en los vasos de mayor diámetro y mas rápidas en los vasos pequeños. Las velocidades disminuyen en las arterias basales craneales con la edad, lo que se correlaciona con cambios relacionados con el envejecimiento en el flujo cerebral, demostrando que la exactitud de la medición de velocidad es una estimación semicuantitativa del flujo, lo cual resulta especialmente cierto con mediciones seriadas en un mismo individuo. (Tablas 1 y 2)
Evaluación de la reserva funcional vasculocerebral
El DTC es un test funcional ideal para detectar cambios rápidos en la perfusión cerebral, y para evaluar los mecanismos de reserva vásculo-cerebral, usando distintos estímulos (hipo o hipercapnia, hipo o hipertensión, e hipoxia). Con concentraciones variables de CO2 la relación entre velocidad sanguínea y el volumen del flujo en las grandes arterias cerebrales es lineal, dado que el nivel de CO2 no afecta directamente el diámetro de estas arterias. Por lo tanto, los cambios que ocurren en la velocidad sanguínea reflejan cambios en el volumen del flujo.
El funcionamiento adecuado de esta reserva vasomotora implica que una caída en la presión de perfusión puede compensarse mediante la vasodilatación de las arteriolas corticales y, así, mantener una irrigación suficiente de la corteza cerebral. Si la reserva está agotada, no puede haber vasodilatación adicional con CO2, condición crítica debido a que la isquemia cerebral ocurrirá como consecuencia de una caída adicional de la presión de perfusión. El test de reactividad al COZ permite estudiar la reacción de las arterias cerebrales en diferentes situaciones patológicas y medir la reserva vascular cerebral.
Estos tests son útiles para evaluar el impacto hemodinámico de la enfermedad oclusiva carotídea extracraneal y otras condiciones con perfusión cerebral reducida como la migraña hipóxica, la exposición a grandes alturas, el trauma encefálico y el ACV embólico.
Aplicaciones clínicas
Enfermedad vascular intracraneal
La ventaja clínica más obvia del DTC es la evaluación rápida del paciente crítico con un ACV para detectar estenosis severas u oclusiones intracraneales.
ESTENOSIS:
Los siguientes son rasgos típicos de estenosis localizada de una arteria basal cerebral:
1) aumenta la velocidad del flujo.
2) flujo turbulento (ensanchamiento espectral y aumento de los componentes sistólico y de baja frecuencia del espectro de Doppler pulsado).
3) fenómeno de "covibración "(vibración de la pared arterial y de tejidos blandos adyacentes). Como en la enfermedad vascular extracraneal, las estenosis leves aumentan sólo la velocidad sístólica sin afectar mayormente el resto del espectro de Doppler, mientras que las estenosis moderadas o severas, provocan mayor aumento de la velocidad, con ensanchamiento espectral, aumento de la velocidad diastólica y flujo turbulento. Generalmente se demuestra también caída postestenótica de la velocidad sistólica pico. Otras condiciones que simulan los hallazgos de las estenosis severas son las arterias intracraneales que actúan como colaterales (presentan aumento de la velocidad y turbulencia) y las que alimentan malformaciones arteriovenosas (aumento de la velocidad). En estos casos, el aumento de la velocidad sanguínea ocurre en todo el trayecto de las arterias comprometidas, lo que las distingue de los hallazgos localizados que ocurren en las arterias con zonas de estenosis. El vasospasmo y la estenosis se diferencian porque el primero es más generalizado que la arteriosclerosis, a menudo es bilateral y en varias distribuciones arteriales y cambia progresivamente con el tiempo, por lo que a estos pacientes es útil seguirlos con exámenes diarios.
OCLUSIÓN:
La oclusión de las arterias basales del cerebro puede diagnosticarse por tres datos:
1) ausencia de señales arteriales a una determinada profundidad en la que dicha arteria debería ser ubicada;
2) presencia de señales de Doppler en vasos que se comunican con la arteria ausente (ocluida);
3) flujo alterado en los vasos comunicantes, (indica colateralización). Por ejemplo, la oclusión de la ACM se diagnostica por la falta de señales de la ACM en presencia de señales de otras arterias (ACP y/o ACA o porción distal del sifón carotídeo), indicando ventana ultrasónica satisfactoria (una ventana inadecuada es causa de falso positivo de oclusión). También lo es la dislocación de la ACM por tumor o hematoma, patologías que deben ser descartadas por TAC. Los pacientes con oclusión de la ACM e infarto cerebral, pueden presentar recanalización de la misma cuando son seguidos seriadamente.
Errores y agudeza diagnóstica:
La demostración no invasiva de estenosis y/u oclusión arterial intracraneal es una herramienta clínica valiosa, pero pueden ocurrir varios errores:
1) interpretar equivocadamente a los canales hiperdinámicos de flujo colateral como estenosis;
2) desplazamiento de las arterias que se buscan por lesiones ocupantes (tumores, hematomas);
3) interpretación equivocada de las variables fisiológicas en el polígono de Willis;
4) diagnosticar un vasospasmo como estenosis.
5) diagnosticar una hiperemia reactiva como estenosis.
La mayoría de estos problemas se solucionan con la experiencia del operador.
Existe poca información sobre la sensibilidad y especificidad del DTC para detectar lesiones intracraneales. Un problema es la variación de la sensibilidad y especificidad de un segmento arterial a otro, por lo que los parámetros de agudeza diagnóstica deben calcularse separadamente para el sifón carotídeo, los distintos segmentos de la ACM, ACA y la ACP y, particularmente, para las arterias vertebrales (AV)y el tronco basilar (TB). La agudeza en detectar lesiones en estas dos últimas es un problema y las dificultades diagnósticas resultan de:
1) el curso y ubicación de las AV y TB es impredecible;
2) a menudo la unión de ambas AV no puede localizarse confiablemente;
3) la ausencia de señales de flujo en una AV puede no representar patología;
4) la oclusión de una AV puede no producir anormalidades de flujo intracraneal;
5) la oclusión distal del TB no necesariamente produce anormalidades en el flujo de las AV;
6) la tasa señal/ruido a la profundidad requerida para ubicar las AV (90mm) es baja.
Evaluación de los efectos hemodinámicos de enfermedad oclusiva extracraneal sobre la circulación cerebral
Estenosis u oclusión carotídea:
El DTC permite la identificación de flujo colateral en las lesiones carotídeas extracraneales (hasta el presente sólo era posible hacerlo mediante angiografía). Además, el DTC estudia la potencialidad del polígono de Willis como vía de circulación colateral (su permeabilidad se evalúa registrando las velocidades y cambios en la dirección del flujo que ocurren en las arterias basales como respuesta a la compresión de la Carótida Primitiva).
La existencia de lesiones carotídeas extracraneales importantes produce cambios significativos en la circulación intracraneal. En presencia de estenosis severa u oclusión carotídeas, la velocidad y los índices de pulsatilidad de la ACM homolateral disminuyen, reflejando vasodilatación distal homolateral a la lesión. Se puede encontrar aumento de la velocidad y turbulencia en las arterias colaterales, hallazgos que se acentúan con la compresión de la Carótida Primitiva contralateral. La presencia de una Arteria Comunicante Anterior (ACoA)funcional se detecta por un aumento de la velocidad en la ACA contralateral a la Carótida Interna estenosada y por reversión del flujo en la ACA homolateral. Hallazgos similares se exhiben en la ACP, revelando flujo colateral funcionante desde la circulación posterior a la ACM y ACA a través de la Arteria Comunicante Posterior (ACoP). En caso de lesión severa en ambas Carótidas (lesiones bilaterales)se observa aumento de la velocidad en la AB, con colateralización a ambos hemisferios a partir de la circulación posterior. Probablemente, el DTC sea más sensible para detectar flujo colateral funcionante que la angiografía. Si bien en presencia de lesiones críticas de una o ambas Carótidas Internas la mayoría de los ACV se deben a un mecanismo tromboembólico más que a un efecto de bajo flujo, este último subgrupo de enfermos está en mayor riesgo y en ellos el beneficio de la cirugía es máximo, siendo importante la evaluación de la hemodinamia en la vía Carótida –ACM: ej. identificación de signos de agotamiento de la reserva vascular cerebral, por medio del test de CO2, indicador confiable de capacidad de reserva colateral; una reducción inferior al 34% (normal 86+/- 16% ), se asocia fuertemente a síntomas isquémicos cerebrales u oculares (infarto cerebral de bajo flujo), ataques isquémicos transitorios posicionales y oftalmopatía isquémica crónica.
Sistema vertebrobasilar:
Un ejemplo típico de alteración hemodinámica en este sistema y su estudio por DTC es el robo de la arteria subclavia, condición benigna que, aún en pacientes sintomáticos, rara vez requiere recanalización arterial dado que los síntomas vertebrobasilares se deben generalmente a microangiopatía. Cualquier cambio brusco del flujo causado por restricción al paso de sangre en alguna de las arterias vertebrales, puede medirse directamente en el TB. En reposo, el flujo sanguíneo del TB casi nunca está críticamente comprometido, incluso en presencia de robo continuo. No obstante, si la AV nutriente contralateral también está enferma, el flujo en el TB puede estar reducido, puede mostrar un patrón de ida y vuelta o incluso estar invertido. Durante el test de hipertermia del brazo claudicante, la velocidad y dirección del flujo en el TB puede estar afectada en mayor o menor medida, dado que es muy resistente a los cambios críticos secundarios al robo subclavio.
Monitoreo de vasoespasmo cerebral:
La aplicación clínica más conocida del DTC es la detección y monitoreo del vasoespasmo causado por hemorragia subaracnoidea, (la cual es motivo de morbilidad y mortalidad significativas)en forma no invasiva y continua. Existe una estrecha relación entre el aumento de la velocidad en las arterias cerebrales básales espásticas (ACM, ACP, ACA) y la severidad de la hemorragia subaracnoidea: tamaño y extensión del coágulo subaracnoideo, estado clínico del paciente y severidad angiográficamente documentada del vasoespasmo (velocidad media mayor de 120 cm/seg). El lado con cambios más severos corresponde a la ubicación predominante del coágulo y a la presunta localización del aneurisma. Un brusco incremento en la velocidad del flujo (mayor de 20 cm/seg por día)en los primeros días después del sangrado, se asocia a mal pronóstico. Generalmente, en pacientes con vasoespasmo, una velocidad de la ACM mayor de 200 cm/seg se asocia a una reducción crítica del flujo cerebral.
El vasoespasmo ocurre usualmente entre los días 4 y 14 posthemorragia subaracnoidea, pero los aumentos en la velocidad detectables por DTC a menudo preceden en horas o días a la aparición de los síntomas, permitiendo tratamiento profiláctico.
El DTC también es una herramienta útil para determinar el momento de la cirugía y evaluar el efecto de nuevos tratamientos médicos.
Monitoreo intraoperatorio:
La gran ventaja de este método es ser completamente no invasivo y muy sensible para detectar rápidas alteraciones en el flujo sanguíneo. La ausencia de métodos adecuados para monitorizar cambios relativos del flujo cerebral durante procedimientos invasivos, hizo que se monitorizaran parámetros electrofisiológicos, pero éstos proveen información del metabolismo anormal secundario a la reducción de la perfusión cerebral. En cambio, el DTC -ubicando el segmento M1 de la ACM en forma intermitente con breves intervalos o continuamente -brinda información inmediata sobre el flujo cerebral, anticipando riesgos potenciales o permitiendo rápidas modificaciones en el tratamiento de situaciones como la endarterectomía carotídea, la cirugía de bypass aortocoronario o en la Sala de Terapia Intensiva,
En el caso del monitoreo con DTC durante la endarterectomía carotídea, al clampear la carótida, una velocidad en la ACM mayor de 10cm/seg o una caída =65% respecto a sus valores basales, indican adecuada colateralización.
El monitoreo con DTC durante la cirugía de bypass puso en duda la teoría de que el daño cerebral y el ACV perioperatorio eran debidos a hipoperfusión. Por el contrario, la hiperperfusión cerebral accidental puede jugar un rol más decisivo, así como la microembolia aérea y la pérdida de la autorregulación cerebral. Preoperatoriamente, el DTC sirve para identificar los pacientes en riesgo de encefalopatía isquémica (evaluación de la capacidad autorregulatoria del cerebro mediante el test del CO2).
Monitoreo en la sala de terapia intensiva:
Este es un campo amplio e inexplorado aún. Como se mencionó previamente, en la evolución de las hemorragias subaracnoideas con vasoespasmo, así como en la hidrocefalia hiper o normotensiva, los estados de bajo flujo asociados a enfermedad oclusiva extracraneal, la claudicación miocárdica o enfermedades valvulares y en la muerte cerebral en curso, el DTC puede ser de gran utilidad. Los fenómenos de hipo o hiperperfusión que siguen a los traumatismos craneoencefálicos son una indicación importante del DTC en la medida que el control estricto del flujo cerebral puede llevar a una reducción del daño cerebral.
Muerte cerebral:
La determinación de muerte cerebral se basa en tres aspectos:
1) criterios clínicos
2) criterios electroencefalográficos
3) demostración angiográfica de ausencia de circulación intracraneal. La ausencia de flujo intracraneal causa un fenómeno de reflujo característico en las arterias basales cerebrales durante la sístole tardía. Este movimiento en vaivén se detecta fácilmente en la onda de velocidad del espectro de DTC. Dependiendo del gasto cardíaco, los perfiles del flujo pueden ser bruscos o pulsátiles, o pueden estar amortiguados en las fases de aceleración y desaceleración.
Malformaciones arteriovenosas y fístulas
Las arterias que nutren a las fístulas AV (malformación congénita)son normales, pero presentan características funcionales anormales en su flujo que pueden ser detectadas por el DTC: aumento de la velocidad (a veces hasta 280 cm/seg.), pulsatilidad reducida (relación diastólica/sistólica mayor de 0, 74)y respuesta reducida al CO 2. Además, existen marcadas diferencias en los valores de la velocidad de un hemisferio con respecto al contralateral. Estas anormalidades permiten localizar la fístula AV y evaluar su importancia hemodinámica. Con la estimulación por inhalación de CO2, las nutrientes de las fístulas AV no muestran cambios en la velocidad (sólo un leve incremento de los valores diastólicos)o no responden en absoluto a la hipocapnia. Aquellas nutrientes que contribuyen escasamente al llenado de las fístulas AV pueden no ser detectadas por los cambios en velocidad y pulsatilidad, pero exhiben escasa respuesta al CO2.
Después de la cirugía de la fístula AV, el reexamen con DTC es particularmente útil para identificar nutrientes residuales y cambios severos relacionados con el sangrado. En las fístulas operadas exitosamente, las nutrientes muestran una caída dramática de la velocidad a valores por debajo de los normales y luego, progresivo retorno a valores característicos de las arterias cerebrales normales.
El aneurisma arterial puede diagnosticarse con el DTC siempre que su tamaño sea superior al del volumen de muestreo; sospecharlo ante la disminución localizada de la velocidad y un índice de pulsatilidad elevado.
Conclusiones
El DTC es una técnica novedosa, con gran potencial en el diagnóstico clínico, que mide parámetros fisiológicos en forma no invasiva con un instrumento barato y portátil, libre de riesgos y en tiempo real, con posibilidades de monitoreo ininterrumpido durante tiempos prolongados (estudio de vasoespasmo, monitoreo intraoperatorio, etc.).
Sin embargo, deben destacarse algunas dificultades del método como lo es el que su capacidad diagnóstica es altamente dependiente de la habilidad del operador y de su experiencia y conocimientos sobre la anatomía y fisiología de la circulación cerebral.
Los usos futuros potenciales del DTC serían la evaluación de la presión intracraneana en pacientes críticos, enfermos con migraña y en niños con enfermedades vasculares.
Referencias
1. Aaslid R., Markwalder T-M, Norris H: Noninvasive transcranial Doppler ultrasound recording of flow velocity in basal cerebral arteries. J Neurosurg 57: 769, 1982. [ Links ]
2. Ringelstein EB, Otis SM, Schneider PA: Noninvasive assessment of CO2-induced cerebral vasomotor reactivity. Comparison with rCBF findings during 133-xenon inhalation measurement. J Cereb Blood Flow Metab, 1991. [ Links ]
3. Otis S, Ringelstein EB: Transcranial Doppler sonography. En Bernstein DE (Ed.): Noninvasive Diagnostic Techniques in Vascular Disease. St. Louis, CV Mosby, 1990, p. 59. [ Links ]
4. Otis S, Ringelstein EB: Transcranial Doppler sonography. En Zwiebel WJ (Ed) : Introduction to Vascular Ultrasonograpy. WB Saunders, 1992, p. 145. [ Links ]
Servicio de Medicina Vascular, Instituto Modelo de Cardiología, Córdoba,
Argentina. e-mail: carloscian@hotmail.com