Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Cardiología
Print version ISSN 1409-4142
Rev. costarric. cardiol vol.5 n.3 San José Dec. 2003
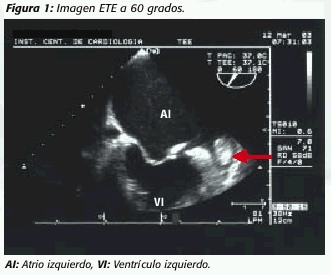
Paciente masculino de 45 años de edad sin factores de riesgo coronario, quien fue admitido a Hospital Clínica Bíblica por cuadro de 24 horas de sensación de palpitaciones y lipotimia. Niega antecedentes de fiebre reumática u otra patología médica, ingresando con presión arterial de 110/60, frecuencia cardíaca de 118 lpm, tonos cardíacos arrítmicos por fibrilación atrial (FA) sin auscultarse soplos y sin signos de congestión venocapilar pulmonar ni sistémica. El electrocardiograma mostró FA de alta respuesta ventricular con complejos QRS y repolarización normales. Se realizó ecocardiograma transesofágico multiplanar (ETE) (figura 1, imagen ETE a 60 grados) como estudio previo a Cardioversión Eléctrica (CE) posterior al fracaso de 12 horas de bolus e infusión de amiodarona intravenosa, el cual mostró dilatación atrial izquierda (AI), una válvula mitral con engrosamiento difuso de grado ligero, fusión comisural con área valvular por tiempo de hemipresión de 1.3 cm 2 , puntos de calcificación en la base de la valva posterior, ecocontraste espontáneo grueso en atrio izquierdo y una orejuela izquierda (OI) ocupada por imagen hiperecoica de 18 x 11 mm, de bordes bien definidos correspondiente a trombo en orejuela izquierda (flecha).
La sensibilidad del ecocardiograma transtorácico (ETT) en la detección de trombos en AI es del 39 al 63%, con un rendimiento diagnóstico aún menor en el diagnóstico de trombosis en la OI, aún cuando algunos estudios recientes indican que los equipos de última generación pueden mejorar la capacidad de visualizar la OI al 75% y se puede interrogar la misma mediante doppler pulsado en el 69% de los casos (1, 2). Debido al buen rendimiento diagnóstico del ETE en estructuras posteriores, se ha constituido en el método de elección para la detección de la trombosis del la OI, la cual es la fuente embólica más frecuente en pacientes en FA, siendo el ETE superior a la medicina nuclear (plaquetas marcadas) o a la tomografía axial en su rendimiento diagnóstico (1, 3, 4). La OI es un fondo de saco remanente del atrio embrionario, frecuentemente multilobulado (25%) con proyección en ejes impredecibles y con trabeculaciones internas por músculos pectíneos de variable grosor, factores que convierten al la ETE en una prueba de sensibilidad y especificidad variable, operador dependiente, encontrándose la mayor discrepancia entre observadores con estructuras de menos de 15 mm en el interior de la OI (5, 6).
La ETE provee otra información adicional como son el estado anatómico y funcional de válvulas cardíacas y tabiques, presencia de ecocontraste espontáneo en atrio y orejuela izquierda y su densidad, así como la presencia de placas de ateroma complicadas en aorta torácica, que se ha constituido en una de las causas más importantes de embolismo en pacientes mayores de 60 años en ritmo sinusal (7, 8).
La FA es la arritmia más frecuente en la práctica clínica, afectando al 0.4% de la población general y entre el 2 y 5% de sujetos mayores de 60 años. La presencia de FA duplica el riesgo de muerte e incrementa 6 veces el riesgo de sufrir un evento cerebrovascular agudo (ECVA), siendo la causa aislada más importante de ECVA isquémico (9). Por estas razones hemos tenido tradicionalmente un interés particular en restablecer el ritmo sinusal en estos pacientes. La nueva clasificación clínica de la FA, con implicaciones pronósticas y terapéuticas, establece que esta puede ser paroxística (generalmente autolimitada, con episodios de duración inferior a 7 días), persistente (no autolimitada, con una duración superior a 7 días) o permanente, en la que no se realizó cardioversión o se prefirió por mantener la frecuencia cardíaca, manteniéndose por tanto en FA de forma crónica. La CE de la FA es un tratamiento muy efectivo para la restauración del ritmo sinusal (permitiendo por ende solamente períodos temporales de anticoagulación), pero con una tasa significativa de recurrencias, sobre todo si la FA tiene una duración mayor al año o con un diámetro de AI mayor a 50 mm, situaciones en las que las posibilidades de mantener al paciente en ritmo sinusal son escasas, debido principalmente al remodelado eléctrico del tejido atrial, con un acortamiento del período refractario (10).
Mediante 18 estudios aleatorizados publicados acerca del uso de anticoagulación oral y antiagregación plaquetaria en FA permanente, se ha concluido que la warfarina (manteniendo el INR entre 2 y 3 en menores de 75 años, entre 1.6 y 2.5 en mayores de 75 años y nunca menor a 1.6) reduce el riesgo de ECVA en alrededor de un 60%, la aspirina en un 20% y la warfarina respecto a la aspirina en un 40%, con el riesgo potencial de sangrado en pacientes adultos mayores principalmente con la warfarina, factor que debe tenerse en mente debido al hecho que la edad promedio de los pacientes que se presentan con un ECVA en FA es de 75 años. El riesgo de embolismo clínicamente significativo en la FA permanente es muy variable, siendo por tanto primordial el detectar en cada paciente los factores que auguren un alto riesgo embólico y por ende un tratamiento agresivo. En este sentido la edad mayor a 65 años, la disfunción sistólica ventricular izquierda concomitante y antecedentes de hipertensión arterial, ECVA o isquemia cerebral transitoria, son factores clínicos predictores de ECVA, sobretodo si actúan de forma combinada. Por tanto un paciente menor de 65 años de edad con FA permanente sin estos factores clínicos de riesgo, y sin evidencia de valvulopatía en el ETT (FA aislada), posee un bajo riesgo de ECVA (0.5%/año) (11). Recientemente han sido publicados los estudios AFFIRM (12) en 4.060 pacientes y el RACE (13) en 522 pacientes, que han tratado de contestar la pregunta si es mejor la estrategia de control del ritmo (CE y antiarrítmicos posteriores) o control de frecuencia cardíaca (tratamiento médico para controlar la respuesta ventricular de la FA), los cuales han tenido un profundo impacto en la opinión cardiológica mundial, al mostrar una mortalidad y una combinación de mortalidad y hospitalizaciones comparables estadísticamente, pero tendientes a ser mayor en los grupos de control del ritmo. Sin embargo hay otros factores que conviene tener en cuenta para una lectura correcta de estos estudios. Se debe considerar que la mayoría de los pacientes incluidos habían tenido episodios previos de FA, o sea se trataban de FA recurrente (RACE en pacientes con FA recurrente posterior a una CE previa), poco sintomáticos, y se excluyeron pacientes jóvenes sin factores de riesgo, por lo cual sus conclusiones no pueden extenderse a un primer episodio de FA, a la FA recurrente muy sintomática ni a la FA aislada. Otros aspectos importantes del estudio AFFIRM son que el 34.6% de los pacientes en control de frecuencia se encontraban en ritmo sinusal al final de los 5 años de seguimiento, el uso de beta bloqueadores fue entre el doble y un tercio más frecuente en los pacientes de control de frecuencia que al de control de ritmo (con beneficios demostrados de mortalidad en todo el espectro de la enfermedad cardiovascular) y el 72% de los ECVA ocurrieron en pacientes que no se encontraban anticoagulados, la habían dejado o esta se encontraba en rangos subterapéuticos, en un grupo de pacientes que por tratarse de FA recurrente, con antecedentes de ECVA previo, deberían de encontrarse en anticoagulación crónica con warfarina (11). Por estas razones considero que sus conclusiones deben limitarse a los pacientes en FA no valvular de edad avanzada con factores clínicos de riesgo tromboembólico y pueden ser tratados controlando la respuesta ventricular a la FA. La ETE puede jugar un papel en la selección de pacientes en FA con moderado a alto riesgo de presentar un ECVA y que requieran un manejo agresivo con anticoagulación oral crónica. En el subestudio con ETE del SPAF III (14), la presencia de flujo lento denso, trombos en orejuela izquierda y placas de ateroma en aorta complicadas, permitieron detectar a los pacientes con riesgo clínico de ECVA con mayor riesgo de presentarlo, mostrando que los pacientes de riesgo clínico que no presentaban dichos hallazgos en el ETE, tienen un bajo riesgo tromboembólico (1.3%/año) independientemente de la estrategia terapéutica utilizada y podrían tratarse con atiagregación plaquetaria con aspirina, y los pacientes con riesgo clínico y con alguno de los 3 factores en el ETE descritos, deben tratarse con anticoagulación oral crónica, recordando que los pacientes con placas de ateroma complicados deben recibir tratamiento para estabilizar la misma (p. ej. Estatinas e IECAS) al no ser la anticoagulación eficaz para reducir significativamente su riesgo.
El manejo tradicional del primer episodio de FA ha consistido en al menos 3 semanas de anticoagulación oral previo a una CE, continuando la warfarina por al menos 4 semanas posteriores, para cubrir el riesgo embólico en ritmo sinusal producido por el aturdimiento atrial. Posteriormente al estudio ACUTE se adoptó la estrategia de anticoagulación aguda intravenosa con ETE preCE a descartar presencia de trombos, seguido por 4 semanas de anticoagulación oral. Se consideraba que en pacientes con FA de menos de 72 horas, podía realizarse la CE de forma segura sin requerir un ETE previo. Sin embargo al demostrarse posteriormente la presencia de trombos en un 10% de pacientes con FA de menos de 72 horas y observarse embolismo en algunos de esos pacientes (9), se adoptó el ETE precardioversión en todos los pacientes en FA aguda independientemente de su evolución, estrategia adoptada actualmente por la mayoría de grupos y que utilizamos en el paciente descrito en este reporte del eco del mes. Recientemente se ha propuesto un abordaje simplificado (15) con el uso de enoxaparina 100 UI/Kg. al ingreso y posteriormente cada 12 horas, ETE subsecuente y CE a las 24 horas de inicio de enoxaparina en ausencia de trombos o ecocontraste espontáneo denso en el ETE. La real novedad se plantea en la realización de un segundo ETE a los 7 días, continuando con anticoagulación únicamente los pacientes con signos al ETE de contusión atrial, siendo posible suspender la anticoagulación al sétimo día en el 75% de los pacientes. Sería razonable combinar ambos planteamientos modificándolo al sustituir la enoxaparina al ingreso con anticoagulación IV y cardioversión inmediatamente posterior al ETE, siendo egresado con enoxaparina subcutánea a dosis de anticoagulación.
El paciente descrito en este ecocardiograma presenta algunas variaciones a los planteamientos descritos que merecen ser comentados: el origen de su FA es reumático por estenosis mitral (que junto con los pacientes en hemodiálisis crónica (16) constituye uno de los grupos con mayor riesgo de trombosis en orejuela izquierda y se asocia a un riesgo tromboembólico 16 veces mayor que la población general); la morfología del trombo que sugiere organicidad del mismo; y finalmente la morfología valvular, con calcificaciones solamente en base de valva posterior y ausente en comisuras que lo hace un candidato potencial a una futura valvuloplastia percutánea. Es generalmente aceptado que 3 semanas de anticoagulación en pacientes con trombosis en OI, permite la resolución del trombo o su organización, siendo posible en dicho momento una CE segura. Sin embargo alrededor del 75% de los trombos no han resuelto completamente a los 4 meses de anticoagulación, y aunque la mayoría están ya organizados, se estima en un 10 a 15% los pacientes que presentaran un evento embólico con la CE después de las 3 semanas de anticoagulación, siendo la estenosis mitral uno de los factores que predispone a una resolución tardía de los trombos en la OI (17). La valvuloplastia mitral percutánea está contraindicada en pacientes con trombos en AI u OI, sin embargo se ha demostrado que la anticoagulación oral resuelve un 62% de los trombos a un seguimiento promedio de 12 meses (18), siendo posible reconsiderar esta opción terapéutica posterior a 6 a 12 meses de anticoagulación. La CE en la FA secundaria a estenosis mitral presenta una menor posibilidad de éxito y una mayor tasa de recurrencia, por lo cual se prefiere reservarla a casos seleccionados de FA en estenosis mitral ligera a moderada, con diámetros de AI menores a 55 mm y precedido de ciclo de amiodarona previo a la CE. Los beneficios potenciales del restablecimiento del ritmo sinusal en estos pacientes sería un beneficio estimado del 20% en el gasto cardíaco, reducción en la velocidad de dilatación de la AI y una protección parcial a la formación de trombos. En el caso descrito, alternativas terapéuticas al control de la frecuencia con digitálicos y cirugía mitral convencional, sería la CE a los 6 meses de anticoagulación y al menos 1 mes de tratamiento con amiodarona; y considerar la valvuloplastia mitral percutánea después de 12 meses de anticoagulación. En cualquier planteamiento requiere anticoagulación oral crónica y deben realizarse ETE previos a cualquier intervención. Además con la evidencia existente del efecto benéfico de algunos IECA o ARA II (enalapril, captopril, trandolapril, losartan, candesartan e irbesartan) en la prevención del remodelado eléctrico atrial, debe considerarse el uso de alguno de estos medicamentos en los pacientes sometidos a cardioversión eléctrica o con FA paroxística.
Finalmente es importante considerar para el futuro cercano otras nuevas opciones terapéuticas de la FA en casos muy seleccionados como son la ablación percutánea, sobretodo con las mejorías técnicas recientes en la prevención de la estenosis pulmonar posterior al procedimiento, y la oclusión de la OI mediante dispositivos de implantación percutánea como el PLAATO o el Amplatzer en pacientes de alto riesgo embólico y contraindicación de anticoagulación oral (19, 20).
Referencias
1- Manning WJ, Weintraub RM, Waksmonski CA, Haering JM, Rooney PS, Maslow AD, Johnson RG, Douglas PS. Accuracy of transesophageal echocardiography for identifying left atrial thrombi. Ann Intern Med 1995; 123:817-822 [ Links ]
2- Omran H, Jung W, Rabahich JR, Wirtz P, Becher H, Illien S, Schimpf R, Luderitz B. Imaging of thrombi and assesment of left atrial appendage function: a prospective study comparing transthoracic and transoesophageal echocardiography. Heart 1999; 81:192-98 [ Links ]
3- Sun SS, Hsieh JF, Tsai SC, Ho YJ, Lee JK, Kao CH. Monitoring the effect of anticoagulants on left atrial thrombi in patients with rheumatic heart disease: assessment with 111ln-oxide-labelled platelet heart scintigraphy and transesophageal echocardiography. Nucl Med Commun 2000; 21:627-30 [ Links ]
4- Tani T, Yamakami S, Matsushita T, Okamoto M, Toyama J, Suzuki S, Fukutomi T, Itoh M. Usefulness of electron beam tomography in the prone position for detecting atrial thrombi in chronic atrial fibrillation. J Comput Assist Tomogr 2003; 27:78-84 [ Links ]
5- Hart RG, Halperin JL. Atrial fibrillation and stroke. Stroke 2001; 32:803-808 [ Links ]
6- Kronik G, Stollberger C, Schuh M, Abzieher F, Slany J, Schneider B. Interobserver variability in the detection of spontaneous echo contrast, left atrial thrombi, and left atrial appendage thrombi by transoesophageal echocardiography. BHJ 1995; 74:80-83 [ Links ]
7- Manning WJ, Douglas PS. Transesophageal echocardiography and atrial fibrillation. Added value or expensive toy? Ann Intern Med 1998; 128:685-687 [ Links ]
8- Lanzoni AM, Parajeles-Vindas A. Placas ateroscleróticas de aorta torácica: una entidad poco diagnosticada de enfermedad tromboembólica. Rev Costarr Cardiol 1999; 1 (1):3-8 [ Links ]
9- Gersh BJ, Gottdiener JS. The role of transesophageal echocardiography in atrial fibrillation. Ann Intern Med 1995; 123:882-884 [ Links ]
10- Moro C, Hernández-Madrid A. Cardioversión eléctrica para la fibrilación auricular. ¿Existe aún indicaciones tras el estudio AFFIRM? Rev Esp Cardiol 2003; 56:751-3 [ Links ]
11- Hart RG, Halperin JL. Atrial fibrillation and thromboembolism: a decade of progress in stroke prevention. Ann Intern Med 1999; 131:688-695 [ Links ]
12- Wyse DG, Waldo AL, DiMarco JP, Domanski MJ, Rosenberg Y, Schron EB, et al. A comparison of rate control and rhythm control in patients with atrial fibrillation. N Engl J Med 2002; 347:1825-33 [ Links ]
13- Van Gelder IC, Hagens VE, Bosker HA, Kingma JH, Kamp O, Kingma T, Said SA, Darmanata JI, et al. A comparison or rate control and rhytm control in patients with recurrent persistent atrial fibrillation. N Engl J Med 2002; 347:1834-40
14- The Stroke Prevention in atrial Fibrillation Investigators Committee on Echocardiography. Transesophageal echocardiography correlates of thromboembolism in high-risk patients with nonvalvular atrial fibrillation. Ann Intern Med 1998; 128:639-47 [ Links ]
15- De Luca I, Sorino M, Del Salvatore B, De Luca L. A new therapeutic strategy for cardioversión of atrial fibrillation. Ital Heart J 2001; 2:831-40 [ Links ]
16- Nishimura M, Hashimoto T, Kobayashi H, Fukuda T, Okino K, Yamamoto N, Iwamoto N, Nakamura N, Yoshikama T, Ono T. The high incidente of left atrial appendage trombosis in patients on maintenance haemodialysis. Nephrol Dial transplant 2003; 18:2339-47 [ Links ]
17- Larsen JA, McPherson DD, Cádiz AH, Goldberger JJ. Course of atrial thrombi resolution using transesophageal echocardiography. Echocardiography 2003; 20:121-8 [ Links ]
18- Silaruks S, Thinkhamrop B, Tantikosum W, Wongvipaporn C, Tatsanavivat P, Klungboonkrong V. A prognostic model for predicting the disappearance of left atrial thrombi among candidates for percutaneous transvenous mitral commissurotomy. J Am Coll Cardiol 2002; 39:886-91 [ Links ]
19- Meier B, Palacios I, Wendecker S, Rotter M, Cao QL, Keane D, Ruiz CE, Hijazi ZM. Transcatheter left atrial appendage occlusion with Amplatzer devices to obviate anticoagulation in patients with atrial fibrillation. Catheter Cardiovasc Interv 2003; 60:417-22 [ Links ]
20- Omran H, Hardung D, Schmidt H, hammerstingl C, Luderitz B. Mechanical occlusion of the left atrial appendage. J Cardiovasc Electrophysiol 2003; 14:S56-9 [ Links ]
* Centro Cardiológico Integral. San José, Costa Rica














