Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Cardiología
Print version ISSN 1409-4142
Rev. costarric. cardiol vol.5 n.2 San José Aug. 2003
Resumen
Palabras clave
- Enfermedad de Kawasaki, aneurisma coronaria gigante.
Introducción
Es reconocida la mayor incidencia en varones sobre mujeres en proporción de 1.5: 1 así como en individuos de raza asiática. El diagnóstico se establece con la presencia de fiebre elevada por 5 o más días, más 4 de los criterios clínicos que se describen en la tabla 1 , o con la evidencia de aneurismas coronarios, asociado a tres criterios clínicos. En estos criterios discrepan las escuelas japonesa y americana. En la tabla 1 se resumen los criterios clínicos y la tabla 2 muestra los principales hallazgos de laboratorio.

A nivel cardíaco la cronología de la afectación vasculítica puede describirse en 4 fases:
1. 0-9º día: Vasculitis de la íntima coronaría con o sin pericarditis, miocarditis, endocarditis, valvulitis o afección de] sistema de conducción.
2. 10º-25º día: Panvasculitis con formación de aneurismas.
3. 28º-30º día: Granulación y resolución a partir de vasos más pequeños.
4. > 40º día: Cicatrización y estenosis con fibrosis endocárdica. A otros niveles la secuencia de la vasculitis es similar, siendo más frecuente la aparición de aneurismas en la arteria humeral y las arterias de los territorios renal, testicular, del mesenterio, pulmón, páncreas, bazo, glándula suprarrenal y tubo digestivo. Cuando los pacientes tienen menos de 2 años la coronaría más afectada es la derecha y a los 5 años, la izquierda. El aneurisma se presenta con más frecuencia entre los días 10 y 25 del comienzo de la enfermedad, alcanzando su cenit a las 7 semanas, estabilizándose y regresando espontáneamente después de 30 meses en un 35-50% de los casos. La fiebre mantenida, la velocidad de eritrosedimentación superior a 100 mm/hora y la edad menor de 6 meses, favorecen la formación del aneurisma coronario. La aparición de trombosis y estenosis en los aneurismas favorece el infarto de miocardio (8 ).La ecocardiografía bidimensional en proyección eje corto paraesternal (9 ) y la resonancia magnética en proyección axial permiten visualizar el aneurisma en su porción proximal y pueden ser válidas para el seguimiento de la enfermedad. La coronariografía se ha considerado como la técnica más completa para obtener imágenes de los aneurismas distases y de las estenosis a diferentes niveles. En cuanto a las características del aneurisma coronaría, este tiene un valor pronóstico que depende de su diámetro, y el tratamiento varía, al enfrentarnos a aneurismas gigantes.
Tradicionalmente se decía que el aneurisma gigante, era aquél mayor a 8 mm de diámetro y se relacionaba con estenosis durante la evolución. Sin embargo, recientemente, Tsuda y colaboradores, en Japón, demostraron que los aneurismas con un diámetro mayor a 6 mm, fueron los que presentaron posteriormente estenosis (10 ). En este mismo centro, se utiliza la tomografía axial ultra rápida, para evaluar la calcificación coronaría de los aneurismas mayores a 6mm, en el seguimiento de los pacientes cada 18 meses, complementando a la ecocardiografía (11 ).
A continuación presentamos un caso reciente de una paciente con enfermedad de Kawasaki complicado con un aneurisma sacular gigante de la arteria descendente anterior.
Caso Clínico
H. M. D, femenina de 9 años, vecina de Tibás, conocida portadora de estreñimiento crónico y reflujo vesico uretral izquierdo grado lI, es referida al Servicio de Emergencias del Hospital Nacional de Niños por presentar cuadro de lo días de evolución de fiebre alta, odinofagia y cefalea. Sus síntomas fueron tratados inicialmente como faringoamigdalitis aguda, (con cefalexina), sin embargo, no hubo mejoría de su cuadro clínico. Al cuarto día de iniciada la fiebre, asoció un brote puntiforme en el tronco y la espalda que luego se extendió a las extremidades. En ese momento se cambió el esquema antibiótico por penicilina benzatínica y amoxacilina, sin embargo, los síntomas persistieron y un día antes de ser ingresada, asoció conjuntivitis y edema de manos y pies con descamación de la piel. Al examen físico se encontró una paciente de bajo peso, decaída, llorosa, taquicárdica y febril al tacto. Presentaba conjuntivitis hiperémica no purulenta y leve prurito, faringe hiperémica y lengua aframbuesada, presencia de adenopatía cervical derecha indurada y dolorosa de aproximadamente 2 cm de diámetro. Presentaba un soplo sistólico de regurgitación, grado 2/6 en foco mitral, campos pulmonares limpios y abdomen sin alteraciones. Se internó con el diagnóstico de enfermedad de Kawasaki y se le indicó gammaglobulina intravenosa 2g/kg en 12 h y aspirina 50 mg/kg en 4 dosis.
Se le practicó ese mismo día un ecocardiograma transtorácico que demostró un corazón sin malformaciones congénitas e insuficiencia mitral leve. La arteria coronaría izquierda presentaba una dilatación del tronco, y la arteria descendente anterior presentaba una dilatación aneurismática con un diámetro medido de 7.5 mm (figura 1 ). La arteria circunflejo y la coronaría derecha se observaron normales.
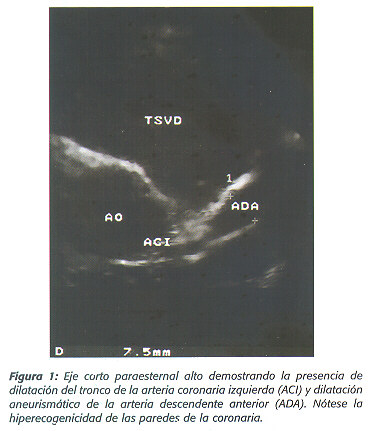
Dos días después de que ingresó al hospital se egresó con resolución de su sintomatología y con tratamiento con aspirina a dosis anti-inflamatorias.
Dos semanas después del egreso, un nuevo ecocardiograma no mostró diferencias con el estudio previo. Un mes y medio después, se le practicó un nuevo ecocardiograma transtorácico de control, encontrándose una dilatación aneurismática de la descendente anterior, que mide en su diámetro mayor 7.5 mm. No se encontraron zonas de disquinesia, aquinesia, o dilatación de cámaras cardíacas. La insuficiencia mitral había desaparecido. El cateterismo cardíaco se le realizó 6 meses después del cuadro agudo y mostró un aneurisma sacular gigante (30 mm de longitud y 7mm de diámetro) de la rama descendente anterior de la arteria coronaría izquierda sin alteraciones en la arteria circunflejo ( Figura 2 ). La arteria coronaría derecha no tenía dilataciones. No se demostró insuficiencia aórtica. La arteriografía de otros territorios vasculares de riesgo, no mostró alteraciones.
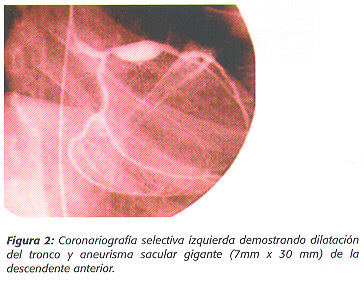
Discusión
En esta paciente, la edad de la presentación de la enfermedad es inusual, sin embargo notamos que su comportamiento clínico es el típicamente descrito para la enfermedad de Kawasaki, sobre todo en lo que respecta al cuadro febril, al no responder a antipiréticos usuales y al no haber mejoría con el uso de antibióticoterapia para la infección de vías respiratorias superiores. Si bien el ecocardiograma es un método diagnóstico seguro, de bajo costo y no invasivo, la determinación de las medidas del aneurisma, de la cual va a depender el tratamiento y el pronóstico de la paciente, son más exactas en la coronariografía, que se considera a nivel internacional como el método patrón de oro.
Se han descrito predictores de riesgo para el desarrollo de aneurismas en la enfermedad de Kawasaki ( 13 ), entre los que se mencionan en varias series la presencia de fiebre sostenida, hemoglobina por debajo de lo gramos, leucocitosis con desviación izquierda, y trombocitosis, elementos que nuestra paciente presentó. El uso temprano de la gammaglobulina asociada a la aspirina ha logrado prevenir la formación de aneurismas coronarlos hasta en un 30 %. Un 5% del total de los pacientes presentan aneurismas a pesar del tratamiento temprano adecuado. Otro porcentaje similar de pacientes presentan regresión espontánea de aneurismas pequeños. las características del grupo de pacientes que desarrollan aneurismas gigantes, encajan dentro del perfil de alto riesgo y ameritan un tratamiento y seguimiento continuo y prolongado. Con respecto al tratamiento a largo plazo, actualmente se recomienda, que los pacientes que no presentan anormalidades de las arterias coronarias, no necesitan tratamiento con aspirina más allá de los tres meses posteriores al cuadro y pueden ser evaluados con electrocardiografía y prueba de esfuerzo cada tres años. Los pacientes con aneurismas coronarlos transitorios o pequeños deben ser tratados con aspirina, a dosis de 3-5 mg/kg/día hasta la resolución de las anomalías y cada año deben ser evaluados con ecocardiograma y prueba de esfuerzo. No es necesaria la restricción física si no hay alteración en la prueba de esfuerzo. Pacientes con aneurismas coronarlos gigantes (> 6-8 mm de diámetro) son los que tiene el peor pronóstico pues pueden desarrollar trombosis coronaria, estenosis o infarto del miocardio. El infarto del miocardio ocurre varios años después del cuadro agudo. En los niños pequeños, los síntomas de infarto agudo incluyen llanto, vómitos, disnea, colapso cardiovascular y choque. Los casos documentados han ocurrido durante el sueño o en reposo ( 14 ). Los aneurismas gigantes usualmente no se resuelven y estos pacientes debe investigárseles por aneurismas en otros sitios (renal, braquial, femoral). Éstos se deben tratar con aspirina a dosis de 3-5mg/kg/día, warfarina y seguimiento cada seis meses. Durante la evolución del paciente cualquier anormalidad en la prueba de esfuerzo debe ser estudiada mediante angiografía. La Asociación Americana del Corazón, estratifica tanto el riesgo, como su tratamiento y control posterior ( 15 ). Los pacientes que desarrollan estenosis son candidatos a revascularización quirúrgica o percutánea. La experiencia con angioplastía coronaria percutánea es muy limitada. La terapia trombolítica intravenosa o intracoronaria se ha utilizado con resultados variados ( 16 ). Alrededor del mundo, cerca de 15 pacientes han recibido un transplante de corazón por enfermedad isquémica severa secundaria a esta enfermedad (17 ).
Los aneurismas de mejor pronóstico son aquellos pequeños, fusiformes y que ocurren en niños menores de un año de edad. Debemos insistir en el pronto diagnóstico y tratamiento de los pacientes con esta enfermedad para disminuir las posibilidades de compromiso cardíaco y la morbimortalidad a corto y largo plazo.
Referencias
1. Kawasaki T. Acute febrile mucocutaneous syndrome with lymphoid involvement with specific desquamation of the fingers and toes in children. Clinical observation of 50 patients. Jpn J Allergy 1967; 16: 178-222. [ Links ]
2. The Etiology and pathogenesis of Kawasaki's disease-how are we to an answer? Curr Op lnfect Dis 1997; 10: 226-232. [ Links ]
3. Kawasaki's syndrome. Pediatrics in Review 1996; 17: 153-62. [ Links ]
4. Kawasaki's Disease Epidemiology, Late Prognosis and Therapy. Rheum Dis Clin of North Am 1994; 17: 907-918. [ Links ]
5. Curtis N, Zheng R, Lamb JR, Levin M. "Evidence for a superantigen mediated process in Kawasaki disease". Arch Dis Child. 1995; 72: 308-311. [ Links ]
6. Leung DYM, Meissner HC, Fulton DR, Murray DL, Kotzin BL, M Schlievert PM "Toxic shock syndrome toxin-secreting Staphylococcus aureus in Kawasaki disease". Lancet 1993; 342: 1385-1388. [ Links ]
7. American Heart Association Comittee in Rheumatic fever, Endocarditis and Kawasaki Disease. "Diagnosis and therapy of Kawasaki Disease in children" Circulation 1993; 87: 1776-1780. [ Links ]
8. Yanagawa H, Yashiro M, Nakamura Y, Sakata K, Kawasaki T.Intravenous gammaglobulin treatment of Kawasaki disease in Japan: Results of a nationwide survey. Acta Paediatr 1995; 84: 765768. [ Links ]
9. Fujimara T, Fujimara H, Ueda T, Nishioka K, Hamashima Y. Comparison of macroscopic postmortem angiographic and 2-dimensional echocardiographic finding oí coronary aneurysm in children with Kawasaki disease. Am J Cardiol 1986; 57: 761-764. [ Links ]
10. Tsuda E, Kamiya T, Ono Y et al. lncidence of stenotic lesions predicted by acute phase changes in coronary arterial diameter during Kawasaki disease: threshold for coronary aneurysm causing stenosis. Circulation 2002; 106: 11-334. [ Links ]
11. Kaichi S, Tsuda E, Fujita H et al. Detection of calcification by electron beam computed tomography in patients with coronary artery lesions due to Kawasaki disease: relationship between the acute coronary artery dilatation and the later appearance of calcification. Circulation 2002; 106: 11-593. [ Links ]
12. Beiser AS, Takahashi M, Baker AJ, et al. for the US Multicenter Kawasaki Disease Study Group. A predictive instrument for coronary artery aneurysms in Kawasaki disease. Am J Cardiol 1998; 81: 1116-20. [ Links ]
13. Susuki A, Kamiya T, Tsuda E, et al. Natural history of coronary artery lesions in Kawasaki disease. Prog. Pediatr Cardiol 1997; 6: 211. [ Links ]
14. Kato H, Ichinose E, Kawasaki T. Myocardial infarction in Kawasaki disease: clinical analyses in 195 cases. J Pediatr 1986;108: 923-7. [ Links ]
15. Adnan S Dajani, et Cols. Guidelines for long - term Management of Patients with Kawasaki Disease. AHA / Scientific Statement. Circulation 1994; 89: 916-22. [ Links ]
16. Kitamura S, Kameda Y, Seki T, Kawachi K, Endo M, Takeuchi Y, et al. Long-term outcome of myocardial revascularization in patients with Kawasaki coronary artery disease. A multicenter cooperativa study. J Thorac Cardiovasc Surg 1994; 107: 663-73. [ Links ]
17. Checchia PA, Pahl E, Shaddy RE, Shulman ST. Cardiac transplantation for Kawasaki disease. Pediatrics 1997; 100: 695-9. [ Links ]
* Asistente del Servicio de Cardiología Pediátrca Hospital Nacional de Niños Dr. Carlos Saénz Herrera CCSS San José Costa Rica
** Especialista en Medicina Interna Residente de Cardiología. Sistema de Estudios de Post-grado CENDEISS.
Correspondencia a. Dr. Carlos Mas Romero, Apartado 72795- 1000 San José. e-mail drmas@doctor.com














