Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Cardiología
Print version ISSN 1409-4142
Rev. costarric. cardiol vol.4 n.3 San José Dec. 2002
Introducción
"Como la obesidad y la diabetes, la hipertensión esencial es una enfermedad de la civilización del hombre, que resulta de la colisión de un moderno estilo de vida con genes paleolíticos. "
Alan B. Weder.
La enfermedad cardiovascular constituye el mayor problema de salud en cifras absolutas de morbi-mortalidad en los países occidentales, principalmente por encima de los 60 años, y la hipertensión arterial (HTA) constituye el principal factor de riesgo asociado al desarrollo de las enfermedades cardiovasculares. Un estudio realizado en nuestro país demuestra que entre los individuos de 35 a 64 años de edad, el 42% de las muertes por enfermedad coronaria, el 46.4% de las muertes por enfermedad cerebrovascular y el 25% de las muertes de cualquier causa están relacionadas con la presencia de HTA (1). En otro reciente estudio español que incluyó más de 32.000 pacientes atendidos en consultas de atención primaria o de cardiología, entre los pacientes con cardiopatía, la HTA estaba presente en un porcentaje muy alto de casos, en el 71% de los pacientes con insuficiencia cardíaca, en el 66% de los pacientes con cardiopatía isquémica y en el 66% de los casos de fibrilación auricular (2). La prevalencia de HTA en España clásicamente se estimaba en un 20%-30% en la población de edad media, alcanzando cifras del orden del 60% en mayores de 65 años (3). Pero estas cifras son considerando HTA con presión arterial (PA) >160/95; si se considera HTA como actualmente, con PA >140/90, las cifras son aún superiores, alcanzando un 45.1% (1). Pero además teniendo en cuenta que la población tiende a envejecer y que está aumentando la cifra de hipertensos entre los adolescentes, no es difícil deducir que la incidencia de HTA aumentará en las décadas futuras con el incremento de morbi-mortalidad por complicaciones cardiovasculares.
Al haberse comprobado una relación lineal entre los valores de PA sistólica y diastólica con la morbi-mortalidad cardiovascular, el objetivo principal del tratamiento de la HTA es reducir la PA hasta los niveles recomendados por las diferentes guías publicadas al respecto (4,5). El desafío del tratamiento farmacológico es sumar los beneficios obtenidos con la Deducción sostenida de la PA a la protección cardiovascular que podrían conferir ciertos fármacos, a través de efectos que serían independientes del descenso de PA(6).
Importancia del Sistema Renina-Angiotensina-Aldosterona en Hipertensión
El sistema renina-angiotensina-aldosterona (SRAA) se ha considerado un sistema encargado de la regulación de la PA y del volumen extracelular. Posteriormente se conoció su influencia en la fisiopatología de la HTA, fundamentalmente basado en la acción de la angiotensina II (Ang II). Esta sustancia forma parte de la familia de factores neurohumorales, que junto a los propios efectos del aumento de PA son los responsables de la repercusión de la HTA sobre los órganos diana (7). La Ang II es un péptido corto de 8 amino ácidos y constituye el principal agente vasopresor del Sistema Renina-Angiotensina-Aldosterona (SRAA). Se forma a partir de la angiotensina I mediante la acción de la enzima convertidora de angiotensina (ECA). Sin embargo, se ha demostrado que en algunos tejidos existen otras enzimas distintas a la ECA que también pueden convertir angiotensina I en Ang II, como quimasa, catepsina G o CAGE (Figura 1). Incluso se han descrito vías alternativas que pueden formar Ang II a partir de angiotensinógeno, como t-PA, tonina, o catepsina. Por otra parte, la ECA es una enzima inespecífico que además de catalizar el paso de angiotensina 1 a Ang II, inactiva la vía de degradación de las quininas y de esta manera aumenta los niveles de bradiquinina circulante. Por todo ello, la acción de los IECA no sólo se basa en la disminución de la producción de Ang II, sino también en el aumento de niveles de bradiquinina. Además los IECA no son capaces de inhibir por completo la producción de Ang II, ya que otras vías enzimáticas pueden producir Ang II de forma independiente de la ECA.
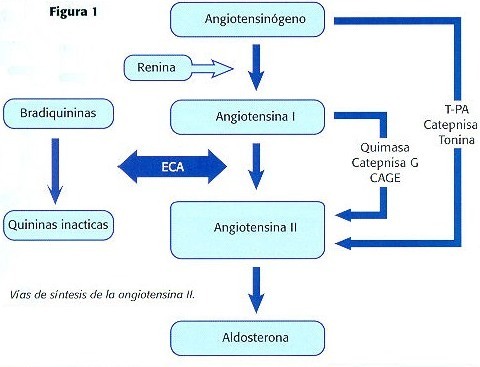
La Ang II ejerce su acción a través de la inhibición de la adenilato-ciclasa, aumentando el calcio intracelular y actúa, tanto a nivel sistémico como hormona circulante, como a nivel local como hormona autócrina-parácrina. A nivel sistémico tiene efectos vasoconstrictores y estimula la síntesis y liberación de aldosterona y vasopresina, lo que produce aumento de las resistencias periféricas y retención de sodio y agua; efectos todos ellos que contribuyen a aumentar la PA. A nivel local actúa en varios tejidos, como corazón, vasos sanguíneos o riñón, produciendo proliferación celular de miocitos, de músculo liso vascular y aumento de la formación de colágeno con fibrosis intersticial y vascular, lo que constituye la principal causa de daño orgánico en una amplia variedad de enfermedades relacionadas con la HTA. En el tejido humano la Ang II tiene dos receptores específicos principales: AT1 y AT2 que ejercen distintos efectos al ser estimulados. La respuesta biológica mediada por la Ang II dependerá de la estimulación de los correspondientes receptores en los órganos diana (8). La mayoría de los efectos no deseados de la Ang II son producidos a través de la activación de los receptores ATI, que son los más extensamente distribuidos y expresados en la mayoría de los tejidos. Por tanto, el efecto principal de la Ang II en condiciones normales estaría determinado fundamentalmente por la estimulación de los receptores ATI. Estos receptores parecen jugar un papel clave en la regulación de la PA (9).
Bloqueo del SRAA en la Protección Cardiovascular
Si bien no existen dudas de que el hecho de disminuir las cifras tensionales en los pacientes hipertensos disminuye la incidencia de patología cardiovascular, como lo demuestran el metaanálisis de McMahon (10) o el "Blood Pressure Lowering Trialist Colaboration Group" (11), el objetivo del tratamiento en la HTA debería ser más ambicioso y buscar beneficios adicionales en términos de protección cardiovascular más allá del propio efecto de la reducción de la PA. En este sentido, los IECAs han demostrado, a través de múltiples estudios, el beneficio que se obtiene en diferentes órganos y tejidos mediante el bloqueo del SRAA. Estos estudios, aunque no fueron realizados específicamente en la población hipertensa, mostraron que los IECAs condicionan protección renal (12), reducción de la morbi-mortalidad en enfermedad coronaria (13,14), en insuficiencia cardíaca (15), en nefropatía diabética (16) y en enfermedad cerebrovascular (17). Pero todos estos estudios fueron realizados comparando los IECAs frente a placebo; es decir, demuestran el beneficio de los IECAs cuando se estudia su efecto en comparación con el comportamiento de pacientes sin tratamiento activo. Sin embargo, en estudios realizados en poblaciones de pacientes hipertensos en que se comparó los IECAs frente a otras clases de antihipertensivos, los IECA no han mostrado mejores resultados en morbi-mortalidad cardiovascular que los fármacos clásicos como betabloqueantes y/o diuréticos (18-20). Estas evidencias sugieren la importancia del bloqueo del SRAA en la protección de órganos diana, pero quizá la inhibición incompleta de la formación de Ang II que producen los IECA podría no ser suficiente para reducir la morbi-mortalidad cardiovascular más que otros fármacos y diferenciarse de éstos. Por tanto surge la necesidad de buscar moléculas que actúen bloqueando de un modo más selectivo y eficaz la Ang II y combinen efectos al menos tan favorables como los de los IECA, con un mejor perfil de tolerancia (21). A partir de estas premisas adquiere relevancia la aparición en el mercado de los antagonistas de receptores de Ang II (ARA II), que a través de su mecanismo de acción proponen un bloqueo específico de los efectos deletéreos de la Ang ll.
Papel de los ARA II en la Hipertensión Arterial
Los ARA II ejercen su acción a través de] bloqueo de los receptores AT1 de la Ang II de forma específica y altamente selectiva y actúan inhibiendo los efectos clásicos desfavorables de Ang II. Así, los ARA II antagonizan la acción de la Ang II producida por cualquier vía enzimática y no actúan sobre la degradación de las quininas, con lo que no condicionan un aumento de sus niveles en sangre. Además al bloquear los receptores ATI los ARA II permiten que la Ang II circulante se pueda ligar a los receptores AT2, lo que puede añadir un efecto adicional potencialmente muy beneficioso (22). Por otra parte, la bradiquinina circulante, además de sus efectos vasodilatadores, parece estar asociada a ciertos efectos adversos como la tos seca, proceso que limita el uso de IECAs hasta en un 5-20% (23). Los ARA lI, por tanto, están libres de esta reacción adversa tan característica de los IECA.
Existen estudios que muestran que los ARA II tienen una tolerabilidad mejor que la de los otros fármacos antihipertensivos. De hecho, Bloom publicó en 1998 un análisis retrospectivo de 21.700 pacientes tratados con distintos fármacos antihipertensivos y analizó la persistencia del tratamiento con la droga inicial a 12 meses de seguimiento. Este autor observó que los pacientes medicados con un ARA II al año tenían una persistencia en el tratamiento superior al del resto de los pacientes que estaban tratados con otros fármacos (24). Posteriormente, Conlin publicó un seguimiento de 15.000 pacientes del estudio de Bloom desde los 12 a los 48 meses, donde encontró que la continuidad del tratamiento inicial seguía siendo superior con ARA II (25). Se ha demostrado que los ARA II presentan menos efectos adversos que los IECA, principalmente debido a la ausencia de tos, y la incidencia de reacciones adversas de estos fármacos es comparable al placebo (26-28). Este excelente perfil de tolerabilidad puede ser fundamental para lograr una mayor adherencia al tratamiento(29). Por otra parte, la eficacia de los ARA II para disminuir la PA está bien demostrada desde hace varios años, tanto en HTA leve como moderada o severa (30-33) y en múltiples estudios comparativos estos fármacos han mostrado una eficacia antihipertensiva similar a la de IECAS, antagonistas del calcio o betabloqueantes (34-39). Por tanto, ante una eficacia antihipertensiva similar y un mejor perfil de tolerabilidad, los ARA II pueden considerarse una familia farmacológica de gran utilidad en el tratamiento actual de la HTA (40). Así, las recomendaciones de la OMS-SIH de 1999 establecen que los ARA II deben considerarse al igual que betabloqueantes, diuréticos, antagonistas del calcio, IECA o alfabloqueantes como tratamiento de primera elección en HTA (5).
Es posible que con las evidencias obtenidas con los ARA lI, en cuanto a eficacia y tolerabilidad en HTA y con los beneficios evidenciados en los pacientes con nefropatía diabética (estudios IDNT y RENAAL) y en los pacientes con hipertrofia ventricular izquierda (estudio LIFE), las indicaciones de estos fármacos pueden ampliarse en un futuro inmediato. Es importante señalar como ejemplo de esto último, que la American Diabetes Association (ADA) ha decidido considerara los ARA II como tratamiento de primera elección en los pacientes hipertensos con diabetes tipo 2, con microalbuminuria o proteinuria (41).
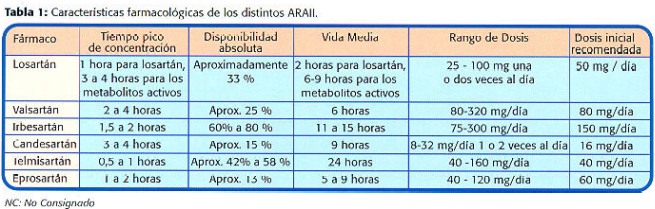
Hasta la fecha son siete los ARA II aprobados para HTA: losartán, valsartán, candesartán, irbesartán, eprosartán, telmisartán y olmesartán (Tabla 1) Estos fármacos tienen idéntico mecanismo de acción y solo difieren en cuanto a sus características farmacológicas. Se han realizado diversos estudios comparativos analizando el efecto sobre la PA. Los resultados obtenidos han mostrado algunas diferencias entre ellos en cuanto a potencia antihipertensiva (42-44). Sin embargo, un metanálisis que agrupó a 11.281 pacientes de 43 estudios diferentes con ARA II no mostró diferencias significativas en cuanto a la reducción de PA alcanzada con los distintos ARA lI, lo que sugiere que los ARA II podrían tener una eficacia similar cuando se administran a las dosis usuales recomendadas (45).
Estudios de Morbi-Mortalidad en Hipertensión con ARA II
La incidencia de complicaciones cardiovasculares relacionadas con la HTA sigue siendo alta, a pesar de las numerosas alternativas terapéuticas disponibles en el mercado y a las diversas estrategias de tratamiento instauradas. En los últimos años se han realizado varios estudios sobre morbi-mortalidad cardiovascular en el paciente hipertenso comparando distintos fármacos entre sí. Principalmente se compararon los efectos de los fármacos "modernos" como antagonistas del calcio e IECAs frente al de los fármacos "clásicos" como betabloqueantes y diuréticos. Al contrario de lo que se pensaba, no se observaron diferencias significativas entre los fármacos en términos de morbi-mortalidad cardiovascular (19,46-49). Estos hallazgos parecen indicar que todos los antihipertensivos son similares y el único efecto beneficioso es el propio de la reducción de PA. En pacientes hipertensos de muy alto riesgo cardiovascular, como son los pacientes con nefropatía diabética, los estudios IDNT y RENAAL realizados con irbesartán y losartán respectivamente, demostraron una reducción significativa de la morbi-mortalidad cardiovascular. En ambos estudios la variable principal de eficacia fue la combinación de muerte, tiempo de duplicación de creatínína sérica y caída en insuficiencia renal terminal. En el estudio IDNT los pacientes se distribuyeron en tres grupos de tratamiento: placebo, amiodipino e irbesartán. En este estudio se demostró que el tratamiento con irbesartán a los 2.6 años de tratamiento produjo una reducción del riesgo relativo del 23% (p=0.006) respecto a amiodipino y del 20% (p=0.024) respecto a placebo, siendo los resultados con amiodipino y placebo similares (50). El estudio RENAAL comparó el tratamiento basado en losartán frente a placebo. También se confirmó, de forma similar al IDNT, una reducción del riego relativo del 16% (p=0.024) en el grupo tratado con el ARA II (51). El hecho de que en dos ensayos clínicos similares con dos ARA II diferentes los resultados sean tan parejos confirma los hallazgos y establece la utilidad de estos fármacos en la protección cardio-vasculo-renal del paciente con nefropatía diabética.
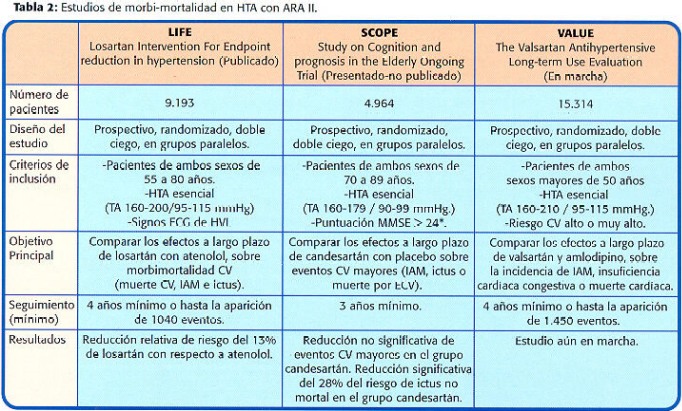
Tres son los grandes estudios de morbi-mortalidad que analizan el papel de los ARA II en HTA: el estudio LIFE (ya publicado), el estudio SCOPE (presentado pero aún no publicado) y el estudio VALUE (aún en marcha)(Tabla 2) Hasta ahora la evidencia disponible es la que proviene del estudio LIFE, el único que ya ha sido publicado (52). El estudio LIFE se diseñó hace varios años con la hipótesis de que el antagonismo selectivo de los receptores ATI de la Ang II con losartán podría ser más eficaz que el betabloqueo con atenolol para reducir la morbilidad y mortalidad cardiovascular en los pacientes con HTA (PA sistólica 160-190 y/o diastólica 95-110) y signos electrocardiográficos de hipertrofia ventricular izquierda, detectada por criterios del producto duración-voltaje de Cornell (>2.440 mmxmsg) o por criterios de voltaje de Sokolow-Lyon (>38 mm). Se realizó una comparación aleatorizada, doble ciego y con doble enmascaramiento de los efectos a largo plazo de losartán con los de atenolol. La variable principal de valoración fue la morbilidad y la mortalidad cardiovasculares, que se definió por la combinación de muerte de causa cardiovascular, infarto agudo de miocardio e ictus (46). Fueron randomizados 9.194 pacientes con una edad media de 67 años y una PA media de 174.4/98.7 mm Hg y se realizó un seguimiento mínimo de 4 años. Basalmente, cerca del 16% había tenido manifestaciones de enfermedad coronaria, 8% ictus previo o accidente isquémico transitorio y el 13% eran diabéticos (53,54). En estos pacientes los betabloqueantes son una opción adecuada para realizar la comparación con losartán, ya que estos fármacos son de primera elección en el tratamiento de la HTA, tienen una eficacia antihipertensiva similar a losartán (55) y han demostrado disminuir la morbilidad y mortalidad al compararse con placebo (56). A los 12 meses de seguimiento, la PA había disminuido a 150.5/85.1 mm Hg pero solamente el 23% de los pacientes estaba tomando el fármaco de estudio en monoterapia (57). Esta tendencia se mantuvo y al finalizar el estudio sólo el 9-10% de los pacientes estaban tratados solamente con la medicación inicial (50 mg atenolol o 50 mg de losartán), lo que enfatiza la necesidad de la politerapia en la gran mayoría de los pacientes hipertensos.
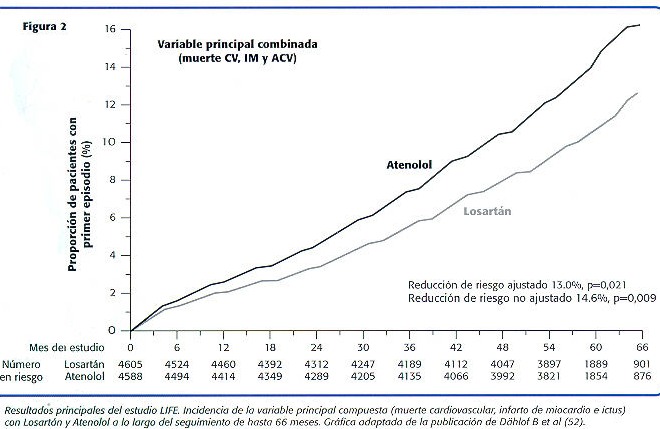
A los 5 años se observó que el grupo de pacientes con tratamiento basado en losartán mostró una reducción relativa del riesgo del 13% respecto al grupo de atenolol de aparición de muerte cardiovascular, infarto de miocardio o ictus (508 pacientes del grupo losartán y 588 pacientes del grupo atenolol, p=0.021). (Figura 2) Esta reducción del riesgo fue debida a una significativa reducción del 25% en la incidencia de ictus (p=0.001), ya que la aparición de muerte cardiovascular y de infarto de miocardio fue similar en ambos grupos de tratamiento. La reducción del riesgo era mayor (14.6%, p= 0,009) sin introducir un ajuste respecto a la puntuación de riesgo de Framingham y el grado de hipertrofia ventricular izquierda (HVI) por ECG en situación basal. En cuanto a la HTA, hubo una reducción de PA importante y muy similar en ambos grupos (30.2/16.6 mm Hg en el grupo losartán y 29.1/16.8 mm Hg en el grupo atenolol). Esto evidencia que los beneficios adicionales obtenidos por el ARA II son independientes del puro efecto sobre la PA. Secundariamente el estudio LIFE mostró una reducción significativa del 25% (p<0.001) del riesgo de padecer diabetes de nueva aparición en los pacientes tratados con losartán frente a los tratados con atenolol. Se observó además una mayor regresión de la hipertrofia ventricular izquierda en el grupo de losartán. Con losartán se observó un reducción del 10% y del 16% con los criterios de Comell y de Sokolow-Lyon, mientras que con atenolol la reducción fue de 4.4% y 9% respectivamente (en ambos casos, p<0.0001). Hay que destacar que ésta mayor capacidad de regresión de la hipertrofia ventricular no explica todo el efecto favorable del ARA II respecto a atenolol. Se demostró también una menor incidencia de efectos adversos en el grupo de losartán (52). En el subestudio del LIFE que evaluó la morbilidad y mortalidad cardiovascular en 1.195 pacientes diabéticos, los beneficios de losartán fueron aún más pronunciados en todas las variables analizadas, sobre todo en un pequeño grupo de pacientes que no habían sido tratados por HTA antes del estudio (58). En este subgrupo de pacientes se observó una reducción del riesgo en la variable primaria del 24% (103 pacientes asignados a losartán y 139 asignados a atenolol, p=0.031). Además se observó una reducción significativa del 37% de riesgo de muerte cardiovascular (fallecieron 38 y 61 pacientes de los grupos de losartán y atenolol respectivamente, p=0.028) y una reducción del 39% del riesgo de muerte por cualquier causa (64 y 104 muertes, p=0.002). Estos hallazgos contrastan con los del estudio UKPDS, en el que se comparó el efecto de captopril y de atenolol en pacientes hipertensos diabéticos. En este estudio no se observaron diferencias significativas en morbi-mortalidad entre el IECA y el betabloqueante (19). Por tanto, los beneficios observados en el LIFE con un ARA lI, no observados antes con IECA, distinguen el efecto de estas dos clases farmacológicas.
También se ha realizado un subestudio del LIFE en el subgrupo de pacientes con hipertensión sistólica aislada, alrededor del 15% del total. Este subestudio fue publicado recientemente en JAMA y los resultados demostraron un beneficio aún mayor en esta población que en los diabéticos. La variable primaria se redujo en 25%, a punto de alcanzar significación estadística (p=0.06), el riesgo de ictus se redujo de forma significativa en un 40% y el de muerte cardiovascular en un 46%. Además losartán disminuyó la hipertrofia ventricular izquierda más que atenolol (p=0,001) y fue mejor tolerado (59).
Un análisis secundario del estudio LIFE examinó un aspecto muy relevante clínicamente: la influencia del control de PA sobre la regresión de la hipertrofia ventricular izquierda determinada por ecocardiografía, tras dos años de tratamiento antihipertensivo. Se realizaron controles ecocardiográficos al año y a los dos años y los resultados mostraron que si bien la PA disminuía significativamente durante el primer año, no se modificaba significativamente durante el segundo. Sin embargo, la regresión de la hipertrofia fue persistente y significativa durante los dos años, por lo que disminuyó la prevalencia de hipertrofia concéntrico y excéntrica y aumentó la proporción de pacientes con geometría ventricular normal. Esto muestra los beneficios adicionales más allá del efecto de reducción de PA y demuestra que la máxima regresión de la hipertrofia requeriría como mínimo dos años de tratamiento antíhipertensivo (60,61).
En los últimos meses se han publicado diversos subestudios del estudio LIFE que han puesto en evidencia los beneficios del tratamiento antihipertensivo sobre la función sistálica (62), la función diastálica (63), correlación de la presión de pulso durante el tratamiento antihipertensivo (64), correlación del tamaño de la aurícula izquierda (65), y la relación del índice albuminuria/creatinina con la función y estructura del ventriculo (66).
Más allá de todos estos hallazgos el resultado más importante del LIFE fue que por primera vez una clase farmacológica, los ARA II (en concreto losartán) se ha mostrado superior a otra clase de antihipertensivos (en este caso betabloqueantes, y en concreto atenolol). Probablemente el efecto sobre la PA no haya tenido mayor influencia en la incidencia de eventos cardiovasculares, y fundamentalmente de ictus, ya que en ambos grupos la PA fue muy similar. De hecho, la PA sistólica en el grupo de losartán fue 1.3 mmhg más baja que en el grupo de atenolol y la PA diastólica 0.4 mmhg más alta en la última vista realizada. Estos hallazgos nos llevan a que la presión de pulso final fue algo menor en el grupo de losartán. Este dato podría tener alguna implicación pronostica en la aparición de ictus, aunque difícilmente puede explicar los beneficios alcanzados con el ARA li, ya que la diferencia de presión entre ambos grupos es muy pequeña. Por otra parte, en el subgrupo de pacientes diabéticos, éstos tenían una mayor presión de pulso que la población general y sin embargo la incidencia de ictus se dio en un pequeño numero de pacientes y las diferencias entre los grupos de tratamiento no fueron significativas. Es interesante resaltar que en el grupo de pacientes randomizados a atenolol había 25 pacientes más con fibrilación auricular, lo que podría tener alguna influencia en la aparición de ictus durante el seguimiento.
Los mecanismos por lo que los ARA II han mostrado ser especialmente útiles en los pacientes de mayor riesgo no son bien conocidos. Quizá pueda influir el probable efecto beneficioso de estos fármacos en la disfunción endotelial y en los procesos de arterioscierosis. De todas maneras se ha sugerido que los resultados obtenidos en el LIFE podrían quizá ser extrapolados también a pacientes de bajo riesgo (67). En cualquier caso, en la realidad de la práctica clínica diaria en nuestro medio, es muy infrecuente la HTA de bajo riesgo. De hecho en un estudio recientemente publicado se demuestra que la mayoría de los pacientes hipertensos que acuden actualmente a la consulta de atención primaria en nuestro país son ya de riesgo alto o muy alto siguiendo la estratificación propuesta por la OMS-SIH de 1999 (68). Se ha sugerido que los beneficios observados con losartán pudieran ser superiores si se administrara una dosis constante de 100mg, ya que en el estudio LIFE menos del 50% alcanzaron esta dosificación y se ha visto que algunos ARA II tienen mayores beneficios a sus dosis máximas (69). Habría que señalar que la mayoría de los pacientes randomizados fueron de raza blanca y debido a la alta prevalencia de HTA en individuos de raza negra sería importante determinar si estos hallazgos pueden ser extrapolables a este grupo étnico.
El estudio SCOPE es el primer ensayo clínico realizado a gran escala para evaluar los efectos del tratamiento con un ARA II (candesartán) sobre eventos cardiovasculares mayores (infarto de miocardio, ictus y mortalidad cardiovascular) y función cognitiva en pacientes ancianos (70). Se trata de un estudio prospectivo, aleatorizado, doble ciego en el que se incluyeron 4.937 pacientes de ambos sexos de 70 a 89 años de edad (76 años de media), con HTA (PA sistólica 160-179 mmhg y/o diastólica 90/99 mmhg) y de riesgo cardiovascular principalmente medio y alto. Los pacientes se distribuyeron aleatoriamente a candersartán o placebo. Hay que destacar que debido a la necesidad de tratar la HTA en algunos pacientes y los cambios que han venido sucediendo en cuanto a los objetivos de control de PA, en el grupo placebo casi el 85% de los pacientes estaba con medicación antihipertensiva, por lo que realmente no puede considerarse que ese grupo de pacientes estuviera en placebo. Los resultados preliminares de este estudio fueron presentados en el último Congreso de la Sociedad Europea de HTA-Sociedad internacional de HTA (junio 2002) y están aún pendientes de publicación. Tras un seguimiento mínimo de 3 años se demostró una reducción no significativa en el riesgo de acontecimientos cardiovasculares mayores en pacientes tratados con ARA II. Sin embargo, sí se observó una reducción significativa del 28% del riesgo de ictus (p=0.04) en el grupo de pacientes tratados con candersartán. El tercer gran ensayo clínico en HTA con ARA II esta aún en marcha, es el estudio VALUE (71). Se trata de un estudio prospectivo, multicéntrico, randomizado, doble ciego, con dos ramas de tratamiento: amiodipino y valsartán. La hipótesis es que a los mismos niveles de control de PA, el ARA II sería más efectivo que amiodipino en disminuir la incidencia de infarto de miocardio, insuficiencia cardíaca congestivo y muerte cardíaca. El seguimiento del mismo será hasta que 1.450 pacientes experimenten alguna variable principal, y la previsión es que eso pueda ocurrir a finales del 2003. Se han incluido más de 15.000 hipertensos mayores de 50 años con PA sistólica 160-210 y/o diastólica 95-115 mmhg y riesgo cardiovascular alto o muy alto. De hecho, los pacientes que han sido incluidos en este estudio son una población de riesgo muy alto: 33% son dislipémicos, 32% de diabéticos, 24% fumadores y un alto número presentan enfermedad cardiovascular, 46% enfermedad coronaría, 20% con enfermedad cerebrovascular y 14% enfermedad vascular periférico (72). Teniendo en cuenta el número de pacientes y el elevado porcentaje de factores de riesgo de los mismos se espera una variada e importante información al finalizar este estudio.
Podemos decir como conclusión que a la buena eficacia y excelente tolerabilidad que han demostrado los ARA II en el tratamiento de la HTA se ha sumado un hecho trascendental como es la disminución de la morbi-mortalidad cardiovascular superior a la de otros fármacos de probada eficacia antihipertensiva. Es de esperar que en un futuro próximo las indicaciones de los ARA II sean más amplias que las actuales, en la medida que estos fármacos sigan demostrando sus beneficios en la protección cardiovascular más allá del simple efecto del control de PA
Bibliografía
1- Benegas JR , Rodríguez-Artalejo F , De la Cruz Troca JJ , Guallar-Castilión P , Del Rey Calero J. La presión arterial en España. Distribución, grado de conocimiento, control y beneficios de una reducción en los niveles medios de presión arterial. Hipertensión 1999; 32: 908-1.002. [ Links ]
2- González Juanatey JR, Alegria Ezquerra E, Lozano Vidal JV, llisterri Caro JL, García Acuña JM y González Maqueda I. Impacto de la hipertensión en las cardiopatías en España. Estudio CARDIOTENS 1999. Rev Esp Cardiol 2001; 54: 139-149. [ Links ]
3- Ministerio de Sanidad y Consumo y Sociedad -Liga Española de Hipertensión arterial. Consenso para el control de la presión arterial en España. Madrid, 1996.
4- Joint National Committee on prevention, detection, evaluation and treatment of high blood pressure. The sixth report of the Joint National Committee on detection, evaluation, and treatment of high blood pressure (JNC-VI). Arch lntern Med 1997; 157: 2313-2446. [ Links ]
5- Guidelines Subcommíttee. 1999 Worid Health Organization lnternational Society of Hypertension guidelines for the management of hypertension. J Hypertens 1999; 17: 151-183. [ Links ]
6- Barrios V, Ruilope LM. Hipertension with left ventricular hypertrophy/diastolic dysfunction. En: Sleight P, Bakris G, Mancia G, Opie FML, eds. Clinica cases in hypertension. Specific treatment strategies. II. Richmond upon Thames (Reino Unido): PAN Communications, 2000; 16-22 [ Links ]
7- Laragh LH, Sealy JE. The renin-angiotensin-aldosterone system in hypertensive disorders: a key to two forms of arteriolar vasoconstriction and a possible clue to risk of vascular injury (heart attack and stroke) and prognosis. En: Laragh JH, Brenner BM, eds. Hypertension: pathophysiology, diagnosis and management. Nueva York: Raven Press, 1990: 1329-1348. [ Links ]
8- Zitnay C, Siragy HM. Action of angiotensin receptor subtypes on the renal tubules and vasculature: implications for volume homeostasis and atheroscierosis. Miner Electrolyte Metab 1998; 24: 362-370. [ Links ]
9- Bermam MA, Waih MF, Sowers JR: Angiotensin II biochemistryan physiologhy. Update on angiotensin II receptor blockers. Cardiovasc Rev 1997; 15: 75-100. [ Links ]
10- Mac Mahon S, Rodgers A. The effects of blood pressure reduction in older patients: an overview of five randomised controlled trials in elderly hypertensives. Clin Exp Hypertens 1993; 15: 967-978.
11- Neal B, Mac Mahon S, Chapman N et al. Effects of ACE inhibitors, calcium antagonists and other blood-pressure-iowering drugs: results of prospectively designed overviews of randomised trials. Blood Pressure lowering Treatment Trialists Collaboration. Lancet 2000; 356:1955-1964. [ Links ]
12- Maschio G, Alberti D, Janin G et al. The angiotensinconverting-enzyme inhibition in progressive renal insufficiency Study Group. N Engl J Med 1996; 334: 939-945. [ Links ]
13- Pfeffer MA, Braunwald E, Moyé LA, Basta L, Brown EJ, Cuddy TE, et al. on behalf of the SAVE lnvestigators. The effect of captopril of morbidity and mortality in patients with left ventricular dysfunction following myocardial infarction. Results of the Survival and Ventricular Enlargement (SAVE) trial. N Engl J Med 1992; 327: 669-677. [ Links ]
14- The Heart Outcomes Prevention Evaluation study investigators. Effects of an angiotensin-converting enzyme inhibitor, ramipril, on cardiovascular events in high risk patients. N Engl J Med 2000; 342: 145-153 [ Links ]
15- The SOLVD lnvestigators. Effect of enalapril on mortality and the development of heart failure in asymptomatic patients with reduced left ventricular ejection fraction. N Engl J Med 1992; 327: 685-691. [ Links ]
16- Lewis EJ, Hunsicker LG, Bain RP, Rohde RD. The effect of angiotensin-converting-enzyme inhibition on diabetic nephropathy: The Collaborative Study Group. N Engl J Med 1993; 329:1456-1462. [ Links ]
17- PROGRESS Collaborative Group. Randomised trial of a perindopril-based blood-pressure-iowering regimen among 6.105 individuas with previous stroke or transient ischaemic attack. Lancet 2001; 358: 1033-1041. [ Links ]
18- Hansson L, Lindholm LH, Niskanen L , Lanke J , Hedner T , Nikiason A , Luomanmaki K , Dahioff B , de Faire U , Morlin C , Kariberg BE , Wester PO , Bjorck J-E. Effect angiotensin-convertingenzyme inhibition compared with convencional therapy on cardiovascular morbidity and mortality in hypertension: the Captopril Prevention Project (CAPPP) randomised trial. Lancet 1999; 353: 61 l616.
19- UK Prospective Diabetes Study Group. Efficacy of atenolol and captopril in reducing risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 39. BMJ 1998; 317: 713720. [ Links ]
20- Hansson L, Lindhoim LH, Ekbom T, Dahioff B, lanke I, Schersten B, Wester PO, Hedner T, de Faire U. Randomised trial of old and new antihypertensive drugs in elderiy patients: cardiovascular mortality and morbidity the Swedish Trial in Old Patients with Hypertension-2 study. Lancet 1999; 354: 1751-1756
21- Barrios V, Jimenez JJ. Corazón e hipertensión. En: RuilopeLM, ed. Nuevas fronteras en hipertensión. Barcelona: Doyma, 1998; 3: 29-63. [ Links ]
22- Ruilope LM, Barrios V. Pharmacologic treatment in hypertensive heart disease. En: Crawford MH, Di Marco JP, eds. Cardiology. London: Mosby, 2001; 8.1-8.8. [ Links ]
23- lsraili ZH, Hall WD. Cough and angioneurotic edema associated with angiotensin-converting-enzyme inhibitor therapy: a review of the literature and pathophysiology. Am Intern Med 1992., 117: 234242. [ Links ]
24- Bloom BS. Continuation of initial antihypertensive medication after 1 year of therapy. Clin Ther 1998; 20: 671-681. [ Links ]
25- Conlin PR, Gerth WC, Fox J, Roehm JB, Boccuzzi SJ. Four-year persistence patterns among patients initiating theraphy with the angiotensina II receptor antagonist losartán versus other antihypertensive drug classes. Clin Ther 2001; 23: 1999-2010. [ Links ]
26- Paster RZ, Snavely DB, Swett AR, Draper RA, Goldberg Al, Soffer BA, Swett CS. Use of losartan in the treatment of hypertensive patients with a history of cough induced by angiotensin-converting-enzyme inhibitors. Clin Ther 1998; 20: 978-989. [ Links ]
27- Black HR, Graff A, Shute D, Stoltz R, Ruff D, levine J, Shi Y, Mallows S: Valsartan, a new angiotensin II antagonist of the treatment of essential hypertension. Efficacy, tolerability and safety compared to an angiotensin inhibitor. lisinopril. J Hum Hypertens 1997; 11: 483-489. [ Links ]
28- Belcher G, Hubner R, George M, Elmfeldt D, lunde H: Candersartan cilexetil: Safety and tolerability in healthy volunteers and patients with hypertension. J Hum Hypertens 1997; 1 1: 585-589. [ Links ]
29- Barrios V, Navarro A, Esteras A, Luque M, Romero J, Tamargo, J, Prieto L, Carrasco JL, Herranz I, Navarro-Cid J and Ruilope LM. Antihypertensive efficacy and tolerability of lercarnidipine in daily clinical practice. The ELYPSE study. Blood Pressure 2002; 11: 95-100 [ Links ]
30- Sever R Candersartan cilexetil: A new, long-acting, effective angiotensin II type 1 receptor blocker. J Hum Hypertens 1997; 11 (suppl 2): 591-595. [ Links ]
31- Johnston Cl. Angiotensin receptor antagonist: focus on losartan. Lancet 1995; 346: 1403-1407. [ Links ]
32- Gillis JC, Markham A. irbesartan: A review oí its pharmacodynamic and pharmacokinetic properties and therapeutic use in the management of hypertension. Drugs 1997; 54: 885-90. [ Links ]
33- Markham A, Goa KL. Valsartan: A review of its pharmacology and therapeutíc use in essential hypertension. Drugs 1997; 54: 299-311. [ Links ]
34- Black HR, Graff A, Shute D, Stoiz R, Ruff D, levine J, Shi Y, Mallows S: Valsartan, a new angiotensin II antagonist for the treatment of essential hypertension. Efficacy, tolerability and safety compared to an angiotensin- converting enzyme inhibitor, lisinopril. J Hum Hypertens 1997; 11: 483-489. [ Links ]
35- Tikkanen I, Omvik P, Jensen HA, for the Scandinavian Study Group: Comparison of the angiotensin II antagonist losartan with the angiotensin converting enzyme inhibitor enalapril in patients with essential hypertension. J Hypertens 1995; 13: 1343-1351. [ Links ]
36- Mimran A, Ruilope LM, Kerwin L, Nys M, Owens D, Kassler-Taub K, Osbakken M: A randomised, double blind comparison of the angiotensin II receptor antagonist irbesartan, with the full dose range of enalapril for the treatment of mild-to-moderate hypertension. J Hum Hypertens 1998; 12: 203-208. [ Links ]
37- Kariberg BE, Lins LE, and Hermansson K, for the TEES Study Group. Efficacy and Safety of Teimisartan, a selectiva AT I receptor antagonist, compared with enalapril in ederly patients with Primary hypertension. J Hypertens 1999; 17: 293-302. [ Links ]
38- Dahiof B, Keller S, Makris L, Goldberg Al, Sweet CS, Lim NY: Efficacy and tolerability of losartan potassium and atenolol in patients with mild or moderate essential hypertension. Am J Hypertens 1995; 8: 578- 583.
39- Corea L, Cardoni O, Fogari R, lnnocenti P, Porcellati C, Providenza M, Meilenbrock S, Sullivan J, Bodin F: Valsartan, a new angiotensin II antagonist for the treatment of essential hypertension. A comparative study of the efficacy and safety agonist amiodipine. Clin Pharm Ther 1996; 60: 341-346. [ Links ]
40- Lombera F, Barrios V, Soria F, Placer L, Cruz JM, Tomás L, et al. Guías de práctica clínica de la Sociedad Española de Cardiología en hipertensión arterial. Rev Esp Cardiol 2000; 53: 66-90. [ Links ]
41- American Diabetes Association. Diabetic nephropathy. Diabetes Care 2002; 25(Suppl): S85-S89. [ Links ]
42- Kassier-Taub K, Little John T, Elliott W, Ruddy T, AdLer E: Comparative efficacy of two angiotensin II receptor antagonists, irbersartan and losartan, in mild to moderate hypertension. Am J Hypertens 1998; 11: 445- 453. [ Links ]
43- Andersson OK, Neldom S: The antihypertensive effect and tolerability of candersartan cilexetil, a new generation angiotensin II antagonist, in comparison with losartan. Blood Press 1998; 7: 53-59. [ Links ]
44- Oparil S. Comparative antihypertensive efficacy of olmesartan: comparison with other angiotensin II receptor antagonists. J Hum Hypertens 2002; 16(suppl 2): 17-23. [ Links ]
45- Conlin P, Spence B, Ribeiro A, Saito I, Benedict C, Bunt M. Angiotensin II antagonist for hypertension: Are there differences in efficacy? Am J Hypertens 2000; 13: 418- 426. [ Links ]
46- Hansson L, Lindhoim LH, Niskanen L, Lanke J, Hedner T, Niklason A, Luomanmaki K, Dahiof B, de Faire U, Morlin C, Kariberg BE, Wester PO, Bjorck J-E. Effect angiotensin-converting-enzyme inhibition compared with convencional therapy on cardiovascular morbidity and mortality in hypertension: Captopril Prevention Project (CAPPP) randomised trial. Lancet 1999; 353: 611-616.
47- Brown MJ, Palmer CR, Castaigne A, de Leeuw PW, Mancia G, Rosenthal T, Ruilope LM. Mordidity and mortality in patients randomised to double-blind treatment with a long-acting calcium-channel blocker or diuretic in the internacional Nifedipine GITS study: lntervention as a goal in hypertension Treatment (INSIGHT). lancet 2000; 356: 366-372. [ Links ]
48- Hansson L, Hedner T, Lund-Johansen P, Kjeidsen S, Lindhoim LH, Syvertsen JO, Lanke J, de Faire U, Dahiof B, Kariberg BE. Randomised trial of effects of calcium antagonists compared with diuretics and Beta-blockers on cardiocascular morbidity and morbility in hypertension: the Nordic Diltiazem (NORDIL) study. Lancet 2000; 356: 359-365. [ Links ]
49- Hansson L, Lindholm LH, Ekbom T, Dahiof B, Lanke J, Schersten B, Wester P-O, Hedner T, de Faire U. Randomised trial of old and new antihypertensive drugs in elderly patients: cardiovascular mortality and morbidity the Swedish Trial in Old Patients with Hypertension-2-study. Lancet 1999; 354:1751-1756.
50- Lewis EJ, Hunsicker LG, Ciarke WR, Beri T, Pohi MA, Lewis JB, Ritz E, Atkins RC, Rohde R, Raz I. Collaborative Study Group. Renoprotective effect of the angiotensin-receptor antagonist irbesartan in patients with nephropathy due to type 2 diabetes. N Engl J Med 2001; 345: 851-860.
51- Brenner BM, Cooper ME, de Zeeuw D, Keane WF, Mitch WE, Parving HH, Remuzzi G, Snapinn SM, Zhang Z, Shahinfar S. Effects of losartan on renal and cardiovascular outcomes in patients with type 2 diabetes and nephropathy. N Eng J Med 2001; 345: 861-869. [ Links ]
52- Dahlof B, Devereux RB, Kjeidsen SE, et al. Cardiovascular morbidity and mortality in the Losartan Intervention For Endpoint reduction in hypertension study (LIFE): a randomised trial against atenolol. Lancet 2002; 359: 995-1003. [ Links ]
53- Dahlof B, Devereux RV, Julius S, et al. Characteristics of 9.194 patients with left ventricular hypertrophy: the LIFE Study. Hypertension 1998; 32: 989-97 [ Links ]
54- Dahlof B, Devereux RB, de Faire U, et al The losartan lntervention For Endpoint reduction (LIFE) in hypertension study: rationale, design, and methods. Am J Hypertens 1997; 10: 705-713. [ Links ]
55- Dahlof B, Keller SE, Makris L, Goldberg Al, Sweet CS, Limn NY. Efficacy and tolerability of losartan potassium and atenolol in patients with mild to moderate essential hypertension. Am J Hypertens 1995; 8: 578-83 [ Links ]
56- Dahlof B, Lindhoim LH, Hansson L, Schersten B, Ekbom T, Wester PO Morbidity and mortality in the Swedish Trial in Old Patients with Hypertension (STOP-Hypertension). Lancet 1991; 338: 1281-1285 [ Links ]
57- Kjeldsen SE, Dahlof B, Devereux RB, Julius S et al for the LIFE Study Group. lowering of blood pressure and predictors of response in patients with left ventricular hypertrophy: the LIFE Study. Am J Hypertens 2000; 13: 899-906. [ Links ]
58- Lindholm LH, lbsen H, Dahlof B, Devereux RB, Beevers G, de Faire U, et al. Cardiovascular morbidity and mortaity in diabetics patients of the LIFE study: a randomised trial against atenolol. Lancet 2002; 359: 1004-1010. [ Links ]
59- Kjeldsen S, Dahlof B, Devereux R, Julius S, Aurup P, Edelman J, Beevers G, de Faire U, Fyhrquist F, lbsen H, Kristianson K et al for the LIFE study. Effects of losartán on cardiovascular morbidity and mortality in patients with isolated systolic hypertension and left ventricular hypertrophy. A Losartán lntervention For Endpoint Reduction (LIFE) Substudy. JAMA 2002; 288: 1491-1498
60- Devereux RB, Palmieri B, Liu J, Wachtell C, Bella J, Boman K, Gerdts E, Nieminen M, Papademetriou V and Dahlof B. Progressive hypertrophy regression with sustained pressure reduction in hypertension: the Losartan lntervention For Endpoint Reduction study. J Hypertens 2002; 20: 1445-1450. [ Links ]
61- Dahiof B, Zanchetti A, Diez J, Nicholis MG, Yu CH-M, Barrios V, Aurup P, Smith R, Johansson M, for the REGAAL Study Investigators. Effects of losartan and atenolol on left ventricular mass and neurhormonal profile in patients with essential hypertension and left ventricular hypertrophy. J Hypertens 2002; 20: 1855-1864.
62- Wachtell K. Change in systolic left ventricular performance after 3 years of antihypertensive treatment: LIFE Study. Circulation 2002; 106: 227-32. [ Links ]
63- Wachtell K. Change in diastolic left ventricular filling after one year of antihypertensive treatment: LIFE Study. Circulation 2002; 105: 1071-1076. [ Links ]
64- Gerdts E. Correlates of pulse pressure reduction during antihypertensive treatment (losartan or atenolol) in hypertensive patients with electrocardiographic left ventricular hypertrophy (the LIFE Study). Am J Cardiol 2002; 89: 399- 402. [ Links ]
65- Gerdts E. Correlates of left atrial size in hypertensive patíents with left ventricular hypertrophy: LIFE Study. Hypertension 2002; 39: 739-743 [ Links ]
66- Wachtell K. Microalbuminuria in hypertensive patients with electrocardiographic left ventricular hypertrophy: the LIFE Study. J Hypertens 2002; 20: 405-412. [ Links ]
67- Brunner HR, Gavras H. Angiotensin blockade for hypertension: a promise fulfilled. Lancet 2002; 359: 990-992. [ Links ]
68- Barrios V, Campuzano R, Peña G, Guzmán G, Ruilope LM. Estratificación del riesgo cardiovascular en hipertensión en Atención Primaria e impacto sobre el tratamiento antihipertensivo. Estudio DIORISC. Hipertensión 2002; 19: 114-120. [ Links ]
69- Parving HH, Lehnert H, Brochner-Mortensen J, Gomis R, Andersen S, Arner P. lrbesartan in Patients with Type 2 Diabetes and Microalbuminuria Study Group. The effect of irbesartan on the development of diabetic nephropathy in patients with type 2 diabetes. N Engl J Med 2001; 345: 870-878. [ Links ]
70- Hansson L, Lithell H, Skoog L, Baro F, Bánki CM, Breteler M et al. Study on Cognition and Prognosis in the Elderly (SCOPE): baseline characteristics. Blood Press 2000; 9: 146-151. [ Links ]
71- Mann J, Julius 5, for the VALUE Trial Group. The Valsartan Antihypertensive long-term. Use Evaluation (VALUE) trial of cardiovascular events in hypertension. Rationale and design. Blood Press 1998; 7: 176-183.
72- Kjeldsen SE, Julius S, Brunner H, Hansson L, Henis M, Ekman S, Laraght J, Mc lnnes G, Smith B, Weber M, Zanchetti A. Characteristics of 15314 hypertensive patients at high coronary risk. The VALUE trial. The Valsartan Antihypertensive Long-term Use Evaluation. Blood Press 2001; 10: 83-91. [ Links ]
* Servicio de Cardiología, Hospital Ramón y Cajal, Madrid, España.
** Unidad de Hipertensión. Hospital 12 de Octubre, Madrid, España.
Dirección para correspondencia:
Ctra. de Colmenar, km 9.100. 28034 Madrid, España.
e-mail: vbarriosa@meditex.es














