Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Cardiología
Print version ISSN 1409-4142
Rev. costarric. cardiol vol.3 n.1 San José Apr. 2001
Utilidad del ecocardiograma transesofágico en el intra y post operatorio de cirugía cardíaca
Dr. Miguel Tibaldi*, Dr. Luis Lema*, Dr. Marcelo Coll*, Dr. Daniel Boccardo*
Resumen
Objetivos: Analizar la utilidad del Ecocardiograma Transesofágico (ETE) en la asistencia al cirujano y al cardiólogo recuperador para la toma de decisiones.
Material y Métodos: Se analizaron retrospectivamente 147 pacientes (p) que requirieron ETE, 110 p (75%) eran hombres con una edad media de 63 años (21-88). Los procedimientos quirúrgicos realizados fueron: By Pass Ao. Co: 70p, reemplazo valvular (RV): 50p, Combinados: 5p, disección aórtica 8p, transplante cardíaco 5p, cierre de CIV: 2 p, aneurismectomía: 2p, extirpación de mixomas: 2p, miectomía: 1p, tromboendarterectomía: 1p y bicavo pulmonar anastomosis: 1p.
Se dividió la muestra en 2 grupos: Grupo A: ETE intraoperatorio 104p (70.7%) y Grupo B ETE postoperatorio 43p (29.3%). Las indicaciones fueron: Grupo A: p con dificultad para retirar de circulación extracorpórea (CEC) (A1) 49p, y p para control de procedimiento (pr) (A2) 55p, 24 de los cuales con plástica valvular (plv).
Grupo B: p con bajo débito (B1) 25p de los cuales 12 presentaban signos de taponamiento (t).
Y p con signos de isquemia perioperatoria 18p.
Se utilizó el test X2 para comparar variables categóricas.
Resultados: Grupo A1: se detectó alteraciones de la motilidad global o regional en 41p, disfunción protésica en 4p, insuficiencia mitral 1p y obstrucción medio ventricular en 3p.
Grupo A2: el ETE indicó 5 RV post plv y 4 RV no programados controlando correctamente el resto de los pr.
Grupo B1: de los 12 p con signos de t, el ETE lo confirmó en 6 (50%), y de los restantes p con Bajo Gasto Cardíaco (BGC) detectó t en 3p.
Grupo B2: en 15p se detectó trastornos segmentarios de la motilidad requiriendo nueva revascularización.
Se consideró como parámetro de utilidad del ETE a los hallazgos que condicionaron un cambio de conducta, presentando una utilidad del 67% en ésta muestra. La mortalidad en el grupo de pacientes en los cuales el ETE produjo un cambio de conducta (98p), obitaron 10 (10%) y en los que no sugirió cambios (39p) obitaron 11 (22%) p=0.04.
Conclusión: El ETE intra y post-operatorio constituye una herramienta valiosa para la toma de decisiones quirúrgicas y el manejo post operatorio, mejorando el pronóstico de esta población de pacientes de alto riesgo.
Palabras Clave: Ecocardiograma Transesofágico, Cirugía Cardíaca, Ecocardiograma Intraoperatorio.
Summary
Objetives: To analize how useful is the TEE to assist the surgeon and recover-room cardiologist in decision making.
M. and M.: 147 patients who required TEE were analysed. 110 p (75%) were male, with a mean ages of 63 (21-88). The surgical procedures were: coronary artery by pass 70p, valvular replacement (VR) 26p, valvular plastic repair (vpl) 24p, combined procedures 5p, aortic disection 8p, cardiac transplant 5p, closure of ventricular septal defect 2p, aneurysmectomy 2p, myxoma resection 2p, myectomy 1p, thromboendarterectomy 1p and bicavo pulmonary anastomosis 1p.
The patients were divided into 2 groups: Group A: intraoperative TEE 1-4p (70.7%) and Group B: postoperative TEE 43p (29.3%). The indications were: Group A p unable to wind them off from extracorporeal circulation (ECC) (A1) 49p, and p who needed procedure control (A2) 55p. Group B: p with low cardiac output syndrome (B1) 25p, 12 of whom presented signs of tamponade and 18p with perioperative ischemia (B2).
The chi square test has used to compare categorical variables.
Results: Group A1 regional or global wall motion abnormalities (WMA) were detected in 41p, prosthetic dysfuntion in 4p, mitral insuffiency in 1 p and mid ventricular obstruction in 3p.
Group A2: 5 valvular replacement were indicated post vpl, 4 replacement were non programmed and the other procedures were correctly controlled.
Group B1: out of 12p with signs of tamponade, the TEE confirmed 6 (50%) and detected 3 in p with low cardiac output.
Group B2: WMA were seen in 15p, who required re-operation and more complete revascularization.
The TEE was considered useful if the findings produced a change in attitude, wich was the case in 67% of the cases. The mortality was less than 10% (10p out of 98p) in the group were there was a change in attitude due to findings of the TEE, while 11p out of 39p died in the group where there was no change due to the TEE findings. (p=0.04).
Conc: the intra and post operative TEE is a valuable tool in surgical and post operation decision making, improving the prognosis in this high risk population.
Key Words
Transesophageal Echocardiogram, Cardiac Surgery, Intraoperative Echocardiogram.
Introducción
La ecocardiografía Doppler se ha convertido en una herramienta imprescindible en el diagnóstico cardiológico actual. Pocas técnicas han experimentado un desarrollo semejante y/o aportan tanta información de tipo anátomo funcional en forma tan rápida y no invasiva.
El ecocardiograma fue introducido en los quirófanos en 1970 aplicándose directamente el transductor sobre el epicardio una vez abierto el tórax (1). La ventaja se notó en la mejoría de la calidad de las imágenes al no existir interferencia alguna. Sin embargo, las limitaciones no eran pocas: riesgo de contaminación, exploración limitada en el tiempo, interrupción del acto quirúrgico, distracción del cirujano, inestabilidad de imagen y dificultad para explorar las estructuras posteriores como, por ejemplo, las venas pulmonares.
El desarrollo de la ecocardiografía intraesofágica nace por inquietud de los anestesistas, a quienes les interesaba conocer y monitorizar la función ventricular, tanto en la inducción anestésica, como a la salida de la circulación extracorpórea, para lo cual montaron transductores sobre fibroscopios como los usados en gastroenterología. Las primeras sondas transesofágicas datan de 1982. (2-3-4)
El desarrollo tecnológico pasó de las sondas con registros monoplanares, a las actuales que son de tamaño más reducido y con posibilidad de cortes biplanares, multiplanares y exploración Doppler en sus formas pulsado, color y continuo direccional, Doppler tisular, segunda armónica, etc. Todo lo anterior ha convertido al eco transesofágico (ETE) en un examen semiinvasivo, rápido y seguro, aplicable al paciente ambulatorio, con algunas ventajas informativas no comparables. (5)
Con el desarrollo de técnicas quirúrgicas como las plásticas valvulares, la cirugía de Ross, las válvulas sin anillo de anclaje, la cirugía en ventrículos con muy baja fracción de eyección, la revascularización empleando múltiples puentes arteriales, etc., el ETE ha sido requerido por los equipos quirúrgicos en numerosas circunstancias específicas, brindando información exacta y a la vez precoz de maniobras quirúrgicas, cambios de actitudes y conductas, o planeando directamente la metodología a seguir, y beneficiar a pacientes generalmente en un estado crítico. (6-7)
El fallo hemodinámico postoperatorio es una complicación no infrecuente y grave, con una elevada morbimortalidad. El taponamiento cardíaco, es una complicación frecuente que sólo en un 50% de los casos se traduce en hallazgos hemodinámicos típicos. El síndrome de bajo débito presente hasta en un 15% de los postoperatorios, que si es expresión de una disfunción ventricular severa se asocia a una mortalidad cercana al 40%. La hipovolemia es una situación ocasionalmente difícil de discernir en pacientes en condiciones críticas, como así también las disfunciones protésicas agudas o las restricciones en el llenado ventricular por hipertrofia concéntrica severa, situación que puede agravarse por el empleo de inotrópicos. (8-9-10)
En estos pacientes la utilidad de la información anátomo funcional que aporta la visión ecográfica no es discutible, pero en la mayoría de los casos la inmovilidad, los vendajes, la intubación e insuflación del respirador, los tubos de drenajes, etc., hacen que el eco convencional pocas veces cuente con una ventana adecuada, reduciendo la confiabilidad de los datos recogidos. Una vez más, el ETE se convierte en una ayuda de primera mano en el control de estos pacientes, brindando información la mayoría de las veces de valor superior a la otorgada por el mismo monitoreo hemodinámico invasivo.
El objetivo de este trabajo es analizar la utilidad del ETE en la asistencia, tanto del cirujano cardiovascular como del cardiólogo encargado de la recuperación postoperatoria y las ventajas del método en un grupo de pacientes críticos.
Material y métodos
Se realizaron 147 ETE en las salas de cirugía y postoperatorio usando un equipo ATL UM6 con sonda monoplanar de 5 Mhz y posibilidades de Doppler pulsado y color, y otro VINGMED CFM 800 con sonda multiplanar 3.5 a 5 Mhz con capacidad para Doppler color pulsado y continuo dirigible. Los estudios se registraron en video con el primer equipo y en video y digitalización de imágenes con el segundo.
Durante la evaluación en quirófano, la sonda la pocisionó el anestesista con el paciente ya dormido e intubado, generalmente antes de la toracotomía y en otras a la salida de la CEC. En la sala de postoperatorio con el paciente intubado o no, previa sedación con propofol.
En total, la muestra incluye 147 pacientes (p) con una edad media de 63 años (21-88), siendo 110 hombres y 37 mujeres.
El ETE fue requerido en las siguientes circunstancias: I) Intraoperatorio (grupo A): Pacientes con dificultad para retirarlos de circulación extracorporea (CEC) y/o para control del procedimiento quirúrgico practicado y II) En sala de recuperación cardiovascular (grupo B) en pacientes con Síndrome de bajo volumen minuto e isquemia post operatoria.
Grupo A: Fueron 104 pacientes (p) (70.7%) de los cuales 49 p (47%) presentaban dificultad para retirarlos de CEC (Sub grupo A1),de estos 38p (77.5%) con By Pass Aorto coronario (BPAC), 6p (12.2%) valvulares, 4p (8.2%) combinados y 1p (2.1%) transplante cardíaco (TC). (gráfico 1)
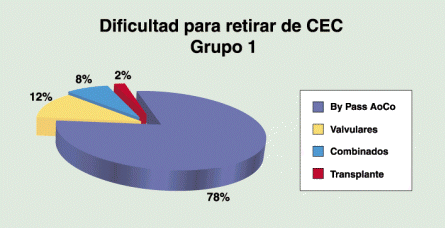
Gráfico 1:Procedimientos quirúrgicos en pacientes con dificultad para retirar de Circulación Extracorpórea
En 53 p (53%) se realizó el ETE para control del procedimiento practicado (Sub grupo A2) e incluyó: 24p (43%) con plásticas valvulares, 21 de la válvula mitral y 3 de la aórtica, 8 p con reemplazo valvulares, 5p (9%) se efectuó control de patología valvular asociada, 8p (14.5%) con disección aórtica, y 10p (19%) con procedimientos varios: 2p con cierre de comunicación interventricular (CIV) post infarto, uno de ellos con reemplazo de válvula mitral (RVM), 2p con mixoma de aurícula izquierda, 1p con miectomía septal y RVM, 2p con TC, 1p tromboendarteréctomia pulmonar, 1p con aneurismectomía y 1 p con anastomosis bicavo pulmonar y plástica atrial derecha. (gráfico 2)
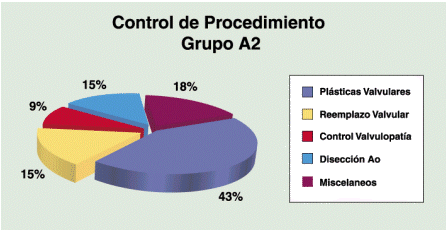
Gráfico 2: Procedimientos quirúrgicos donde se requirió ETE para evaluar la técnica quirúrgica efectuada
Grupo B: Fueron 43p; que incluye 31p (72%) en postoperatorio de BPAoCo, 8p (18%) de RV, 2p (5%) de Transplante Cardíaco, 1p (2.5%) de aneurismectomía +RVM, 1p (2.5%) con cirugía combinada. (gráfico 3)
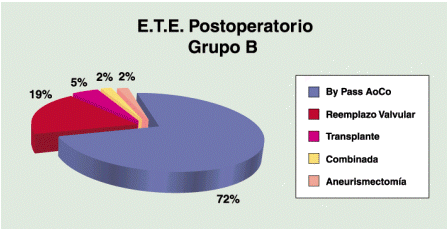
Gráfico 3: Procedimientos quirúrgicos realizados en los pacientes en la sala de recuperación.
Se dividió al grupo de acuerdo al motivo por el cual se solicitó el ETE: Sub grupo B1: 25p (58%) con diagnóstico de síndrome de bajo volumen minuto (Signos clínicos+IC<2.2) 12 de los cuales presentaban parámetros hemodinámicos de taponamiento cardíaco (TAM <60, igualamiento de presiones, índice AD/AI 0.8) y 13p sin tales parámetros. Sub grupo B2 18p (42%) con signos de isquemia perioperatoria (ST supradesnivelado, TV o Trastornos de conducción agudos+bajo gasto cardíaco).
Se utilizó el test X2 para el análisis estadístico de las variables categóricas.
Resultados:
Grupo A: ETE intraoperatorio
Sub grupo A1 en 41 p (83.6%) el ETE detectó alteraciones de la motilidad, de los cuales en 29 p (71%) la alteración fue global: indicando en 11 p inotrópicos, en 16 p inotrópicos+balón de contrapulsación aórtica (BCPAo) y en 2p la indicación fue administrar volumen. En los 12p restantes (29%) el ETE evidenció trastornos segmentarios de la motilidad parietal: en 9p se realizó un nuevo puente venoso (PV) a la arteria que involucraba el segmento comprometido y en 3p se un realizó nuevo PV+apoyo con BCPAo. En 4p el ETE detectó disfunción protésica como causa de imposibilidad para retirar de CEC, 3 p con hemidisco trabado (Fig 1-2) y 1p con leak periprotésico severo, los cuales pudieron solucionarse en el mismo acto. En 1 p se comprobó IM severa post aneurismectomía de cara lateral y se reemplazó la válvula mitral. En 3p se objetivó obstrucción dinámica medio ventricular debido a severa hipertrofia ventricular izquierda, indicándose en 2 de ellos retirar inotrópicos y administración de volumen y en el restante se agregó también infusión con ß-bloqueantes. (gráfico 3)
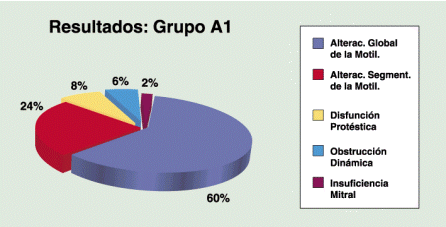
Gráfico 4: Hallazgos del ETE en pacientes con dificultad para retirar de Circulación Extracorpórea
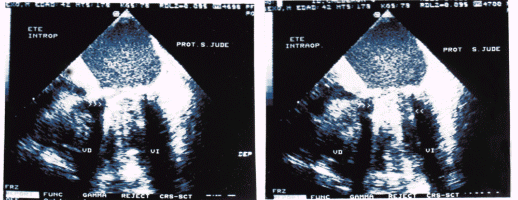
Fig 1: a) ETE intraoperatorio. Paciente con imposibilidad para retirar de CEC. Prótesis mecánica en posición mitral durante la sístole la prótesis está cerrada (flechas), b) en la diástole se abre un hemidisco mientras el izquierdo permanece cerrado (flechas)
Fig 2 y 3: Vista transgástrica por ETE, donde se observa hipocinesia global de paredes del VI
En este grupo 40 p (98%) luego de las medidas guiadas por ETE pudieron ser retirados con éxito de CEC y 1 p (2%) obitó en el quirófano.
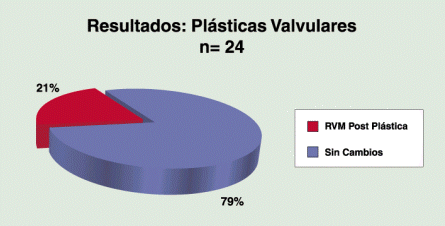
Sub grupo A2: en 55p (52%) el ETE fue solicitado para controlar el procedimiento realizado: de 24p (43.5%) con plásticas valvulares en 5p luego del examen se indicó reemplazo valvular al constatarse un fracaso en el procedimiento (Gráfico 5).
En 5 p en los cuales se solicitó el ETE para evaluar el comportamiento post quirúrgico de una válvula nativa que no motivó la cirugía, se encontró: en 3 p con reemplazo aórtico se valoró la válvula mitral y se indicó el reemplazo de ésta, 1p con BPAoCo se valoró una IM pero no fue necesario el reemplazo ya que mejoró con la revascularización. En el p restante con reemplazo mitral se evaluó la válvula aórtica y se indicó también su recambio al objetivar insuficiencia severa.
En 8p (14.5%) el ETE verificó el comportamiento del reemplazo valvular, (5 con prótesis Stenless, 2 con prótesis mecánicas y una cirugía de Donald Ross).
En 4p el ETE puso en evidencia la presencia de un flap íntimo medial traumático post canulación aórtica que fueron solucionados exitosamente y en otros 4p con hematomas disecantes aórticos evaluó el resultado post operatorio.
Dentro del subgrupo misceláneas que fueron10p (18%), en 1p se detectó un shunt residual por cierre de CIV post IAM el cual fue corregido; controló la extirpación total de los mixomas en 2 p, evaluó la desobstrucción del tracto de salida del VI en la miectomía septal, comprobó la permeabilidad de la rama pulmonar derecha post tromboendarterectomía, y evaluó el funcionamiento post bomba de la circulación venosa-pulmonar en una anastomosis bi cavo pulmonar.
Grupo B: ETE en la sala de recuperación
Sub grupo B1: 25p (58%) con síndrome de bajo gasto cardíaco, en 12p con parámetros hemodinámicos de taponamiento cardíaco, confirmó la sospecha diagnóstica en 6 (50%) los que fueron reintervenidos, y en los restantes 6 p descartó taponamiento y objetivó: disfunción de VD en 2p sugiriendo la administración de volumen y continuar con inotrópicos; en 2p con hipocinesia global se indicó continuar con inotrópicos; en 1p diagnosticó hipertensión pulmonar con IT severa indicando inotrópicos y vasodilatadores y en el restante p se objetivó función sistólica normal y derrame pericárdico leve sin cambios de conducta post ETE. (gráfico 6)
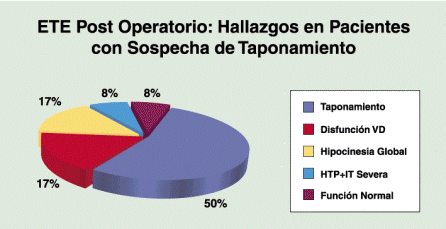
Gráfico 6: Hallazgos del ETE en pacientes con signos hemodinámicos de taponamiento
Los p con bajo gasto cardíaco pero sin parámetros de taponamiento (13p 52%) 3 presentaron derrame pericárdico con signos ecocardiográficos de taponamiento y fueron reintervenidos, en 1p con transplante cardíaco detectó un hematoma retroauricular izquierdo y la conducta fue expectante; en 7p se detectó disfunción ventricular izquierda y se continuó con soporte inotrópico y/o mecánico, 1p mostró hipocinesia global leve ligada a una sepsis y 1p con buena función de VI e hipercontractilidad superó el cuadro con la indicación de volumen. (Gráfico 7)
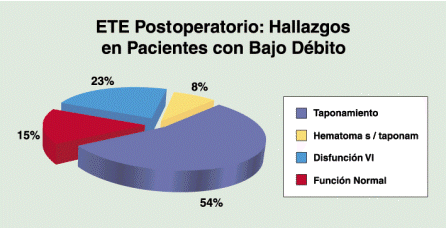
Gráfico 7: Utilidad del ETE en pacientes con bajo débito en el post operatorio
Sub grupo B2:Entre los pacientes con sospecha de isquemia post operatoria (18p 42%), 3 no presentaron trastornos de la motilidad que correspondieran a la sospecha ECG y la conducta fue expectante. En los 15p restantes se detectó trastornos segmentarios de la motilidad; 4p fueron reintervenidos con nuevo PV sin CCG previa y en 11 p se realizó una CCG cuyos hallazgos se correspondieron con las zonas de alteraciones evidenciadas por el ETE, de éstos, en 9 se realizó ATC del PV, arterial o de la arteria nativa revascularizada y en los 2 restantes se realizó una nueva revascularización quirúrgica.
Se valoró la utilidad del ETE teniendo en cuenta si hubo o no un cambio de conducta posterior, presentando una utilidad en el 67% de los casos (98p); y sin cambiar la conducta terapeútica en el 33% de los casos (49p). La mortalidad de los primeros fue del 10 % (10/98) y de los segundos del 22% (11/49), con una p= 0.04. (gráfico 8)
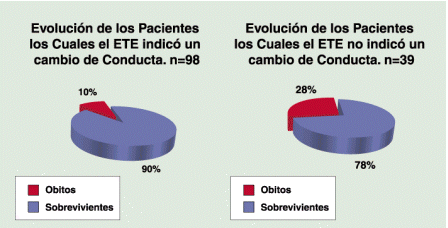
Gráfico 8:Mortalidad según si el ETE modificó o no la conducta terapeútica
Discusión
Durante el período operatorio y perioperatorio, se producen cambios hemodinámicos importantes, como alteraciones fisiológicas ligadas al estrés, que se acentúan en los pacientes coronarios incrementándose el riesgo de isquemia o infarto de miocardio, tanto intra como perioperatorio. La detección precoz de tales eventos y su reversión es esencial para la evolución clínica alejada de estos pacientes.
Por otro lado, se reconoce la baja sensibilidad del electrocardiograma en la detección de isquemia intraoperatoria, primero porque cuando las alteraciones del ST-T aparecen, la isquemia ya está bien establecida y, por otra parte, los cambios del ECG pueden ser secundarios a la cardioplejia, el frío y los frecuentes trastornos de la conducción post quirúrgicos.
Las modificaciones hemodinámicas, tanto de las presiones pulmonares como las sistémicas, son parámetros también influenciados por la isquemia, aunque siempre de aparición tardía, y es bien conocido que el tiempo de isquemia está en directa relación con la recuperación posterior y el riesgo de daño residual permanente.
El ECG y los parámetros hemodinámicos no son los indicadores más precoces de posible isquemia. La visualización directa de la motilidad ventricular global y regional a través del ETE es un método de detección de isquemia intraoperatoria precoz (fig 2-3). Existen ciertas dudas de que las alteraciones de la motilidad detectadas intraoperatoriamente, sean con seguridad producidas por verdadera isquemia miocárdica. La alta incidencia intraoperatoria de disfunción regional de la motilidad (21 a 30%), genera las dudas de los posibles falsos positivos diagnosticados por ETE. Lo cierto es que la detección de isquemia a traves de las alteraciones de la motilidad es de 3 a 4 veces superior que el ECG aun de múltiples derivaciones. Las publicaciones en la literatura mundial demuestran una estrecha relación entre la detección de isquemia intraoperatoria (precoz) y la evolución y sobrevida alejadas de los pacientes, lo que confiere un importante valor pronóstico al ETE. (18-19) (cuadro1).

Cuadro 1: Utilidad del ETE en presencia de alteraciones de la motilidad
La detección precoz de isquemia miocárdica puede ser monitorizada desde la inducción anestésica hasta la salida misma del quirófano: esto permite al cirujano, al señalarle la zona comprometida, reestablecer la circulación rápidamente, evitando el infarto perioperatorio.
Con el desarrollo de los equipos de última generación, dotados de Doppler tisular y color kinesis, podemos maximizar la precocidad para detectar isquemia, por medio de la evaluación de la función diastólica regional la que se altera antes que los parámetros sistólicos (11-12) detección que puede ejecutarse durante todo el clampeo aórtico, pudiendo evaluar su mejoría luego de la revascularización. (Fig 4-5)
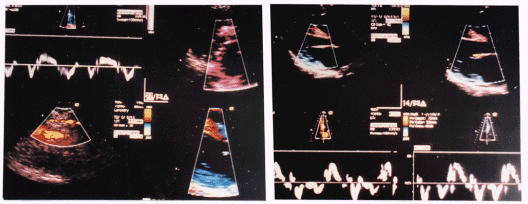
Fig 4 y 5: Evaluación de la función diastólica regional por Doppler tisular y función sistólica con color kinesis
La incorporación de los medios de contraste ecocardiográfico (13) y los equipos con recepción de armónicas (14) nos confieren la oportunidad de evaluar la perfusión en las distintas zonas miocárdicas antes de la cirugía. En pacientes con lesiones severas de múltiples vasos en los cuales existen dudas en cuanto a la distribución de la cardioplejia y la protección brindada por ésta, la perfusión con contraste identifica estas zonas que serían las primeras a reperfundir por el cirujano, además de ser un método que puede detectar indemnidad a nivel microcapilar, lo cual guarda estrecha relación con la recuperación posterior. (15-16-17)
En nuestro trabajo 49 p correspondían a aquellos que no podían ser retirados de circulación extracorpórea. De posible causa isquémica detectamos: 29p con alteración global de la motilidad y no fue interpretado como factible de corregir con mayor o nueva revascularización, por lo que se indicó inotrópicos solos o asociados a balón de contrapulsación aórtico, pero en 12p la alteración detectada fue de la motilidad regional, se les realizó a 9 de ellos un puente al territorio sugerido por el ETE y en otros 3p nuevo puente con apoyo del BCPAo. Basados en esta metodología, pudimos en forma más racional, tomar decisiones y evaluar su respuesta.
Del mismo grupo de p con imposibilidad para retirar de CEC, pudimos rescatar a 4p con disfunción protésica, y en otro se indicó reemplazo valvular mitral luego de realizar aneurismectomía lateral que involucraba el músculo papilar.
Algunos pacientes sometidos a reemplazo valvular aórtico por severa estenosis y marcada hipertrofia ventricular presentan dificultad para mantenerse fuera de CEC, en éstos la conducta inicial es la administración de inotrópicos; pero con la ayuda del ETE se puede identificar la causa de este problema, que no es más que una obstrucción dinámica medioventricular que se produce al desaparecer la barrera al vaciado que era la válvula aórtica (27). En nuestro grupo en 3p evidenciamos esta condición e indicamos volumen, suspender inotrópicos y en uno de ellos administrar ß-bloqueantes pudiéndolos retirar de quirófano. Del total de este sub grupo de 41 p, 40 pudieron ser retirados de CEC registrándose un solo óbito en quirófano.
Actualmente, es de generalizado conocimiento la necesidad del ETE para la cirugía de plásticas valvulares. La tendencia actual, es tratar, dentro de lo posible, de preservar la válvula nativa y es por este hecho que el ETE adquiere importante valor aún antes de llegar al quirófano, aportando datos acerca de la etiología, severidad y estado de la función ventricular y según ello planear la cirugía e inferir la factibilidad de realización de la misma (20).
El estudio transesofágico es el método de elección para evaluar la anatomía y función de la válvula mitral. El éxito de la plástica está directamente relacionado con la etiología de la enfermedad valvular, de tal modo que si es por degeneración mixomatosa, apriori tiene grandes posibilidades de reparación, siendo ésta mayor si la insuficiencia es de valva posterior, en menor grado si es anterior y considerablemente menor si es de ambas valvas. La posibilidad de una plástica se reduce si la etiología es reumática o isquémica (22).
Teniendo en cuenta tales datos, se puede indicar plástica o reemplazo, evitando intentar la reparación en una válvula que de antemano tiene pocas posibilidades de éxito. (23-24) Una vez decidida la reparación, el ETE puede efectuar el análisis anatómico valvular y del jet regurgitante en distintos planos y dividir las valvas posterior claramente en 3 zonas, anterior, medio y posterior, de ese modo según la localización y dirección del jet podemos indicar cuál valva y en qué sitio tiene que repararse, variando de esa manera la técnica y las posibilidades de éxito.(21-22) En nuestro trabajo incluimos 24p sometidos a plástica valvular, luego de la evaluación pre y post procedimiento, una vez retirados de CEC, en 5p se indicó reemplazo valvular al constatar el fracaso de la reparación. La evaluación de la regurgitación tricuspidea durante la cirugía valvular mitral es otro importante paso previo antes de dar por finalizado el acto quirúrgico, ya que aquellos pacientes con insuficiencia tricuspidea severa no solucionada con anuloplastia, muestran mayor mortalidad inmediata y alejada. El ETE es el patrón oro para evaluar el grado IT y la necesidad o no de realizar anuloplastia (25).
En muchas oportunidades la cirugía de la válvula aórtica está asociada a valvulopatía mitral secundaria difícil de mensurar en su severidad, conociendo previamente que luego del reemplazo aórtico ésta puede disminuir en su severidad, sin embargo, en 3p de nuestro grupo luego de la información aportada por el ETE se indicó reemplazo mitral. En otro paciente con IM isquémica, luego de la revascularización el ETE informó la desaparición casi total de la regurgitación, no siendo necesario el reemplazo.
En la exploración de la patología aórtica, ya sea aguda o crónica, el ETE ocupa un lugar de preponderancia, más aún cuando la patología base es un hematoma disecante, mostrando una sensibilidad y especificidad similar a la resonancia nuclear magnética, hoy considerada el patrón de oro (28-29). El ETE nos informa de la existencia del flap íntimo medial y su extención, nos permite distinguir entre verdadero y falso lumen, el comportamiento de los flujos, la puerta de entrada de la disección, la presencia de reentradas, el compromiso de la válvula aórtica, los vasos del cayado, la existencia de derrame pericárdico o pleural y el estado de la función ventricular. Toda esta información rápida y sin movilizar el paciente es fundamental para establecer el plan quirúrgico (30-31).
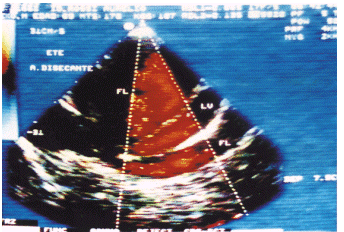
Durante el acto quirúrgico pudimos informar al cirujano del comportamiento del flap íntimo medial, y posterior a la reparación la existencia de flujo residual en el falso lumen, como la persistencia de comunicantes hiperfuncionantes. También fue útil para evaluar la válvula aórtica y la necesidad o no de resuspensión o colocación de tubo valvulado. El pronóstico alejado depende en gran parte de esta información, siendo conocida la mala evolución en aquellos pacientes en que persiste flujo pulsátil en el falso lumen o comunicantes hiperfuncionantes (32-33-34). Ocho pacientes de nuestro grupo fueron operados de disección aórtica con la guía transesofágica (Fig 6, 7 y 8).
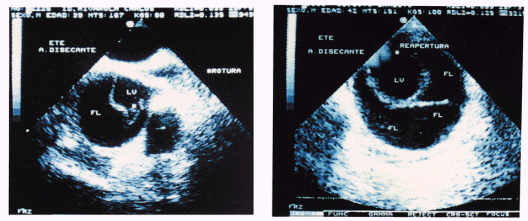
Fig 6: ETE que muestra una disección aórtica con una gran comunicación entre el lumen verdadero (LV) y falso (FL) (asterisco).
Fig 7: ETE de un paciente con hematoma disecante aórtico que muestra prácticamente la disección completa de la luz aórtica con el FL y LV y una comunicación entre ambos (asterisco)
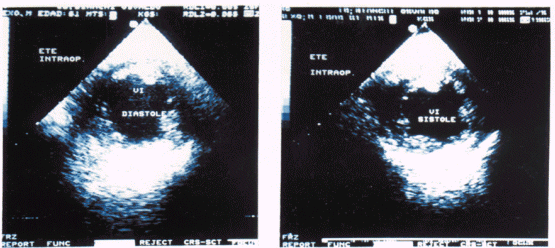
En la actualidad existen variadas propuestas para el tratamiento de la miocardiopatía hipertrófica obstructiva, que van desde el tratamiento médico farmacológico, marcapasos fisiológicos, alcoholización de las ramas septales de la coronaria izquierda y la cirugía de miotomía miectomía, intentando modificar la obstrucción sistólica. Durante la cirugía de ésta patología, el ETE es capaz de guiar al cirujano en relación a la magnitud de la resección y verificar de inmediato el éxito de la intervención (caída del gradiente), la posible detección de defectos septales iatrogénicos y la desaparición del movimiento anterior sistólico de la válvula mitral. Es conocido el mal pronóstico de los pacientes con persistencia de compromiso hemodinámico post miectomía. (35) En nuestro paciente, luego de la miectomía persistió con movimiento anterior sistólico e insuficiencia mitral severa, indicando el reemplazo de la válvula, y de esta manera solucionar el problema. (Fig 9 y 10)
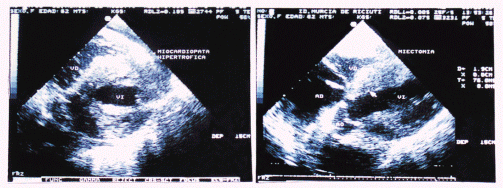
Fig 9 y 10: ETE intraoperatorio en un paciente con miocardiopatía hipertrófica septal obstructiva pre cirugía y luego de
liberar el tracto de salida del VI (flecha)
La detección de anomalías que pasaron sin diagnosticar o la presencia de shunt residuales post cirugía en las cardiopatías congénitas, es la principal indicación del ETE intraoperatorio (36). En dos pacientes detectamos shunt residual que fue corregido antes de la salida de CEC luego del cierre de sendas CIV post IAM.
La identificación de trombos intracavitarios, tumores u otras masas intracardíacas es uno de los campos explorados por la ecografía intraesofágica. Sobre este aspecto asistimos en colaboración a la cirugía de pacientes con mixomas atriales, y en el diagnóstico y resección de un trombo oclusivo total de la rama pulmonar derecha en un paciente joven con hipertensión pulmonar de reciente aparición (síndrome antifosfolípido), comprobando también en el acto quirúrgico la permeabilidad de la rama una vez extraído el mismo (37) (Fig 11 y 12).
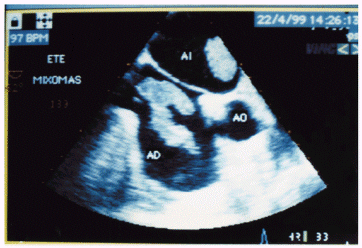
Fig 11: ETE intraoperatorio: Mixomas bilaterales
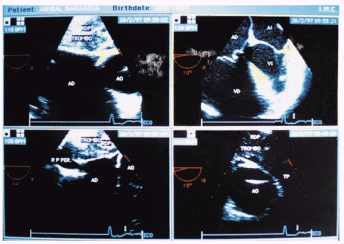
Fig 12: ETE intraoperatorio: Paciente con trombosis completa de la rama pulmonar derecha (superior e inferior izquierda).
Imagen de la rama pulmonar luego de extirpado el trombo (inferior derecha)
Los pacientes en la sala de recuperación que presentan un cuadro de descompensación aguda y grave configuran en muchos casos una encrucijada diagnóstica y terapéutica. Varias son las condiciones peculiares en esta situación: los pacientes están inmovilizados, la mayoría de las veces en asistencia respiratoria mecánica (ARM), con vendajes, tubos de drenajes, electrodos, dispositivos de asistencia circulatoria, etc. Por otro lado los parámetros hemodinámicos suelen no ser representativos de lo que realmente está pasando, dado que muchos factores pueden influir: la hiperinsuflación por la ARM, la presión positiva de fin de espiración, taquipnea del paciente, lo que convierte al ecocardiograma en un método de diagnóstico con información anátomo funcional que se puede realizar al pie de la cama. También es cierto que por las condiciones anteriormente enumeradas sólo tendremos una ventana acústica transtoráxica adecuada en un limitado número de casos (38). En este panorama el ETE es de una inapreciable ayuda, con facilidad para su introducción y muy escaso índice de complicaciones (39)
Si bien es reconocido el valor del ETE en situaciones como hipoxemia inexplicada, endocarditis bacteriana, diagnóstico de disección aórtica, inestabilidad hemodinámica y complicaciones mecánicas del IAM (40-41-42): durante el postoperatorio de cirugía cardíaca es solicitado en la mayoría de las oportunidades por: síndrome de bajo gasto cardíaco, hipoxia inexplicada y sospecha de disfunción miocárdica (cuadro 2). El impacto del estudio se traduce en un cambio de medidas terapeúticas que van desde un 30 a un 55% (42-43).
Cuadro 2: Utilidad del ETE para discriminar los mecanismos involucrados en el Síndrome de Bajo Volumen Minuto
En nuestros pacientes durante el post operatorio, el ETE fue requerido por dos motivos principales: bajo gasto cardíaco y cambios isquémicos (ECG). El síndrome de bajo volumen minuto se presenta en el post operatorio inmediato con una incidencia del 12%, independientemente de los adelantos técnicos quirúrgicos actuales (44). Es bien conocido la necesidad de un diagnóstico precoz de la causa que lo desencadena, ya que su falta de reconocimiento y el tratamiento tardío, conlleva una alta mortalidad. Los causados por alteraciones mecánicas de solución quirúrgica, tienen mejor pronóstico que aquellos causados por disfunción miocárdica: 17% vs 45% (45-46).
El taponamiento cardíaco es una de las causas frecuentes de síndrome de bajo volumen minuto durante el postoperatorio de cirugía cardíaca, con una incidencia del 0,1 al 3%(47), a pesar que la presencia de derrame pericárdico hemodinámicamente no significativo es superior, llegando al 80% en algunas publicaciones (48-49).
Nadie en la actualidad pone en dudas la utilidad de la ecografía transtoráxica en el diagnóstico de derrame y taponamiento, pero por las limitaciones ya mencionadas que presentan los pacientes en la sala de recuperación, el ETE juega un rol fundamental. En nuestro grupo, realizamos el estudio en 25 p con bajo gasto cardíaco de los cuales 12 se encontraban con parámetros hemodinámicos de taponamiento, confirmando la sospecha clínico-hemodinámica sólo en 6 (50%) solucionando el cuadro con la evacuación quirúrgica. En los 6 restantes descartó taponamiento evitando una reintervención. (Fig 13)
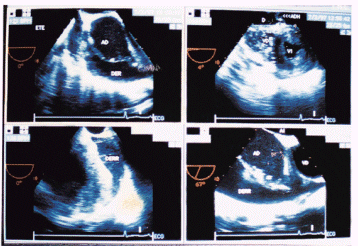
Fig 13: ETE post operatorio: Paciente con síndrome de bajo gasto cardíaco producido por taponamiento.
Notese la compresión diastólica del VD. (Cuadro superior izquierdo e inferior derecho)
La radiografía de tórax y el electrocardiograma son de poca sensibilidad y especificidad para el diagnóstico de taponamiento, el pulso paradojal se presenta en sólo el 50% de los casos (50-51) y los parámetros hemodinámicos son imprecisos a causa de la ARM o la presión positiva de fin de expiración, lo que torna imprescindible la confirmación ecocardiográfica del cuadro. Cabe destacar que los datos signados como diagnóstico de taponamiento como son el colapso de la AD, vena cava superior y ventrículo derecho, como las variaciones del flujo transmitral, son inconstantes y muchas veces no evaluables. La hipertensión pulmonar también enmascara o simula estos datos (52). Nuestros hallazgos coinciden con los publicados en que los datos hemodinámicos son concordantes con verdadero taponamiento sólo en el 50% de los casos; el derrame pericárdico loculado o coágulos intrapericárdicos pueden producir clínica de taponamiento con bajo débito sistémico que se soluciona con el drenaje y el ETE en la mayoría de la veces es quien sugiere el mismo (53-54-55) (Fig 14).
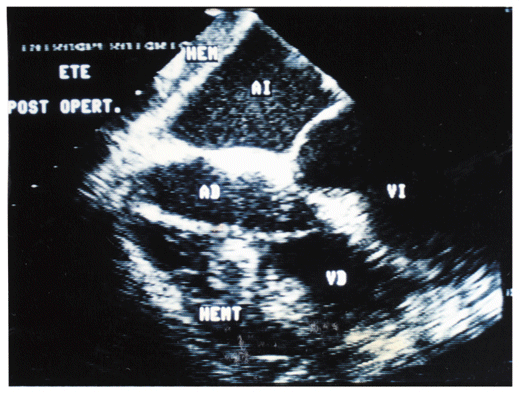
Fig 14: ETE post operatorio: Paciente con síndrome de bajo gasto cardíaco, con derrame loculado y hematoma compresivo
Otro grupo de pacientes en quienes fue requerido el ETE son aquellos con sospecha de isquemia aguda. La motilidad parietal y la función ventricular global se pueden ver comprometidas durante las primeras horas del post operatorio, lo que puede estar relacionado a cierto grado de atontamiento miocárdico que va recuperándose progresivamente (56). En nuestra experiencia efectuamos ETE en aquellos pacientes con trastornos electrocardiográficos sospechosos de isquemia, y dada la baja sensibilidad para la detección de la misma, el hallazgo de una hipocinecia global conduciría a pensar en un deterioro ventricular previo o bien al atontamiento antes mencionado disminuyendo así la sensibilidad del método. Pero en pacientes que desarrollan cambios isquémicos, la detección de alteraciones de la motilidad regional, que no estaban previos a la cirugía o grados mayores de alteración de los trastornos previos y en especial de las zonas revascularizadas, son datos fundamentales para decidir la conducta. También debemos reconocer que existen ciertas áreas que son difíciles de explorar por el ETE, como lo es el ápex del VI (57-58).
En nuestro grupo de 18 p, 3 no presentaron trastornos regionales de la motilidad y la conducta fue expectante a pesar que los ECG indicaban isquemia. En los 15 p restantes al detectarse trastornos segmentarios, todos ellos fueron reperfundidos, 4p por un nuevo puente venoso sin CCG previa, 9p con angioplastia del puente o de la arteria nativa, y 2p con una nueva revascularización quirúrgica posterior al cateterismo. Existe evidencia que la detección de trastornos segmentarios de la motilidad en la cirugía y post operatorio incrementa el riesgo de infarto perioperatorio, disfunción ventricular y muerte súbita.
Nuestro trabajo no fue diseñado estrictamente para determinar la utilidad del ETE intraoperatorio y en la sala de recuperación, ya que los pacientes reclutados en el mismo fueron producto de la solicitud del estudio cuando presentaban un problema; lo que explica nuestro alto porcentaje de utilidad medido en relación a los cambios de conducta sugeridos y adoptados.
García Fernández et al analizaron una población no seleccionada y consecutiva de pacientes sometidos a cirugía cardíaca con control transesofágico, reportando la utilidad del ETE basada en la modificación de la táctica quirúrgica y/o anestésica de un 1/3 de los casos, (59) llegando a la conclusión luego de analizar la relación costo-beneficio, que el ETE es el mejor método de monitoreo intraoperatorio en los pacientes cardiópatas.
En nuestro grupo, si analizamos la utilidad solamente en base al cambio de conducta generado, ésta fue del 67% (98p), mientras que en el resto de la muestra a pesar de proporcionar una valiosa información fisiopatológica no se pudo cambiar o mejorar la intervención terapéutica, (trastornos difusos de la motilidad manejados con soporte inotrópico y/o mecánico, reemplazo valvular, transplante cardíaco).
Mientras que en el primer grupo la mortalidad fue del 10% (10p), en el grupo de pacientes en los cuales no surgió un cambio de conducta luego del ETE, la mortalidad fue del 22% (11p), correspondiendo en su totalidad con el hallazgo de un deterioro severo de la función ventricular izquierda. Estos resultados son concordantes con los encontrados en la literatura coincidiendo con los grupos de mayor riesgo identificados en el estudio CONAREC III (60) para nuestro país. La diferencia de mortalidad, según las complicaciones con relación a nuestro trabajo, radica fundamentalmente porque en el estudio CONAREC se incluyeron centros sin disponibilidad del ETE de rutina, por lo que en un gran número se vieron privados de esta ayuda diagnóstica.
Conclusiones
Estos datos indican que el ETE intraoperatorio y perioperatorio constituye una herramienta valiosa para la toma de decisiones quirúrgicas y el manejo de las complicaciones post operatorias, mejorando el pronóstico de esta población de pacientes de alto riesgo.
* Este trabajo recibió el premio de la Sociedad de Cardiología de Córdoba, Argentina, año 2000 *
Referencias
1- Likoff m, Reicheck N, Sutton M et al: Epicardial mapping of segmental myocardial function: an echocardiography method applicable in man. Circ 1982, 66:1050. [ Links ]
2- Matsamuto M. Et al: Aplication of transesophageal echocardiography to continuos monitoring of left ventricular perfomance. Am.J.Cardiol 1980, 46:95 [ Links ]
3- Schulter M. Et al: Transesophageal cross-sectional echocardiography with a phased array transducer system: Technique and initial clinical results. Br.Heart J. 1982, 48:67 [ Links ]
4- Souquet J., Hanrath P., Zitelli L, et al: transesophageal phased array for imaging the heart. IEEE Trans Biomed Eng. 1982, 29:707. [ Links ]
5-Seward J. Et al : Biplanar transesophageal echocardiography: Anatomic correlations, image orientations, and clinical applications. Mayo Clinic Proc 1990, 65:1193. [ Links ]
6- Freeman W., O`hara P., Abel M. Et al: Intraoperative applications of transesophageal echocardiography. En Freeman W., Seward J. Kandheria B: Transesophageal echocardiography. Boston. Little Brow and Company 1994 cap 16 pag 503. [ Links ]
7-Kandheria B, Oh J.: Transesophageal echocardiography: state of the art and future directions. Am. J. Cardiol. 1992, 69:614. [ Links ]
8- Beampre P. Et al: Intraoperative detection of changes on left ventricular segmental viale motion by transesophageal two dimentional echocardiography. Am Heart J. 1984, 10:1021 [ Links ]
9- Branwald E., Kloner R.: The stunned myocardium: Prolonged post ischemic ventricular dysfunctions. Circ 1982, 66:1146. [ Links ]
10-Rodriguez L., Garcia M., Ares M., Griffin B., Nokatomi S., Thomas J.: Assesment of mitral anular dynamics during diastole by Doppler Tissue imaging: Comparison match mitral Doppler inflow in subjets without heart disease and in patients with left ventricular hypertrophy. Am Heart J. 1996 131:982. [ Links ]
11-Mc Dicken W., Sutherland G., Moran C., Gordon L.: Color Doppler velocity of the myocardium. Ultrasound in medicine and biology 1992, 18:651 [ Links ]
12-De Jong N., Ten Cate F.: New ultrasound contrast agents and technological innovations ultrasonics. 1996, 34:587. [ Links ]
13-Burns P., Pomers J., Simpsom D. : Harmonic Imagin: Principles and preliminary results. Clin Radiol. 1996, 51 (suppl) 50-55. [ Links ]
14-Villanueva F., Kaul S.: Assesment of myocardial perfusion in coronary artery disease using myocardial contrast echocardiography. Coron. Art. Dis. 1995, 6:18. [ Links ]
15-Villanueva F., Camarano G., Ismail S., Goodman N., Skilman J., Kaul S.: Coronary reserve abnormalities in the infarcted myocardium: Assesment of myocardial viability inmediately versus late after reflow by contrast echocardiography. Circulation 1996, 94:748. [ Links ]
16-Hirata N., Shimazaki Y., Nakano S., Sakao K., Sakaki S., Matsuda H: Evaluation of regional myocardial infarction after revascularization by mean of intraoperative myocardial contrast echocardiography. J. Thoracic. Cardiovascular Surg. 1994, 108:1119. [ Links ]
17-Rin et al: Effect of coronary by pass surgery and valve replacement on the left ventricular function: Assesment by intraoperative two dimensional echocardiography. Am.Heart J. 1985, 109:281. [ Links ]
18-Topol E., et al: Inmediate improvement of dysfunctional myocardial segments after coronary revascularization: detection by intraoperative transesophageal echocardiography. J.Am.Coll.Cardiol. 1984 4(6):1123. [ Links ]
19-Stemart W., Currie P., Salcedo E., et al: Evaluation of mitral leaflet motion by echocardiography and jet direction by Doppler color flow mapping to determine the mechanism of mitral regurgitation. J.Am.Coll.Cardiol. 1992, 20:1353. [ Links ]
20-Stemart W., Currie P., Salcedo E., et al: Intraoperative Doppler color flow mapping for decission making in valve repair for mitral regurgitation. Technique and results in 100 patients. Circ 1990, 81:556. [ Links ]
21-Carpentier A., Relland J., De Loche A., et al : Conservative managment of the prolapsed mitral valve. Ann. Thorac.Surg 1978, 26:294. [ Links ]
22-Equaras M., et al: Intraoperative contrast two dimensional echocardiography: Evaluation of the presence and severity of aortic and mitral regurgitation during cardiac operations. J. Thorac. Cardiovasc. Surg 1985, 89:573. [ Links ]
23-Takamoto S., et al: Intraoperative color flow mapping by real time dimensional Doppler echocardiography for evaluation of valvular and congenital heart disease and vascular disease. J. Thorac. Cardiovasc. Surg. 1985, 90:802. [ Links ]
24- King R., et al: Surgery for tricuspid regurgitation late after mitral valve replacement. Circ 70 (suppl 1) 1984 1:193. [ Links ]
25-Syracuse D., et al: Intraoperative intracardiac echocardiography during left ventriculotomy and myectomy for IHSS (abstract) Circ. (Suppl 3) 1977, 56:27. [ Links ]
26-Freeman W., Schoff F., Oh J.m et al: Evaluation of hipertrophic cardiomiopathy by intraoperative transesophageal echocardiography. J. Am.Coll.Cardiol (suppl A) 1993, 21:321. [ Links ]
27-Laissy J. Blanc F., Soyes P., et al: Thoracic aortic disection. Diagnosis with transesophageal echocardiography versus M.R. imagin. Radiology 1995, 194:331. [ Links ]
28-Sommer T., Fehske W., Holzknecht N., et al: Aortic disection: a comparative study of diagnosis with spiral C.T., multiplanar transesophageal echocardiography and M.R.imagin. Radiology 1996, 199:347. [ Links ]
29-Adachi H., Omoto R., Kjo S., et al: Emergency surgical intervention of acute aortic dissection with the rapid diagnosis by transesophageal echocardiography. Circ 1991, (suppl III) 84:14. [ Links ]
30-Simon P., Owen A., Havel M., et al: Transesophageal echocardiography in the emergency managment of patients with aortic dissection. J.Cardiovasc.Surg. 1992, 103:1113. [ Links ]
31-Mohr-Kahaly S., Erbel R., Rennollet H., et al: Ambulatory follow up of aortic dissection by transesophageal two dimensional and color coded Doppler ehocardiography. Circ 1989, 80:24. [ Links ]
32-Balld R., Nanda N., Gatewood R., et al: Usefulness of transesophageal echocardiography in assesment of aortic dissection. Circ. 1991, 84:1903. [ Links ]
33-Hanrich A., Miller D., Scott W., et al: Acute and chronic dissections, determinants of long term outcome for operative survivors. Circ 1985, (suppl II) 72:22. [ Links ]
34-Daniel W., Schoeder E., Nellessen V., Hausmam D.: Diagnosis of intra and extra cardiac masses by echocardiography. Comparison between the transthoracic and transesophageal approach. Circ 1987 (suppl IV) 76:38. [ Links ]
35-Romeo F., Pellicia F., Cristofani R., Reale A.: Hipertrophic cardiomyopathy: Is a left ventricular outflow tract gradient a major prognostic determinant? Eur.Heart.J 1990, 11:233 [ Links ]
36-Ungerleider R., Sheik H., Philips J., Pearce F.: Routine use intraoperative epicardial echocardiography and Doopler color flow imagind to guide and evaluate repair of congenital heart lesions: A prospective study. J.Thorac.Cardiovasc.Surg. 1990; 100:297-309. [ Links ]
37-Daniel W., Schoeder E., Nellessen V.: Diagnosis of intra and extracardiac masses by echocardiography. Comparison between the transthoracic and transesophageal approach. Circ 1987 (supp IV) 76, CV 38 [ Links ]
38-Parquer M., Perrillo J.: Echocardiography and nuclar cardiac imaging in the critical care unit. JAMA 1985, 254:2935. [ Links ]
39-Pearson A., Castillo R., Labovitz A.: Safety and utility of transesophageal echocardiography in critically ill patients. Am.Heart J. 1994; 127:1363. [ Links ]
40-Perez de Prado A., García Fernández M., Moreno M., Torrecillas E., San Roman D., Delcan J.: Utilidad de la ecocardiografía transesofágica en las unidades de cuidados cardíacos intensivos generales. Rev.Esp.Cardiol. 1994; 47:735. [ Links ]
41-Oh J., Sinak L., Freeman W., Seward J., Khandheria B.: Transesophageal echocardiography in patients with shock syndrome. Circ. 1991; 84 (Supl II):127. [ Links ]
42-Shama M., Novara A., Van de Putte P., Diebold B., Safar M., Assart M.: Diagnostic and therapeutic implication of transesophageal echocardiography in medical ICU patients with unexplained shock, hipoxemia, or suspected endocarditis. Intensive Care Med. 1996; 22:916. [ Links ]
43-Apridi I., Quiones M., Zoglibi W.: Transesophageal echocardiography in critically ill patients: Feasibility, safety, and impact on management. Am.Heart J.; 127:1363. [ Links ]
44-Gray R., Metloff J.: Medical management of cardiac surgical patients. Ed William & Wilbuir. Baltimore. Maryland USA 1990. [ Links ]
45-Davila Roman V., Waggoner A., Hopkins W., et al: Right ventricular disfunction in low output syndrome after cardiac operation: Assesment by transesophageal echocardiography. Ann.Thorac.Surg. 1995; 60:108. [ Links ]
46-Reichtert C., Visser C., Koolen J., Wezel H., et al: Prognostic value of biventricular function in hipotensive patients after cardiac surgery assesed by transesophageal echocardiography.J.CardiothoracicVasc.Anesth.1992; 6:429. [ Links ]
47-Stevenson L., Child J., Laks H., Kern L.: Incidence and significance of early pericardial effusion after cardiac surgery. Am.J.Cardiol. 1984;54:848. [ Links ]
48-Pepi M., Barbier P., Dona E., Arena V., Bert M., et al: Pericardial effusion after cardiac surgery: Incidence, site, size, and hemodinamic consequences. Br Heart J. 1994; 72:327. [ Links ]
49-Ikaheimo M.,Huikuri H., Tarkka M., et al: Pericardial effusion after cardiac surgery: incidence, relation to type of surgery, antitrombotic therapy, and early coronary by pass graft patency. Am.Heart J. 1988; 116:97. [ Links ]
50-Chuttami K., Tiscker M., Paudian N.: Diagnosis of cardiac tamponade after cardiac surgery: relative value of clinical, echocardiography, and hemodinamics signs. Am.Heart J. 1994; 127:913. [ Links ]
51-Russo A., O`Connor W., Waxman H.: Atipical presentations and echocardiographyc findings in patients with cardiac taponade occuring early and late after cardiac surgery. Chest 1993; 104:71. [ Links ]
52-Frey M., Beiko B., Polevky H., Herman H.: Recognition of cardiac taponade in the presence of severe pulmonary hipertension. Ann.Inter.Med. 1989; 111:615. [ Links ]
53-Simpson I., Smith E., Parker D.: Pericardial hemorhagea causing rigth atrial compression after cardiac surgery: role of transesophageal echocardiography. Br.Heart J. 1991; 65:355. [ Links ]
54-Kochar G., Jacobs L., Kother M.: Right atrial compression in postoperative cardiac patients: detection by transesophageal echocardiography. J.Am.Coll.Cardiol. 1990; 16:511. [ Links ]
55-Beppu S., Tanaka N., Kumon K.: Pericardial clot after open heart surgery: Its specific localization on haemodinamic. Eur.Heart J. 1993; 14:230. [ Links ]
56-Brisblatt W., Stein K., Wolfe C., et al: Acute myocardial dysfunction and recovery: a common occurence after coronary by pass surgery. J.Am.Coll.Cardiol. 1990; 15:1261. [ Links ]
57-Shively B., Watters T., Schiller N., Benefield D., et al: The intraoperative detection of myocardial infarction by transesophageal echocardiography (abstract) J.Am.Coll.Cardiol. 1986; 7:2ª.
58-Chung F., Sayone C.: Transesophageal echocardiography may fail to diagnose perioperative myocardial infarction. Can.J.Anesth. 1991; 38:98. [ Links ]
59-García Fernández M., Tizon G., Moreno M., et al: Rentabilidad de la ecocardiografía transesofáfica de rutina en la cirugía cardíaca en enfermos no seleccionados. Analisis de 130 casos consecutivos. Rev. Arg. Cardiol. 1995; 63: (6) 543. [ Links ]
60-Ciruzzi M., Henquin R., Aranda G., Bozovich G., investigadores del CONAREC III.: Evolución de los pacientes sometidos a cirugía coronaria. Estudio multicéntrico. Rev.Arg.Cardiol. 1996; 64:(1) 91. [ Links ]
*Servicio de técnicas no invasivas,
Instituto Modelo de Cardiología – F.U.C.C.A.D.I.M. –
Sagrada Familia 359 - UP21. 5003. Córdoba.
Córdoba, Argentina.
e-mail: fliatibaldi@arnet.com.ar