Introducción
El arsénico está presente en el agua como un oxianión y tiene dos estados de oxidación mayoritarios en la naturaleza: el arsenito o As (III) y el arseniato o As (V). Estas dos especies están en la fracción soluble del arsénico, por lo que la filtración de las muestras con un filtro de membrana de 0,45 µm permite separar el arsénico particulado del arsénico disuelto en el agua.
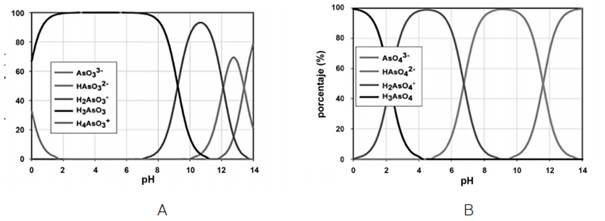
Generalmente, en ambientes oxidantes prevalece el As(V), el cual hidroliza cómo ácido arsénico, (H3AsO4). Sus correspondientes productos de disociación son: H2AsO4 -, HAsO4 2- y AsO4 3-. En ambientes bajo condiciones reductoras prevalece el As (III) que hidroliza como ácido arsenioso, (H3AsO3). Sus correspondientes productos de disociación son: H2AsO3 -, HAsO3 2- y AsO3 3- (1), (2). En el ámbito de pH de las aguas naturales, el arsénico +5 se encuentra cargado negativamente mientras que el arsénico +3 es una especie neutra, por eso no se retiene en cromatografía de intercambio aniónico (4), (5). La figura 1 presenta los diagramas de solubilidad para las especies As (III) y As(V) según el pH del medio.
Sin embargo, algunas aguas subterráneas pueden tener solamente As (III), otras sólo As (V), o bien, presentar una combinación de ambos estados de oxidación (4) ya que esto también depende del ambiente geoquímico de las aguas (5).
La cuantificación de arsenito y arseniato en el agua es fundamental para interpretar la toxicidad y movilidad del arsénico en el ambiente, ya que el arsenito es más tóxico que el arseniato (6), pues se bioacumula de forma distinta al arsénico pentavalente (7). Desde el punto de vista de remediación, aporta valiosa información sobre la tecnología de remoción más apropiada porque es más complejo la remoción del arsenito (3).
En el año 2014, el AyA instaló seis plantas de remoción de arsénico empleando la tecnología de adsorción - filtración en los pozos en: Bebedero de Cañas, Falconiana, Montenegro y Quintas Don Miguel en Bagaces, Cristo Rey y Santa Cecilia de El Amparo en Los Chiles, (véase la figura 2).
En estos lugares, las concentraciones de arsénico superaban los 10 µg/L, siendo este, el valor máximo admisible (VMA) según el Reglamento para la Calidad del Agua Potable de Costa Rica (Decreto N° 38924-S) (8) y la OMS (8), (9). La presencia del arsénico es de origen natural y se le relaciona con fallas geológicas en las zonas e hidrotermalismo (10).
El objetivo de este trabajo es ejecutar y validar un método analítico para separar y cuantificar As (III) y As (V) en las aguas de los pozos de las plantas de remoción de arsénico mediante la cromatografía de intercambio aniónico y la espectrometría de masas con plasma de acoplamiento inductivo.
Metodología
El desarrollo de la investigación estuvo dividido en 5 fases:
Optimización de ICP-MS según las especificaciones de Agilent Technologies para ICP-MS modelo 7700 (11).
Optimización de las columnas cromatográficas de intercambio aniónico, empleando resina Dowex 1X-8 de 50 a 100 mallas en forma de acetato, a partir de una simulación del procedimiento de separación con diferentes mezclas de As (III) y As (V) en agua sintética. Se trabajó en dos ámbitos de concentración: En ámbito alto los niveles de concentración fueron de 50,0 µg/L y 25,0 µg/L y en ámbito bajo a 5,0 µg/L y en ausencia de As (III) y As (V) realizando siete repeticiones de cada mezcla para evaluar recuperaciones.
Validación de la metodología.
Muestreo y separación de las formas arsenicales en el campo.
Cuantificación en el laboratorio mediante ICP-MS y tratamiento de resultados.
Para la preparación de la resina y la separación de las distintas especies arsenicales se siguió el procedimiento descrito en (12).
El procedimiento de separación de las especies se resume en la figura 3: a) se abre la llave de chorro del pozo, b) se toma muestra de agua del pozo, c) se recolecta en la botella A parte de la muestra y se preserva con 0,5 mL de ácido nítrico grado traza metal al 70 % (arsénico total), d) se acopla el filtro de 0,45 µm a la jeringa previamente enjuagada con la muestra, e) cuidadosamente se introduce la jeringa en el beaker que contiene la muestra para filtrarla, f) se recolecta la muestra filtrada en la botella B (arsénico soluble) y se preserva con 1,3 mL de ácido sulfúrico traza metal al 5 %, g) la botella B se agita vigorosamente para mezclar con el ácido adicionado, h) se pasa 40 mL de la muestra de la botella B a través de la columna para lavar la resina, i) se recolecta aproximadamente 20 mL de la muestra tratada en la resina en la botella C (arsenito) y se preserva con 1 gota de ácido nítrico grado traza metal al 70 %, j) se transportan las muestras en hielo.
Las concentraciones de las tres muestras se cuantificaron en ICP-MS y por diferencia, se obtuvieron las concentraciones de arsénico particulado (retenido en el filtro) y arseniato (retenido en la columna). Cabe resaltar que en cada gira se hizo duplicado el procedimiento por pozo y que los resultados de cada muestreo corresponden al promedio.
Resultados y discusión
Validación
En el cuadro 1 se presentan las figuras de mérito obtenidas en la validación de la metodología, esto se realizó según lo establecido en la EURACHEM (13).
Cuadro 1 Figuras de mérito para la determinación de arsénico total por ICP-MS.
| Límite de detección | 0,1 µg/L |
| Límite de cuantificación | 0,2 µg/L |
| Repetibilidad | 0,2 % |
| Repetibilidad intermedia | 0,3 % |
| Veracidad, % de recuperación | 97 % - 104 % |
Concentración de arsénico total en los seis pozos
La concentración de arsénico total de cinco pozos: Bebedero, Montenegro y Agua Caliente, Falconiana, Santa Cecilia y Cristo Rey oscilaron en el ámbito de (13,1 ± 0,1) μg/L y (23,7 ± 0,1) μg/L en todo el periodo de muestreo.
El pozo de Quintas Don Miguel tuvo la mayor concentración de arsénico total. De setiembre a diciembre de 2014 la concentración estuvo entre (16,0 ± 0,1) µg/L y (20,0 ± 0,1) µg/L. Sin embargo, en enero del 2015 la concentración aumentó un 47,2 % pues se cuantificó (43,6 ± 0,1) µg/L de arsénico total. Para octubre del 2015, la concentración en dicho pozo disminuyó a (36,6 ± 0,1) µg/L y en noviembre del mismo año, la concentración descendió nuevamente hasta (19,2 ± 0,1) µg/L.
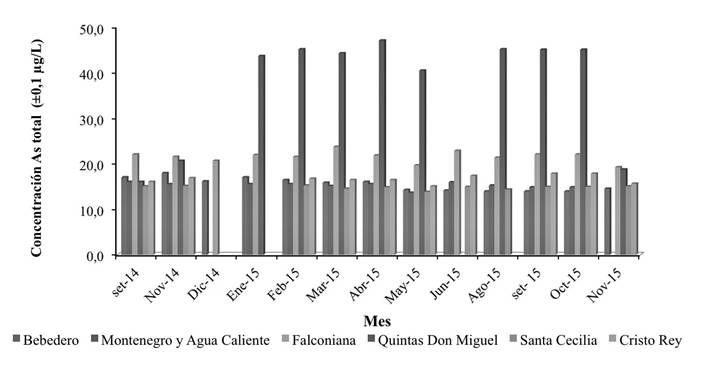
Figura 4 Concentración de arsénico total en los pozos de las seis plantas de remoción de arsénico de setiembre del 2014 a noviembre del 2015.
Arsénico particulado y soluble en los pozos
En el cuadro 2, se muestra que las concentraciones de arsénico particulado no superaron el 9,0 % de las concentraciones de arsénico total, por lo que muy poco arsénico está de forma particulada, o bien, retenido en el filtro de 0,45 µm.
Cuadro 2 Porcentaje de arsénico total presente como arsénico particulado en los pozos de las plantas de remoción de arsénico en el año 2015.
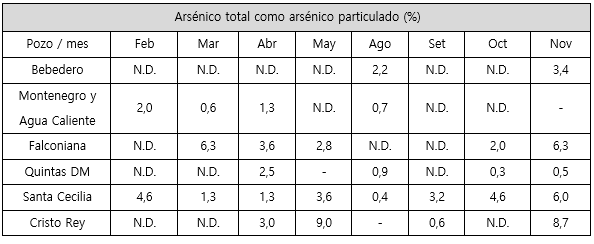
N.D.: No detectable
Por lo tanto, el arsénico en los seis pozos se encuentra mayoritariamente en su forma disuelta, como se muestra en el cuadro 3. El porcentaje de arsénico soluble representó entre 91 % el 100 % del arsénico total cuantificado.
Cuadro 3 Porcentaje de arsénico total presente como arsénico soluble en los pozos de las plantas de remoción de arsénico en el año 2015.
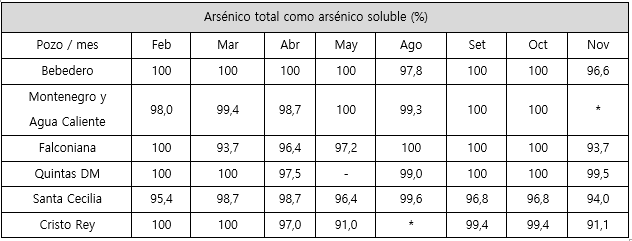
*No se tomó muestra pues no había bombeo al momento de la visita.
Concentración de arsenito y arseniato
En los cuatro muestreos que comprenden la poca seca, solamente en marzo del 2015 se detectó arsenito en el pozo de Quintas Don Miguel. La concentración de arsenito fue no detectable en los pozos de las cuatro plantas ubicadas en la provincia de Guanacaste (Bebedero, Montenegro y Agua Caliente, Falconiana y Quintas Don Miguel), por lo que todo el arsénico soluble de estos pozos se encontraba como As(V).
En Santa Cecilia de El Amparo fue posible la cuantificación de arsenito y en febrero de 2015 se obtuvo la concentración más alta de As (III) de la época seca: (10,0 µg/L). En marzo y abril del 2015, la concentración de arsenito se mantuvo constante: (8,3 ± 0,1 µg/L) y (8,4 ± 0,1 µg/L), respectivamente, y en mayo disminuyó a (5,8 ± 0,1) µg/L. Por su parte, en el pozo de Cristo Rey, la concentración de arsenito corresponde al límite de detección en el mes de febrero de 2015, mientras que, de marzo a mayo del mismo año, solo fue posible su detección, pero no su cuantificación.
Para los muestreos de la época de lluvia, fue posible la detección y cuantificación de arsenito en los pozos de Bebedero, Montenegro y Agua Caliente y Falconiana. En Montenegro y Agua Caliente sólo pudo detectarse As(III) de agosto a noviembre de 2015, mientras que en Falconiana se presentó una situación similar, a excepción del mes de octubre, donde la concentración de arsenito fue igual al límite de cuantificación (0,2 µg/L).
En Bebedero y Quintas Don Miguel se obtuvieron concentraciones no detectables, detectables y de hasta (0,4 ± 0,1) µg/L. En el caso específico de Santa Cecilia se continuó cuantificando arsenito en toda la época: de (6,9 ± 0,1 µg/L) a (8,7 ± 0,1) µg/L y en Cristo Rey la concentración de arsenito estuvo entre el límite de detección y (0,3 ± 0,1) µg/L.
Como se muestra en los cuadros 4 y 5, en todos los pozos prevalece el arseniato sobre el arsenito a excepción de Santa Cecilia de El Amparo. En los ocho muestreos, la concentración de arsenito y arseniato fluctúo mes a mes en esa zona, ya que en los primeros tres muestreos hay prevalencia del arseniato sobre el arsenito (superior al 57,5 %). En el mes de mayo se reduce la concentración de arsenito por lo que el arseniato se encuentra como estado de oxidación mayoritario (60,9 %). Entre agosto y noviembre de 2015, la concentración de arsenito incrementó nuevamente y osciló entre 48,9 % y el 57,6 % del arsénico soluble de dicho pozo.
Cuadro 4 Porcentaje de arsénico soluble presente como As (III) en el agua de los pozos de las plantas de remoción de arsénico en el año 2015.
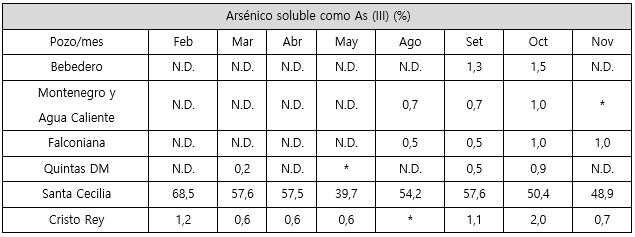
N.D.: No detectable *No se tomó muestra por no haber bombeo en el momento del muestreo
Cuadro 5 Porcentaje de arsénico soluble presente como As (V) en el agua de los pozos de las plantas de remoción de arsénico.
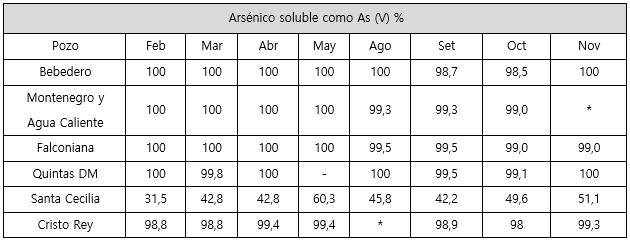
*No se tomó muestra por no haber bombeo en el momento del muestreo.
Con el fin de asociar los resultados en cuanto a la prevalencia de As (III) o As (V) en los pozos, se procedió a efectuar otras determinaciones para explicar y complementar los resultados obtenidos de las concentraciones de arsenito y arseniato.
Determinación de pH
Santa Cecilia y Cristo Rey de Los Chiles presentaron los pH más alcalinos de los seis pozos y para el caso de los pozos de Guanacaste, el pH fue bastante similar entre ellos, estos comportamientos no variaron en todo el periodo de muestreo. No se encontró relación directa entre el aumento o disminución de la concentración del arsenito con el aumento o disminución del pH y así relacionar la presencia o ausencia de As (III) o As(V) con valores de pH más alcalinos o más ácidos.
Cuantificación de manganeso
El pozo de Santa Cecilia presenta altas concentraciones de manganeso donde se ha cuantificado desde (385,0 ± 1,0) μg/L hasta (474,9 ± 1,0) μg/L. A su vez, es el único pozo donde fue posible cuantificar arsenito y arseniato en relación de concentraciones muy similar.
No se encontró relación directa entre la concentración de manganeso y la concentración de arsenito. En la primera gira efectuada en dicha comunidad se obtuvo (10,0 ± 1,0) µg/L de arsenito y (474,9 ± 1,0) µg/L de manganeso, siendo las concentraciones de arsenito y de manganeso más altas de los ocho muestreos. Sin embargo, en concentraciones de manganeso de (414,9 ± 1,0) µg/L y hasta (448,8 ± 1,0) µg/L, la concentración de arsenito fluctúa entre (5,8 ± 1,0) µg/L hasta (8,7 ± 1,0) µg/L.
Concentración de oxígeno disuelto
Se efectuaron las determinaciones de oxígeno mediante el método de Winkler, donde se fijó el oxígeno disuelto del agua en el campo, para posteriormente cuantificarlo en el laboratorio mediante una titulación. Los resultados obtenidos de oxígeno disuelto son los siguientes.
Cuadro 6 Concentración de oxígeno disuelto y temperatura en el agua de los pozos de las plantas de remoción de arsénico para la época seca y lluviosa.
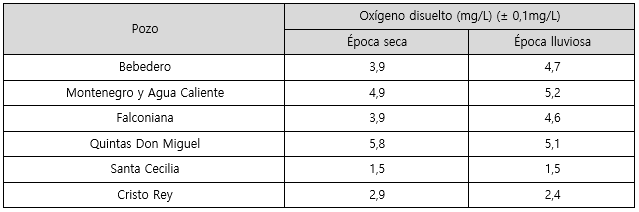
Incertidumbre: ±0,1 mg/L. LD: 0,2 mg/L, LC: 0,5 mg/L.
Los pozos de Guanacaste presentaron mayor concentración de oxígeno disuelto en el agua, siendo Quintas Don Miguel el pozo con las concentraciones más altas en las dos épocas. Por su parte, el pozo de menor concentración en todo el muestreo fue Santa Cecilia (1,5±0,1) mg/L, coincidiendo con el hecho de ser el único en el que se cuantifica más arsenito en el agua. Si hay menos oxígeno disuelto, hay mayor probabilidad de encontrar arsénico en estado de oxidación tres.
Concentración de sulfatos y nitratos en los pozos
Los sulfatos y nitratos compiten con el arseniato por los sitios de intercambio de la resina (14). Este método de separación con cromatografía de intercambio aniónico es aplicable en aguas cuya concentración de sulfatos y nitratos sea inferior a 120 mg/L y 200 mg/L, respectivamente. Las concentraciones de sulfatos no superaron los (11,8 ± 0,8) mg/L, mientras que los nitratos fueron inferiores a (22,9 ± 0,5) mg/L.
Conclusiones
Las resinas de intercambio aniónico son una opción económica, pueden emplearse varias veces antes de que la resina se sature y poseen la ventaja de separar el arsénico trivalente del pentavalente de manera “in situ”, asegurando que el equilibrio de estas especies no se modifique en el traslado al laboratorio para posteriormente separar y cuantificar.
El arsénico se encuentra mayoritariamente como arsénico soluble en los seis pozos. La mayor concentración de arsénico particulado se cuantificó en el pozo de Cristo Rey en el mes de mayo de 2015 (8,7 ± 0,1) µg/L y en noviembre del mismo año (9,0 ± 0,1) µg/L.
En febrero de 2015, en Santa Cecilia de El Amparo se cuantificó la mayor concentración de As(III) de todos los pozos, donde el 68,5 % del arsénico soluble estuvo como As(III), sin embargo, en los siguientes muestreos se obtuvieron concentraciones de arsenito y arseniato en proporciones muy similares, variando de mes a mes la prevalencia de un estado de oxidación sobre el otro.
En Bebedero, Montenegro y Agua Caliente, Falconiana, Quintas Don Miguel y Cristo Rey se detectó arsenito en algunos muestreos y cuando fue posible cuantificarlo, se encontró entre el límite de cuantificación y (0,4 ± 0,1 µg/L).
El pozo con menor concentración de oxígeno disuelto es precisamente donde hubo una combinación de arsenito y arseniato. Aunque la literatura indica que el As (III) predomina en condiciones reductoras y el As(V) prevalece en condiciones oxidantes, no siempre esto se presenta, siendo una consecuencia el ambiente geoquímico de suelos y minerales, así como de las condiciones hidrogeológicas específicas del acuífero, entre otros.
Recomendación
En las seis plantas, el sistema de cloración se encuentra antes de la etapa de remoción, con el objetivo de asegurar que todo el arsénico se encuentre oxidado antes de la remoción, ya que el medio adsorbente a base de dióxido de titanio retiene de forma más efectiva el As (V) que el As (III).
De acuerdo con la experiencia de los ingenieros de AyA involucrados con estas plantas, el medio adsorbente (dióxido de titanio) pierde vida útil de forma más rápida cuando pasa agua clorada por los filtros presurizados. Si ya se conocen los niveles de As (III) y As(V) en los pozos, se podría optimizar la dosis de cloro necesaria para oxidar el arsenito presente y a su vez, para desinfección del agua. Esto se traduciría en reducción de costos para AyA pues se podría incrementar la vida útil del medio adsorbente y se reduciría el consumo de gas cloro.