Introducción
Uno de los componentes más importantes de los conectores es el recubrimiento con una capa de oro, como lo indica Ponce [1], el principal componente de la demanda mundial de oro lo constituye el uso para fabricación de bienes (joyería, electrónica, odontología, entre otros). En este caso, la demanda de oro para el área de la electrónica es muy grande, y en este segmento de mercado se utiliza el oro por sus características físicas y químicas. Además cerca del 6.6% del oro extraído se utiliza en electrónica.
El oro es llamado metal noble, ya que según Kirkemo, Newman y Ashley [2] este no se oxida bajo condiciones ordinarias. Esto también lo respalda Ponce [1] el oro es el más “no reactivo” de todos los metales, es benigno en todos los ambientes naturales e industriales. El oro nunca reacciona con oxígeno o sea difícilmente se oxidará o se empañará.
Además de sus características químicas, como la poca reactividad, el oro es muy empleado en los conectores por su buena conductividad eléctrica. Lo anterior lo confirma López y Peña [3], el oro es una aplicación no muy usada en la electrónica aunque en casos de exigencia y calidad es lo más adecuado por sus excelentes propiedades conductivas, estos recubrimientos otorgan buenas características en las puntas ya que las hace duraderas y aseguran una buena adherencia.
Los recubrimientos de oro en los conectores se realizan por medio de la electrodeposición, la cual según Imaz [4] es una tecnología muy extendida en muchos campos y sectores industriales para la obtención de recubrimientos metálicos.
Sobre el proceso de electrodeposición, Díaz del Castillo [5] menciona que el éxito de la operación está en función del control de los fenómenos involucrados, por lo que es necesario mencionar los principios a los que se sujetan éstos, ya que cualquier variación en el proceso se verá reflejada de manera significativa en el resultado obtenido.
Por la necesidad de controlar las diferentes variables que se presentan en la electrodeposición, se muestra la importancia de desarrollar métodos analíticos eficientes para el análisis de oro, tal y como lo indican Sánchez, Hernández y López [6], un grupo reciente y atractivo de métodos para la determinación de oro hacen uso de la formación y extracción en disolventes orgánicos de compuestos de asociación iónica entre complejos aniónicos de Au (III) con cationes orgánicos voluminosos y determinación de la especie extraída con una técnica analítica adecuada según las características del par iónico formado.
Debido a la gran importancia que tiene el oro para la industria eléctrica y su proceso de producción, se pretende determinar cuál técnica analítica es la más eficiente para su cuantificación, y así poder tener un mejor control sobre la concentración del mismo en las celdas donde se realiza la electrodeposición.
En la empresa interesada en realizar este proyecto, se utilizan diferentes metales de recubrimiento para los conectores, entre ellos estaño, níquel y oro. Dichos metales se encuentran en diferentes soluciones y luego se adhieren por electrodeposición a las piezas metálicas. Para que el producto final sea de buena calidad, la concentración del metal en el tanque, específicamente oro, debe ser la indicada. Para ello se realizan con frecuencia análisis que determinan la cantidad de oro presente en la solución.
De una semana a otra se han encontrado variaciones de hasta el 6% en la cantidad de oro presente en la misma muestra. Diferentes controles realizados muestran que la concentración no presenta tendencias de incrementar ni de disminuir, por lo tanto se descarta la opción de algún efecto de la matriz que cambie la concentración con el tiempo. Bajo estas condiciones, la variación que se tiene entre los resultados de una semana a otra utilizando la misma muestra, representan cerca de 42 onzas de oro en el peor de los casos. Esto podría traer consecuencias en la preparación de las soluciones que se utilizarán para la electrodeposición del metal de interés, lo cual a su vez afecta directamente el proceso de producción y la calidad del producto final.
Debido a la gran variación mencionada anteriormente y los impactos negativos que esta representa en el proceso de producción de la empresa, se requiere implementar un método analítico que sea capaz de disminuir dicha variación entre los resultados de una misma muestra medida en semanas diferentes.
Fundamento
El oro es el elemento con el símbolo Au y número atómico de 79, según Ponce [1] es fácilmente soluble en agua regia o en otras mezclas que desprenden cloro, también lo disuelve el yodo en estado naciente y los cianuros. No lo atacan el ácido clorhídrico ni tampoco el ácido nítrico solo, no lo atacan los álcalis fundidos y el ácido sulfúrico lo ataca por encima de los 300 °C.
El oro se adhiere a los conectores mediante un proceso de electrodeposición, el cual López [7] indica que es un proceso electro-químico donde se realiza un recubrimiento (normalmente metálico) a una pieza con un sistema de ánodo y cátodo, sumergiendo dicha pieza en un baño químico y aplicando cargas eléctricas debidamente calculadas para cubrir o depositar una capa protectora o decorativa a la pieza.
Con respecto al proceso de electrodeposición, el baño químico mencionado contiene el oro que se desea depositar sobre los conectores. Dicho baño debe ser capaz de disolver el oro para luego ser depositado, debido a ello, Lillo, Aros y Carlesi [8] mencionan que las reacciones que describen el proceso para la disolución de oro en una solución cianurada son:
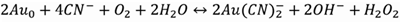
(1)
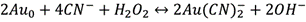
(2)
Las reacciones anteriores muestran el proceso por el cual se mantiene el oro disuelto, además constituye la matriz de interés, junto con otros componentes como cobalto.
Para la cuantificación de oro en soluciones cianuradas, Fouad, Elrakaiby y Hashim [9] indican que muchas técnicas son viables para la determinación de oro usando tanto los métodos clásicos como ensayos al fuego, o métodos instrumentales como espectrometría de absorción atómica de llama, las cuales se acoplan con extracciones con solventes para dar resultados confiables.
Sobre la técnica de Absorción Atómica, Rocha [10] menciona que tiene como fundamento la absorción de radiación de una longitud de onda determinada. Esta radiación es absorbida selectivamente por átomos que tengan niveles energéticos cuya diferencia en energía corresponda en valor a la energía de los fotones incidentes. La cantidad de fotones absorbidos, está determinada por la ley de Beer, que relaciona ésta pérdida de poder radiante, con la concentración de la especie absorbente.
El oro tiene dos bandas de absorción, una a 242.8nm [11] y otra a una longitud de onda de 267.6 nm [12]. La que mejores resultados brinda es la línea de absorción de 242.8nm, por lo tanto es la seleccionada para realizar la cuantificación de oro.
Una de las ventajas de la Espectrofotometría de Absorción Atómica, según Skoog, James y Crouch [13] es que los métodos de absorción son muy específicos debido a que las líneas de absorción atómicas son notablemente estrechas (0.002 a 0.005 nm) y porque las energías de transición electrónicas son únicas para cada elemento.
Otra técnica analítica para la cuantificación de oro es la Espectroscopía de Fluorescencia de Rayos X, en la cual según Skoog et al [13], la absorción de rayos X produce iones excitados electrónicamente que vuelven a su estado fundamental mediante transiciones en las que intervienen electrones de los niveles de mayor energía, después de un breve periodo, el ion vuelve a su estado fundamental mediante una serie de transiciones electrónicas que se caracterizan por la emisión de radiación X. Esta emisión de rayos X es característica para cada elemento, lo cual permite la cuantificación de oro con un mínimo de interferencias.
Un aspecto importante de la Espectroscopia de Fluorescencia de Rayos X es que se trata de una técnica no destructiva, por lo que la hace ampliamente utilizada en la determinación de oro [14].
Para una buena cuantificación de oro, sin importar la técnica analítica utilizada, es indispensable la validación del método. Según Rodríguez et al [11] la validación de técnicas analíticas proporciona un alto grado de confianza y seguridad en el método analítico y en la calidad de los resultados que se obtienen, lo que hace de este proceso una necesidad en todo laboratorio, para garantizar la fiabilidad de los resultados obtenidos.
El proceso de validación de un método analítico es definido como la aportación de evidencia objetiva de que un elemento satisface un requisito especificado [15]. En este caso, la validación se utilizará para asegurarse que el método analítico cumpla con los requerimientos establecidos.
Para llevar a cabo la validación de un método analítico, se hace el estudio de diferentes aspectos como selectividad, especificidad, linealidad, veracidad, precisión y robustez, para concluir con el cálculo de la incertidumbre respectiva.
Metodología
El trabajo analítico se llevó a cabo en el laboratorio físico químico de una industria de dispositivos electrónicos en Costa Rica, durante el período comprendido entre agosto y diciembre del 2015.
Para la ejecución del estudio, primero se establecieron las condiciones óptimas para la realización de los análisis, tanto para Absorción Atómica (AA), como para la Espectroscopia de Fluorescencia de Rayos X. En el Cuadro 1 se muestran las condiciones del equipo de AA para la cuantificación de oro.
El equipo de absorción atómica utilizado es marca Agilent Technologies 240FS AA, con un automuestreador Agilent Technologies SPS 3. El estándar utilizado es una solución de 1000 µg/ml de oro marca J.T.Baker. En cuanto a la Espectroscopia de Fluorescencia de Rayos X, el equipo utilizado fue un Fischerscope X Ray XDV-µ.
Para determinar si ambas técnicas son capaces de cuantificar oro en soluciones cianuradas, se realizará y medirá una curva de calibración para cada técnica. Tomando en cuenta las referencias bibliográficas, así como las capacidades de los equipos, la curva de calibración para Absorción Atómica comprende puntos de 1, 3, 6, 9 y 12 mg/L. Mientras que la de Espectroscopia de Fluorescencia de Rayos X se elaboró a concentraciones de 1, 5, 10, 15 y 20 g/L.
Cuadro 1 Parámetros y condiciones del equipo de Absorción Atómica
| Parámetro | [76]Valor |
|---|---|
| Llama | [79]Aire:acetileno |
| Flujo de Aire | [82]13.50 L/min |
| Flujo de Acetileno | [85]2.0 L/min |
| Longitud de Onda | [88]242.8 nm |
| Slit | [91]1 nm |
| Lámpara | [94]Cátodo Hueco de Oro |
| Corriente de la lámpara | [97]4.0 mA |
| Corrección de Fondo | [100]On |
Luego se midieron diferentes muestras por ambas técnicas para determinar si son capaces de cuantificar oro en soluciones cianuradas. Una vez obtenidos los resultados de cada técnica, se compararon entre sí para lograr determinar cuál de las técnicas presenta más eficiencia a la hora de cuantificar oro en soluciones cianuradas, tomando en cuenta la veracidad y la precisión de cada técnica analítica. Para ello se realizó un análisis de Repetibilidad y Reproducibilidad utilizando el programa estadístico Minitab 17.
Para la ejecución del análisis de repetibilidad y reproducibilidad se midieron dos réplicas de 10 muestras diferentes, por tres analistas diferentes; con ello se tendrán datos sobre la precisión de cada técnica. Con respecto a la evaluación de la veracidad de cada técnica para su comparación, se efectuó la medición de un material de referencia certificado; con estos resultados se realizó una prueba de significancia t de Student, para determinar si existe diferencia significativa entre el valor obtenido por cada técnica y la concentración teórica.
Tomando en cuenta aspectos como veracidad y precisión de cada técnica, se comprobó estadísticamente cuál de ellas presenta mejores resultados y por último se realizó la validación del método seleccionado según la Guía de Validación de Métodos ECA-MC-PO01-G01 del Ente Costarricense de Acreditación versión 03.
Resultados y Discusión
Determinación de la factibilidad de las metodologías analíticas de Absorción Atómica y
Espectroscopia de Rayos X para la cuantificación de oro en soluciones cianuradas
Como parte inicial de la investigación se pretendía determinar si los métodos analíticos de Absorción Atómica y Espectroscopia de Fluorescencia de Rayos X son capaces de determinar oro en la matriz de interés, sin tomar en cuenta parámetros estadísticos de los mismos, ya que estos serán evaluados posteriormente. Primero se realizó el estudio de la técnica de Absorción Atómica para determinar su factibilidad para determinar oro. El método analítico de Absorción Atómica, y sus variantes, ha sido ampliamente estudiado para la determinación de oro. Como lo indica Patiño [12], la absorción atómica es una técnica valiosa para la determinación de pequeñas cantidades de oro.
Con el método analítico de Absorción Atómica se pueden determinar cantidades de hasta unos pocos miligramos de oro por litro, tal y como lo menciona Fouad et al [9] la Ley de Beer fue obedecida desde 0.01µg/ml hasta una concentración máxima de 10 µg/ml. Como vemos, existe gran cantidad de referencias bibliográficas sobre Absorción Atómica para la cuantificación de oro.
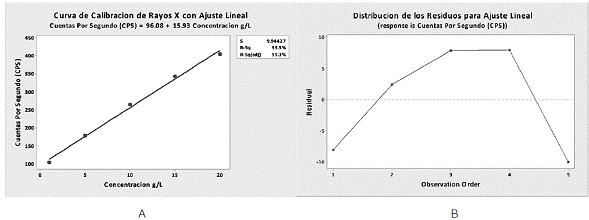
De manera experimental se probó lo mencionado anteriormente, esto para verificar que se cumpla la Ley de Beer en concentraciones que van de 1 mg/L hasta los 12 mg/L, ya que es un rango de trabajo muy similar al que se recomienda en otras referencias bibliográficas. Se obtuvieron los resultados que se muestran en la Figura 1A, con respecto al ajuste lineal de los patrones ensayados.
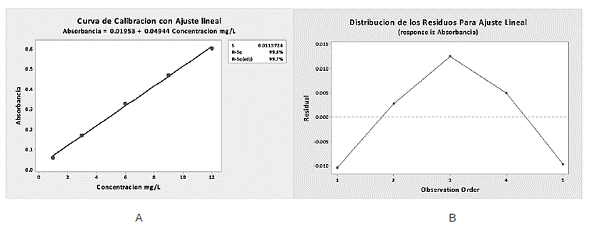
Figura 1 Curva de calibración (A) y distribución de los residuos (B) para ajuste lineal por Absorción Atómica
Tomando en cuenta el valor obtenido del coeficiente de determinación (0.998), se podría pensar que la curva de calibración es óptima para una cuantificación de oro. Sobre este tema Mongay [16] menciona que será la unidad cuando el modelo de regresión explique toda la variación de los datos, en cuyo caso el ajuste de los datos experimentales al modelo será perfecto. El coeficiente de determinación obtenido se encuentra muy cerca de la unidad, por lo que parece un buen modelo de ajuste.
Pero además de dicho parámetro, se deben considerar otros aspectos relacionados con el modelo de regresión para asegurarse que este sea el adecuado, como es el caso del análisis de los residuos. Para que el modelo de regresión sea confiable, los residuos deben distribuirse aleatoriamente alrededor de cero, cualquier tendencia es indicativa que el modelo no presenta un buen ajuste. Esto lo confirma Mongay [16], indicando que se asume que la media de los residuales es cero y que los errores son independientes, sin tendencias predominantes. Considerando lo anterior, se realizó un análisis de los residuos de la regresión con ajuste lineal y se obtuvieron los resultados ilustrados en la Figura 1B. Como se aprecia, los residuos no tienen una distribución aleatoria alrededor de cero, tienen una tendencia a aumentar y luego a disminuir. Esto es indicativo que el ajuste seleccionado, en este caso lineal, no es el adecuado.
Una vez que se determinó que el ajuste lineal no es el que mejor resultados ofrece, se probó un ajuste polinómico para la regresión, esto utilizando el mismo rango de concentraciones (1-12 mg/L), obteniendo lo ilustrado en la Figura 2A.
En este caso, el coeficiente de determinación tuvo una leve mejoría ya que paso de 0.998 a un 1.00, pero como se mencionó anteriormente, no solo se debe considerar este valor para asegurar un buen modelo de regresión. Por esta razón se realizó un nuevo análisis de los residuos para el ajuste polinómico, obteniendo los resultados evidenciados en la Figura 2B.
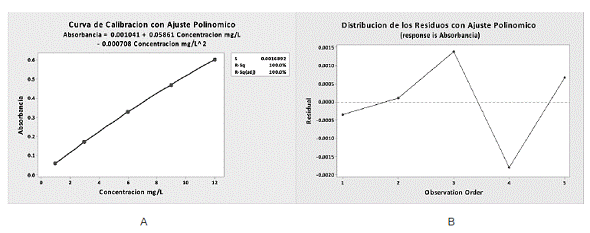
Figura 2 Curva de calibración (A) y distribución de los residuos (B) para ajuste polinómico por Absorción Atómica
Para la regresión con un ajuste polinómico los residuos presentan una distribución aleatoria alrededor de cero, además no tienen ninguna tendencia, por lo que se puede afirmar que la regresión con ajuste polinómico es el mejor modelo para la cuantificación de oro por Absorción Atómica.
Una vez establecidas las condiciones del equipo, así como el mejor modelo de regresión, se realizó la medición de algunas muestras obteniendo resultados satisfactorios, por lo tanto se puede concluir que el método analítico de Absorción Atómica puede utilizarse para la determinación de oro. Es importante aclarar que esta conclusión es basada únicamente en el principio fisicoquímico de la técnica, aun no se está tomando en cuenta parámetros de desempeño como veracidad y precisión.
Para el método analítico de Espectroscopia de Fluorescencia de Rayos X, el procedimiento que se siguió fue similar. La diferencia es que el equipo utilizado si tenía capacidad de medir soluciones con una concentración más alta, hasta de g/L de oro. Tomando en cuenta esto y la concentración de analito esperada, se preparó una curva de calibración en el rango de 1 g/L hasta 20 g/L, obteniendo los resultados que se muestran en la Figura 3A con respecto al ajuste lineal.
Como se aprecia, se obtuvo un coeficiente de determinación cercano a uno (0.995), lo cual es lo más deseable. Al igual que para el método de Absorción Atómica, se realizó un estudio de los residuos, ya que anteriormente se expuso la importancia de los mismos. Los resultados del análisis de los residuos se presentan en la Figura 3B.
El resultado del análisis de los residuos de la curva de calibración por Rayos X con ajuste lineal es muy similar al obtenido para un ajuste lineal en Absorción Atómica, primero se presenta una tendencia a aumentar y luego a disminuir.
Anteriormente se mencionó las implicaciones de la distribución de los residuos obtenida, por lo tanto se corrigió de la misma manera, probando un ajuste polinómico para la regresión y se obtuvo lo ilustrado en la Figura 4A.
De la misma forma, se obtuvo una mejoría en el coeficiente de determinación, ya que paso de 0.995 con un ajuste lineal a un 1.00 con un ajuste polinómico. En este caso también se realizó el estudio de los residuos y se obtuvo lo ilustrado en la Figura 4B.
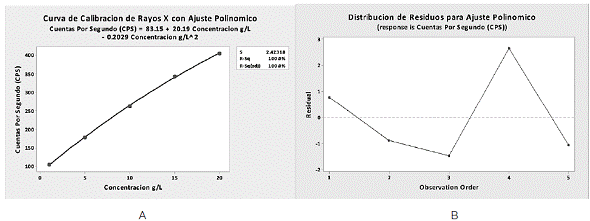
Figura 4 Curva de calibración (A) y distribución de los residuos (B) para ajuste polinómico por Rayos X
Como se aprecia la distribución de los residuos es aleatoria alrededor de cero, además no presenta ninguna tendencia. Tomando en cuenta el coeficiente de determinación, así como la distribución de los residuos, se evidencia que el mejor ajuste para la regresión es el polinómico, al igual que se demostró en Absorción Atómica.
Es importante destacar que, en el método analítico de Rayos X, una de las variables más importantes es el tiempo de medición, ya que puede afectar los resultados arrojados por el equipo. Brouwer [17] indica que un ajuste deficiente de los parámetros instrumentales puede conducir a obtener resultados pobres. En la medición de la curva de calibración, el fabricante del equipo utilizado recomienda un tiempo de 100 segundos, por lo tanto se siguió dicha recomendación y se midió al tiempo mencionado. Pero en el caso de la medición de muestras, el tiempo puede variar, dependiendo del equipo utilizado. Esto implica que no se encuentren muchas referencias sobre un tiempo de medición recomendado.
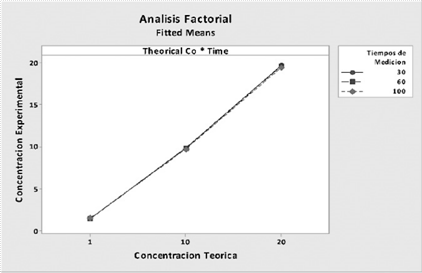
Para lograr establecer el mejor tiempo de medición para las muestras se llevó a cabo un análisis factorial, donde la variable experimental fue la concentración obtenida en el equipo de Rayos X y los factores fueron tres niveles de concentraciones de la curva de calibración, 1 g/L, 10 g/L y 20 g/L, y tres tiempos de medición, 30 segundos, 60 segundos y 100 segundos. Con ello se pretende identificar el efecto del tiempo de medición en los diferentes niveles de concentración de la curva de calibración seleccionada. Luego de las mediciones de las diferentes concentraciones a tiempos distintos de medición, se obtuvo lo ilustrado en la Figura 5.
En el análisis factorial realizado se aprecia el valor obtenido para cada concentración teórica analizada a diferentes tiempos de medición. Este análisis muestra que los valores experimentales son muy similares entre sí a cada tiempo de medición, por lo tanto no existe un efecto significativo del tiempo de medición sobre el resultado de la medición en el equipo de Rayos X utilizado.
Una vez que se determinó que no existe un efecto significativo del tiempo de medición sobre la concentración experimental, se estableció 60 segundos para la medición de las muestras. Se seleccionó dicho tiempo de medición debido a que es suficiente para irradiar la muestra y obtener una buena señal, además es un período corto para agilizar el análisis de oro.
Sobre el tiempo de medición en Espectroscopia de Fluorescencia de Rayos X, De la Fuente et al [14] menciona que con una tensión de 50 kV en la fuente, el tiempo de contaje para la obtención del espectro es de 50 segundos. Lo anterior es muy semejante al tiempo de medición seleccionado.
Cuando se estableció el tiempo de medición para las muestras, se procedió con la medición de algunas de ellas obteniendo resultados satisfactorios, por lo que se comprobó que la técnica analítica de Espectroscopia de Fluorescencia de Rayos X es funcional para la cuantificación de oro. Una vez más se debe aclarar que aún no se está considerando parámetros de desempeño como veracidad y precisión.
Tomando en cuenta todos los resultados expuestos anteriormente, se puede concluir que ambos métodos analíticos, Absorción Atómica y Espectroscopia de Fluorescencia de Rayos X, son capaces de medir la cantidad de oro en soluciones satisfactoriamente.
Comparación entre las técnicas analíticas de Absorción Atómica y Espectroscopía de Fluorescencia de Rayos X para determinar cuál es la más indicada para la cuantificación de oro en soluciones cianuradas
Gracias a los resultados obtenidos que demuestran la eficacia de los métodos analíticos en estudio para cuantificar oro, se puede tener ambas posibilidades para la determinación del analito de interés. Sin embargo, se debe poner un mayor énfasis sobre uno de ellos para su implementación.
A continuación se realiza un análisis de varios aspectos de ambos métodos analíticos, como precisión y exactitud, esto con el fin de determinar cuál es la mejor opción para una cuantificación de oro más confiable.
Para llegar a la conclusión de cual método analítico se seleccionará para su implementación se analizó primero un parámetro comparando ambos métodos, y luego el otro parámetro de igual manera con las dos técnicas. El primer aspecto para la escogencia del método es la precisión.
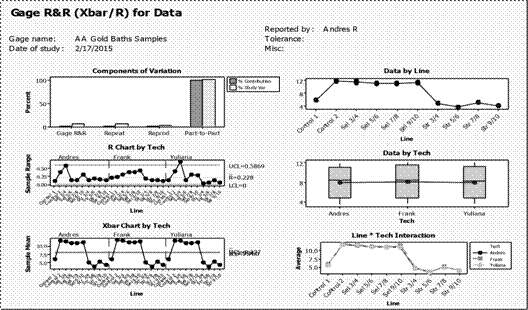
Previamente se había realizado un estudio de repetibilidad y reproducibilidad para el método analítico de Absorción Atómica, se obtuvo que la repetibilidad representa un 5.27% de la variación total del Sistema de medición. Además a la reproducibilidad le corresponde un 2.46%. La representación gráfica del estudio de repetibilidad y reproducibilidad para Absorción Atómica se muestra a continuación en la Figura 6.
La figura anterior arroja una gran cantidad de información sobre el sistema de medición, en este caso el método analítico Absorción Atómica. Entre la información valiosa que se muestra es que la mayor variación entre los datos medidos la representa las diferentes muestras utilizadas, lo cual es lo más deseable en un método analítico. Esto se debe a que lo anterior refleja dos cosas, primero que la repetibilidad y reproducibilidad del método son buenas, además de que el método es capaz de diferenciar entre una muestra y otra, aunque tengan valores muy similares.
Otra información relevante que se muestra en la Figura 6 es que las muestras tienen un comportamiento muy parecido independientemente del analista que realice la medición. Lo anterior quiere decir que el método analítico de Absorción Atómica presenta una buena reproducibilidad, ya que se mantiene constante aunque se cambie de analista.
Finalmente, la figura 6 también indica que la variación entre los datos de cada analista es muy similar, por lo tanto se confirma que la repetibilidad del método de Absorción Atómica es muy buena y constante.
Con respecto al otro método analítico analizado de Espectroscopia de Fluorescencia de Rayos X, también se realizó un estudio de repetibilidad y reproducibilidad del sistema de medición. Esto con el fin de tener las mismas condiciones para ambos métodos y que así la comparación sea lo más veraz posible.
El estudio de repetibilidad y reproducibilidad indica que la repetibilidad aporta un 3.94% de la variación, mientras que la reproducibilidad representa un 4.18% de la misma, esto para la Espectroscopia de Fluorescencia de Rayos X.
De igual manera, se presenta una representación gráfica del estudio de repetibilidad y reproducibilidad para el método analítico de Rayos X, según se ilustra en la Figura 7.
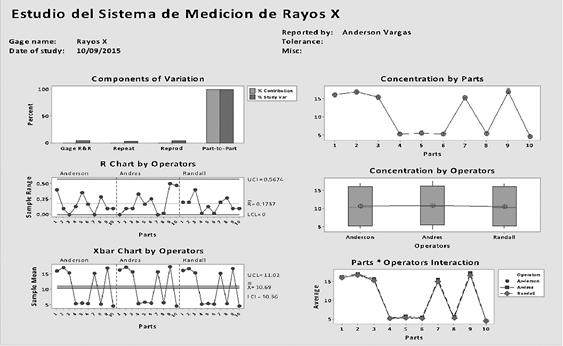
Figura 7 Estudio de Repetibilidad y Reproducibilidad para Espectroscopia de Fluorescencia de Rayos X
En la Figura 7 se puede observar situaciones similares a las mencionadas anteriormente para Absorción Atómica. Por ejemplo que la mayor variación en los datos se debe a las muestras, los resultados son independientes del analista que realice la medición y que la desviación de cada analista es muy similar a la desviación de los demás.
Tomando en cuenta lo expuesto anteriormente, además de los porcentajes que aportan la repetibilidad y la reproducibilidad a la variación total de cada método analítico, 5.27% y
2.47% respectivamente para Absorción Atómica y 3.94% y 4.18% respectivamente para Espectroscopia de Fluorescencia de Rayos X, no se aprecia una diferencia significativa, en términos de precisión, entre ambos métodos analíticos.
El otro parámetro seleccionado para la escogencia del método analítico más adecuado fue la exactitud. Se inició con la medición con el método analítico de Espectroscopia de Fluorescencia de Rayos X de una muestra control, misma que se encontraba caracterizada mediante el otro método analítico, Absorción Atómica.
Con la medición de una muestra control se pretendía demostrar si existe una diferencia significativa entre la medición de una misma muestra por ambos métodos. El resultado promedio para Absorción Atómica, método por el cual se caracterizó la muestra, fue de 4.29 g/L, mientras que el resultado promedio de la medición de la misma muestra por Espectroscopia de Fluorescencia de Rayos X fue de 5.42 g/L.
Una vez obtenidos los datos, se aprecia a simple vista que difieren en cerca de 1.13 g/L, lo cual es una cantidad bastante elevada. Para confirmar que existe una diferencia estadísticamente significativa entre ambos promedios, se realizó una comparación de dos medias con muestras relacionadas. Con relación a dicha prueba, Mongay [16] menciona que se acude al test de Student para contrastar la hipótesis nula de que las muestras proceden de la misma población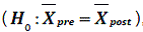 , o lo que es lo mismo que la diferencia
, o lo que es lo mismo que la diferencia 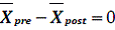 , hipótesis que será rechazada cuando Sign.<α.
, hipótesis que será rechazada cuando Sign.<α.
En la referencia anterior, los términos “pre” y “post” el autor los explica como una muestra a la cual se mide su característica de interés, luego se le hace un tratamiento para volver a medir su característica, pero siempre tratándose de la misma muestra aunque en condiciones diferentes de la misma. Una vez aclarado lo anterior, se debe comprender que la muestra control utilizada para la comparación entre ambos métodos analíticos fue la misma, pero se varió las condiciones de medición, en este caso el método analítico.
El resultado de la comparación entre dos medias con muestras relacionadas mostró un valor de p = 0.000 < 0.05 = α, por lo tanto se rechaza la hipótesis nula, la cual establecía que no había diferencia entre las dos medias. Esto quiere decir que las mediciones realizadas por medio del método analítico de Absorción Atómicas son diferentes a las realizadas con la Espectroscopia de Rayos X.
Una vez que se estableció que si existe diferencia entre las mediciones en ambos métodos, se debe determinar cuál de ellos arroja el resultado más cercano al valor real, o sea el método más exacto. Con ello se puede generar un criterio sobre cual método es el óptimo para su validación y posterior implementación.
Para lograr decidir el mejor método analítico, en cuanto a exactitud, se analizó una solución con concentración conocida de 1 g/L de oro por ambos métodos. La Espectroscopia de Fluorescencia de Rayos X obtuvo un valor promedio de 1.79 g/L, mientras que la Absorción Atómica reporto un valor de 1.03 g/L.
De igual manera, se realizó una prueba de hipótesis de t de Student, solo que en este caso para una sola muestra. Sobre dicha prueba, Mongay [16] menciona que se trata de comparar si existe alguna diferencia significativa entre una media muestra y un valor teórico de prueba. El criterio de aceptación sigue siendo el mismo mencionado previamente.
Los resultados para la Espectroscopia de Fluorescencia de Rayos X obtuvieron un valor de p = 0.000, por lo tanto se rechaza la hipótesis nula, la cual plantea que la media experimental es igual a 1 g/L. Para el caso de Absorción Atómica se presentó un valor de p = 0.129, ya que este valor es mayor que α = 0.05, indica que no existe diferencia entre la media experimental y el valor teórico de 1 g/L.
Con este resultado, es más factible llegar a una conclusión verdadera sobre cual método presenta una mejor exactitud, ya que las pruebas estadísticas realizadas demuestran que la técnica de Absorción Atómica presenta una exactitud superior a la obtenida por la Espectroscopia de Fluorescencia de Rayos X, en este caso específico de cuantificación de oro bajo las condiciones implementadas.
Gracias al estudio de varios parámetros de desempeño como precisión y exactitud, se puede tener criterio válido para seleccionar un método analítico para implementación. Tomando en cuenta los resultados de los estudios se concluye que el mejor método analítico para su validación y posterior implementación es la Absorción Atómica. Además se presentaron suficientes evidencias estadísticas para justificar la selección del método analítico.
Proceso de validación del método analítico de Absorción Atómica para cuantificación de oro en soluciones cianuradas
En la parte final de esta investigación se realizó la validación correspondiente al método analítico de Absorción Atómica. Para ello, el proceso de validación se realizó por un único analista, en un mismo laboratorio y se utilizó un único un equipo de Absorción Atómica.
El objetivo del proceso de validación es la caracterización del método analítico de Absorción Atómica y así determinar la confiabilidad de los resultados que arroje el mismo. Uno de los objetivos más importantes que debe cumplir el método, es tener una precisión menor al 4%, así como una recuperación de 100 ± 4%, ya que estas fueron las principales metas de la empresa interesada en la validación del método de Absorción Atómica.
El alcance de la validación incluye parámetros como especificidad, selectividad, linealidad, precisión, veracidad, ámbito de trabajo, robustez y finaliza con el cálculo de la incertidumbre expandida del método. Se excluyen los límites de detección y cuantificación debido a que ya se cuenta con una concentración esperada de analito presente en las muestras, las cuales son cercanas a 4 mg/L y 6 mg/L. Por lo tanto el método no deberá medir concentraciones muy pequeñas, esto permitió omitir la determinación de los límites de cuantificación y detección.
Los primeros parámetros evaluados fueron la selectividad y la especificidad, esto para determinar el efecto que tiene la matriz sobre la cuantificación de oro. En el caso de la especificidad se obtuvieron muy buenos resultados, tanto para estándares, como para blancos enriquecidos.
Es necesario recalcar el hecho que se demostró en apartados anteriores con respecto al modelo de regresión, ya que en el caso de Absorción Atómica el mejor ajuste corresponde a uno polinómico, no a un ajuste lineal como se presenta en la mayoría de referencias. Por lo tanto todas las mediciones que se realizaron por dicho método analítico, se llevaron a cabo utilizando este modelo de ajuste para la regresión.
Según la regresión de blancos enriquecidos a los mismos niveles de concentración que los utilizados para los estándares, comparando los interceptos obtenidos 0.000695 en el caso de la regresión con estándares y 0.000491 para los blancos enriquecidos, se aprecia que ambos son muy cercanos a cero, aunque no iguales al mismo. Según el Ministerio de Salud de Costa Rica [18] los efectos de la interacción entre la matriz y el analito, se encuentran ausentes si los intercepto del placebo enriquecido y los estándares son estadísticamente iguales a cero.
Como se indicó, los interceptos obtenidos no son iguales a cero, pero si son muy cercanos a ese valor. Esto indica que si hay efecto de la matriz en la cuantificación de oro, aunque el mismo es muy reducido. Lo anterior se confirma con la determinación de la selectividad del método. Uno de los componentes de la matriz es el cobalto, el cual como lo menciona Catalá [19] absorbe a una longitud de onda de 240.7 nm, muy cercana a la longitud de onda a la que absorbe el analito de interés, ya que el oro según Rodríguez et al [11], absorbe a 242.8 nm.
Debido a que la diferencia entre ambas longitudes de onda es únicamente de 2 nm, se realizó la determinación de la selectividad del método con respecto al cobalto. Los resultados obtenidos se representan en el Cuadro 2.
Cuadro 2. Medición de estándares de 5.0 mg/L adicionando diferentes cantidades de cobalto
| Co agregado | [200]Au obtenido |
|---|---|
| 0.0 mg/L | [203]4.97 mg/L |
| 1.0 mg/L | [206]4.93 mg/L |
| 3.0 mg/L | [209]4.91 mg/L |
| 5.0 mg/L | [212]4.78 mg/L |
Los resultados obtenidos en la determinación de la selectividad del método indican que conforme aumenta la cantidad de cobalto presente en la muestra, la cantidad de oro medida por el equipo disminuye, aun cuando se tenga certeza que la concentración de analito se mantuvo constante en todas las mediciones. Esto confirma que la presencia de cobalto inhibe la señal del analito, por lo que representa una interferencia en la cuantificación de oro. Sin embargo la cantidad de cobalto presente en las muestras es muy pequeña, por lo tanto no se espera que afecte la veracidad del método.
En la determinación del intervalo de trabajo, se estimó de 0.01 mg/L hasta 10 mg/L. Esto lo respalda Rodríguez et al [11] que menciona que el rango en el cual el oro presenta linealidad es de 2 mg/L a 7 mg/L.
Además de lo anterior, Mongay [16] indica que la precisión con la que se determina el valor interpolado aumentará conforme la señal analítica se aproxime a la correspondiente a la concentración media de los patrones. En otras palabras, lo ideal es que las valores interpolados sean lo más semejantes posibles a la concentración media de la curva de calibración.
Debido a que las concentraciones esperadas de las muestras son de 4 mg/L y 6 mg/L de oro, se escogió el rango de trabajo que va de 1 mg/L hasta 12 mg/L, el cual cubre holgadamente los valores esperados de las muestras y sus posibles variaciones. Una vez determinado el rango de trabajo, se deben verificar una serie de aspectos que aseguren la confiabilidad de los resultados dentro del rango seleccionado. Para ello, el siguiente parámetro que debe incluirse dentro del proceso de validación es la linealidad, la cual se divide en dos partes, linealidad del sistema y linealidad del método. Debido a que ya se demostró que la cuantificación de oro por Absorción Atómica no presenta un buen ajuste lineal, no se realizó el estudio de linealidad como tal, ya que se caería en un error de definición. Tomando en cuenta esto, a partir de ahora se trabajara con la regresión, tanto del sistema como del método, adoptando las metas que se proponían para una regresión lineal. El análisis de regresión del sistema arrojó resultados satisfactorios para la medición de tres curvas de calibración a 5 niveles de concentración cada una.
Dada la importancia del coeficiente de determinación y su implicación sobre el modelo de regresión y el ajuste seleccionado, la regresión obtenida para el sistema con un ajuste cuadrático tiene un coeficiente de determinación de 1.00, lo cual sobrepasa el valor establecido como objetivo de 0.995.
Además de verificar visualmente el comportamiento de la regresión y el valor del coeficiente de determinación, se deben analizar otros aspectos para confirmar el buen ajuste de la regresión del sistema. Uno de ellos es la homocedasticidad, la cual según Rial y Mallou [20] es la homogeneidad de las varianzas de los grupos a comparar.
Para el estudio de la homocedasticidad del sistema se recurrió a la prueba de Levene, ya que según Mongay [16] es un contraste que analiza la homogeneidad de las varianzas y es menos dependiente del supuesto de normalidad.
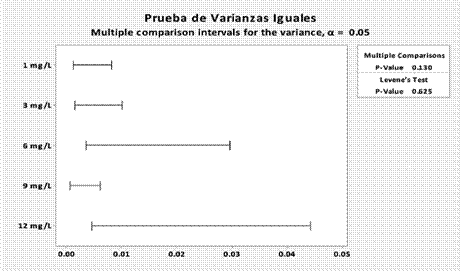
Luego de realizada la prueba de Levene, se obtuvo un valor de p = 0.625, el cual es mayor que el valor establecido de α = 0.05. Al cumplirse la condición de p >α, se concluye que todas las varianzas estudiadas son estadísticamente iguales, en este caso se compararon las varianzas de cada nivel de concentración, 1 mg/L, 3 mg/L, 6mg/L, 9 mg/L y 12 mg/L.
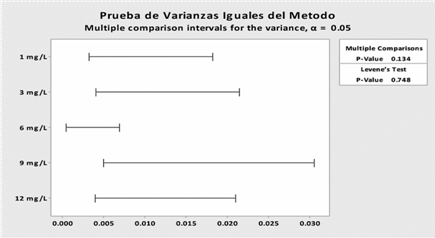
Para representar de una forma más clara el cumplimiento de la homocedasticidad de la regresión del sistema, a continuación se muestran los resultados de manera gráfica según se ilustra en la Figura 8.
En la figura anterior, se observa como todas las varianzas se sobreponen en algún punto, por lo tanto se concluye que todas las varianzas son iguales. Adicionalmente se muestra el valor de p = 0.625 obtenido en la prueba de Levene, lo cual confirma la igualdad entre las varianzas de cada nivel de concentración.
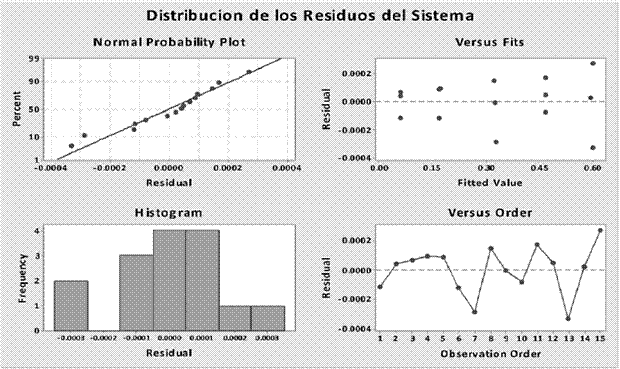
El siguiente aspecto relacionado con la regresión del sistema fue la distribución de los residuos. Anteriormente se explicó la importancia de los mismos, sin embargo es necesario recordar que los residuos deben tener una distribución normal alrededor de cero.
A diferencia del caso anterior donde solo se presentó un gráfico de la distribución de los residuos, para el análisis de la regresión, tanto del sistema como del método, se presentaran una serie de gráficos relacionados a los residuos para tener un panorama más amplio de los mismos. En el análisis de los residuos de la regresión del sistema se obtuvieron los resultados que se muestran en la Figura 9.
La interpretación de los residuos sigue siendo la misma que la presentada anteriormente, deben estar distribuidos aleatoriamente alrededor de cero. Lo anterior implica que los residuos presentan una distribución normal, lo cual es el objetivo que se pretende alcanzar, ya que según Mongay [16] se acepta que los residuales tengan una distribución normal.
Sobre el tema de normalidad de los residuos, en la Figura 9 se muestran dos representaciones típicas de normalidad. En el primer recuadro se observa el resultado de un análisis de normalidad, el cual tuvo un resultado satisfactorio, ya que se aprecian todos los residuos siguiendo la tendencia central, marcada por una línea. Además, se presenta un histograma con las frecuencias de los residuos, el cual tiene similitud a la campana de Gauss; y según Mongay [16] las muestras tienen una distribución normal cuando sus valores se ajustan a una curva de Gauss.
Una vez obtenidos los resultados de los diferentes parámetros para evaluar la regresión con ajuste polinómico del sistema, se puede concluir que el ajuste seleccionado cumple con los objetivos establecidos previamente. Ahora se debe analizar la regresión con ajuste polinómico del método, siguiendo los mismos procedimientos y los mismos criterios de aceptación que los fijados para la regresión del sistema.
Se prepararon y se midieron blancos enriquecidos a los mismos niveles de concentración que los evaluados para la regresión del sistema, obteniendo excelentes resultados, ya que, una vez más existe una relación entre ambas variables, concentración y absorbancia, lo que se confirma con la obtención de un coeficiente de determinación de 1.00, el cual supera la meta establecida de 0.995.
Con respecto a la homocedasticidad, la prueba de Levene obtuvo un resultado de p=0.748, valor que es mayor que α = 0.05. Esto indica que las varianzas estudiadas son iguales, lo que quiere decir que la regresión del método presenta la misma varianza en todos los niveles de concentración. Lo anterior se aprecia de una mejor manera en la Figura 10.
La Figura 10 demuestra que la varianza es la misma en todos los niveles de concentración, por lo tanto, la regresión con ajuste polinómico del método presenta homocedasticidad.
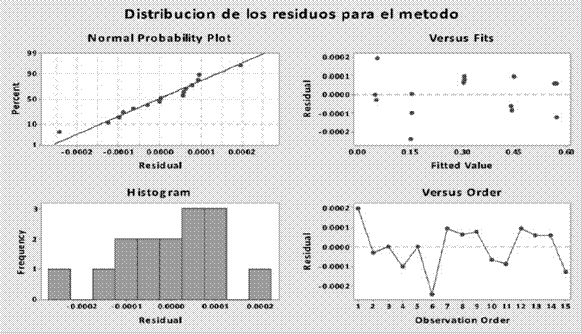
Finalmente, el estudio de los residuos de la regresión muestra que los mismos se encuentran distribuidos normalmente alrededor de cero, además no se presentan tendencias que indiquen una mala correlación entre las variables. Esto se aprecia gráficamente en la siguiente Figura 11.
Como se aprecia en la figura anterior, los residuos tienen un comportamiento lineal, que es lo más deseado. Además el coeficiente de determinación fue de 1.00 superando el objetivo de 0.995; y la prueba de Levene demostró que no hay diferencia entre las varianzas de los diferentes niveles de concentración, por lo tanto la regresión con ajuste polinómico del método presenta homocedasticidad. Tomando en cuenta lo mencionado anteriormente, se puede concluir que la regresión con ajuste polinómico del método cumple satisfactoriamente con los objetivos establecidos.
El siguiente parámetro incluido dentro de la validación fue la precisión del método, la cual toma en cuenta repetibilidad y precisión intermedia. En el caso de la repetibilidad, Mongay [16] indica que se establece como la precisión de un método en función de análisis independientes realizados por un mismo analista, en el mismo laboratorio, con la misma técnica y el mismo instrumento en un intervalo corto de tiempo.
Bajos esas condiciones, se realizó la determinación de la repetibilidad del método analítico de Absorción Atómica. Se analizaron seis muestras, tres con concentraciones esperadas cercanas a 4.0 g/L y tres con concentraciones esperadas de 6.0 g/L, debido a que las concentraciones mencionadas son las que se espera que determine en método que se encuentra en validación.
Entre las tres muestras con concentraciones bajas, el valor más alto para la desviación relativa fue de 0.93%, mientras que para las muestras con concentraciones más elevadas la mayor desviación relativa fue de 0.67%. Ambos valores se encuentran muy por debajo de la desviación relativa establecida como criterio de aceptación, la cual es de 4%.
Con respecto a la precisión intermedia, el Ente Costarricense de Acreditación (ECA) menciona en su política de validación de métodos [21] que se refiere a la precisión obtenida aplicando un mismo procedimiento, sobre una misma muestra, en el mismo laboratorio, bajo condiciones diferentes de operación. Estas condiciones pueden estar relacionadas a las siguientes variables: tiempo, operador, equipamiento o calibración. La variable que se cambió para la determinación de la precisión intermedia fue el tiempo.
Luego de realizar las mediciones con las condiciones mencionadas anteriormente, pero en diferentes días, se obtuvo una desviación relativa de 1.56%. Dicho valor es más alto que los obtenidos en el análisis de la repetibilidad, pero aun así continúa siendo menor al objetivo planteado de 4%. Tomando en cuenta las desviaciones relativas obtenidas para repetibilidad y la reproducibilidad, se concluye que el método analítico de Absorción Atómica presenta una buena precisión, ya que todos los valores fueron menores al objetivo establecido.
El siguiente parámetro sometido a validación fue la veracidad del método analítico, la misma incluye el estudio de sesgo y la recuperación. Para comenzar a evaluar la veracidad, primero se analizó el sesgo del método.
El sesgo se midió utilizando un estándar de referencia certificado, esto porque como lo indica La Guía de Laboratorio de Validación de Métodos y Temas Relacionados [22] para métodos utilizados por largo tiempo dentro del laboratorio, una muestra estable puede ser utilizada para monitorear el sesgo, pero se debería utilizar un material de referencia certificado cuando se trate de las primeras mediciones realizadas.
La determinación del sesgo se realizó a tres concentraciones diferentes, una baja de 3.0 mg/L, una intermedia de 5.0 mg/L y a una concentración alta de 7.0 mg/L. Se obtuvieron sesgos relativos de 0.47% en la concentración baja, -0.08% a una concentración intermedia y de 0.37% para una concentración alta del rango comprendido.
Los tres niveles de concentración presentan un sesgo relativo menor al ±0.5% establecido como criterio de aceptación, por lo tanto se puede concluir que el método analítico de Absorción Atómica no presenta un sesgo significativo. Pero además del sesgo, se debe analizar el porcentaje de recuperación, ya que en este parámetro si interviene la matriz de la muestra.
Para el análisis de la recuperación, nuevamente se trabajaron tres niveles de concentración, los mismos que en la determinación del sesgo. Los porcentajes de recuperación obtenidos fueron de 97.22% para una concentración baja, 97.53% para la intermedia y en el caso de una concentración alta la recuperación fue de 97.33%, se puede apreciar que todas obtuvieron valores similares de recuperación.
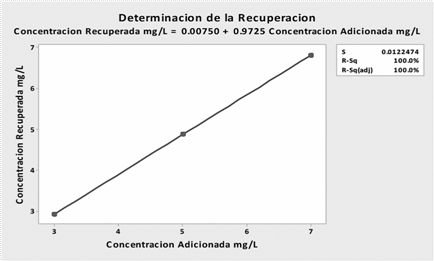
Una manera más fácil de visualizar la recuperación es mediante un gráfico (ver Figura 12), en el cual se grafica la concentración recuperada por el método contra la concentración agregada. Idealmente, el grafico debe presentar un coeficiente de determinación de 1.00, una pendiente con el mismo valor de 1.00 y un intercepto de 0.00.
En la figura anterior se muestra que, efectivamente, el coeficiente de determinación es de 1.00, sin embargo la pendiente presenta un valor de 0.9725 y el intercepto es de 0.00750. Dichos valores se acercan mucho a los valores ideales mencionados anteriormente, pero también indican que no se tiene una recuperación del 100%.
Tomando en cuenta lo mostrado en la Figura 12, así como los valores de los porcentajes de recuperación de los tres niveles de concentración, el método analítico de absorción atómica presenta una exactitud dentro del intervalo meta, el cual es de 96%-104%.
Con respecto a la veracidad del método, se confirmó, gracias a los resultados obtenidos en el sesgo relativo y el porcentaje de recuperación, que posee una buena veracidad. Esto quiere decir que el método analítico de Absorción Atómica es capaz de medir la cantidad de oro con una buena certeza de que el resultado se acerca de manera estadísticamente confiable al valor real.
Otro parámetro incluido dentro del proceso de validación fue la robustez, para el cual se realizaron mediciones sobre la misma muestra, pero cambiando algunas condiciones del análisis. Con ello se pretende detectar cuales procedimientos influyen significativamente en el resultado, y una vez detectados, poner especial énfasis sobre ellos para asegurar que el resultado del análisis sea confiable.
La primera condición que se vario fue la adición de Cloruro de Lantano LaCl3, el cual funciona como supresor de ionización. La primer medición de la muestra se realizó agregando 1ml de LaCl3, obtuvo un promedio de 4.03 g/L. La misma muestra preparada sin agregar LaCl3 dio como resultado 4.00 g/L.
Con los datos anteriores se realizó una prueba de comparación de dos medias con muestras relacionadas, dicha prueba mostro un resultado de p = 0.171, valor que es mayor que α = 0.05. Con esto se confirma que ambos valores estadísticamente no se pueden considerar diferentes y que la medición de oro no sufrió cambios significativos al no agregar supresor a las muestras.
Pese a que la adición de LaCl3 no representa ningún efecto sobre la cuantificación de oro, es importante mencionar que siempre se debe agregar a todas las muestras, ya que se observó que si es necesario para la construcción de la curva de calibración. Como lo indica Mongay [16] patrones y muestras son de la misma naturaleza y se tratan de forma idéntica a lo largo del proceso analítico.
Lo anterior indica que, aunque se demostró que no existe efecto del LaCl3 sobre las muestras, al ser necesario para los patrones de la curva de calibración debe agregarse a todas las muestras.
La otra variación realizada sobre el método de Absorción Atómica fue el uso de agua del tubo, en lugar de agua des ionizada. Esto porque al tratarse de un método donde la ionización influye en gran cantidad, se pretendía demostrar el impacto de un solvente que no estuviera libre de iones. De igual manera, se midió la misma muestra en dos ocasiones, una utilizando agua desionizada como solvente, y otra utilizando agua del tubo. El promedio obtenido para el primer caso fue de 3.43 g/L, mientras que para la segunda condición fue de 3.46 g/L. Se realizó la misma prueba de comparación entre dos medias con muestras relacionadas y obtuvo un valor de p = 0.164, el cual nuevamente fue mayor que α = 0.05, por lo tanto se asegura que no hay diferencia significativa entre ambos promedios. Esto indica que no se presenta ningún efecto al utilizar agua del tubo como solvente en lugar de agua desionizada.
Tomando en cuenta los resultados de las variaciones efectuadas deliberadamente al método analítico de Absorción Atómica, se concluye que dicho método es robusto, por lo tanto se espera que responda de forma correcta cuando se esté empleando en los análisis de oro.
El aspecto final relacionado con el proceso de validación es el cálculo de la incertidumbre del método analítico. Para ello, primero se calculó una incertidumbre combinada, tomando en cuenta aspectos como precisión intermedia, el equipo de Absorción Atómica y el material volumétrico utilizado. Dicha incertidumbre obtuvo un valor de ± 0.137 g/L.
Sin embargo, lo ideal es abarcar un rango más amplio de valores dentro de la incertidumbre para darle más confiabilidad al resultado reportado. Con respecto a ello, Remache [23] menciona que con el fin de incrementar la confiabilidad la incertidumbre combinada se multiplica por un factor de cobertura que generalmente es cercano a 2 y se representa con la letra “k”. La incertidumbre resultante es llamada “incertidumbre expandida” (U), y es la que típicamente se reporta en un informe de ensayo o calibración. La incertidumbre expandida, utilizando un factor de cobertura de dos, es de ± 0.274 g/L. El valor de incertidumbre reportado es de ± 0.3 g/L con un nivel de confianza del 95%.
Tomando en cuenta todos los parámetros evaluados dentro del proceso de validación del método analítico de Absorción Atómica, a continuación, en el cuadro 3 se presenta un resumen con los resultados obtenidos para cada parámetro, así como su criterio de aceptación.
Con base en los resultados mostrados en el Cuadro 3, se puede efectuar la declaratoria de conformidad para el método analítico de Absorción Atómica. El método sometido al proceso de validación cumple satisfactoriamente con los criterios de aceptación para todos los parámetros analizados.
Cuadro 3 Resultados de la validación del método analítico para cuantificar oro por Absorción Atómica
| Parámetro | [283]Criterio de Aceptación | [284]Resultado Obtenido en la Validación |
|---|---|---|
| Especificidad | [287]Interceptos de estándares y blancos enriquecidos cercanos a 0.000 | [288]Intercepto de estándares = 0.000695 [289] Intercepto de blancos enriquecidos = [290] 0.000491 |
| Selectividad | [293]Debe detector únicamente la señal del analito | [294]El cobalto inhibe la señal del analito |
| Linealidad del Sistema | [297]R2> 0.995 [298] Homocedasticidad p > 0.05 Residuos aleatorios | [299]R2 = 1.00 [300] Homocedasticidad p = 0.625 Residuos aleatorios |
| Linealidad del Método | [303]R2> 0.995 [304] Homocedasticidad p > 0.05 Residuos aleatorios | [305]R2 = 1.00 [306] Homocedasticidad p = 0.748 Residuos aleatorios |
| Precisión | [309]Desvío Relativo < 4.0% | [310]Repetibilidad 0.93% y 0.67% Precision Intermedia 1.56% |
| Veracidad | [313]Sesgo Relativo < ± 0.50% Recuperación 96% - 104% | [314]Sesgo [315] - Concentración baja 0.47% [316] - Concentración media -0.08% [317] - Concentración alta 0.36% Recuperación [318] - Concentración baja 97.22% [319] - Concentración media 97.53% [320] - Concentración alta 97.33% |
| Ámbito | [323]--------- | [324]De 1 mg/L hasta 12 mg/L |
| Robustez | [327]El método debe permanecer invariable ante cambios deliberados | [328]La ausencia de supresor de ionización en las muestras y el uso de agua del tubo como solvente no tienen efecto sobre los [329] resultados |
| Incertidumbre | [332]--------- | [333]± 0.3 g/L |
Consideraciones finales
Las técnicas analíticas de Absorción Atómica y de Espectroscopia de Fluorescencia de Rayos X son capaces de realizar una cuantificación de oro en soluciones cianuradas, para lo cual se recomienda utilizar un ajuste polinómico en el modelo regresión, para ambas técnicas, con el fin de obtener los mejores resultados. Aun así, la cuantificación de oro por Absorción Atómica presentó mejores resultados en términos de exactitud, con respecto a la Espectroscopia de Fluorescencia de Rayos X, y se evidenció que existe una diferencia estadísticamente significativa en la medición de una misma muestra con ambas técnicas analíticas.
En la validación del método analítico por Absorción Atómica, la regresión del método analítico obtuvo un coeficiente de determinación de 1.00, sobrepasando el objetivo establecido de 0.995. La prueba de Levene muestra que la varianza es la misma para todos los niveles de concentración, por lo tanto presenta homocedasticidad; finalmente los residuos reflejan un comportamiento normal, lo cual es contundente para aseverar que el método es apropiado para cuantificar oro.
La matriz de las muestras tiene un papel muy importante en la cuantificación de oro, ya que durante el proceso de validación, específicamente la selectividad y la especificidad, se demostró que disminuye la señal del analito ante la presencia de interferencias como el cobalto, en este caso específico.
El método de Absorción Atómica presenta buena veracidad, ya que el porcentaje de recuperación obtenido es bastante alto, cercano al cien por ciento en tres concentraciones diferentes ensayadas, y el análisis de la robustez muestra que dicho método se mantiene invariable ante situaciones inesperadas cuando se utilice para realizar la cuantificación de oro.
Por último, el método analítico sometido al proceso de validación cumple satisfactoriamente con los criterios de aceptación de los parámetros validados, por lo que se declara conforme y apto para su uso bajo las condiciones aquí indicadas.