Introducción
La especie Plantago major es una planta herbácea, procedente de la familia Plantaginaceae. Se caracteriza por poseer una altura aproximada de 15 cm, con hojas en forma de roseta ovaladas hasta elípticas; presenta inflorescencias tipo espigas en colores del café al verde que dan origen a gran cantidad de semillas diminutas, alrededor de 20 mil por planta, contenidas en cápsulas [1]. En la semilla se ha determinado la presencia de triterpenos, iridoides, aceites fijos, alcaloides monoterpénicos y carbohidratos. Además, se conoce de la presencia de otros compuestos, principalmente en órganos aéreos, como es el caso de alcaloides como la plantagonina, flavonoides como luteolinas, hispidulinas, baicaleina, plantaginina y homoplantaginina, algunos de los cuales tienen propiedades antioxidantes; los glicósidos iridoides como la aucubina, se consideran responsables tanto de la capacidad antiinflamatoria como de la acción antiespasmolítica [2]-[3].
En el seguimiento de investigaciones acerca de esta especie y su potencial para la producción de compuestos bioactivos, la técnica de inducción de cultivos celulares se plantea como una prometedora opción para el estudio a nivel celular de la presencia de estos compuestos y la posibilidad de su producción a mayor escala. Con el uso de la técnica de cultivos celulares, se minimiza el gasto energético de regenerar plantas completas y se incrementa el nivel de asepsia del manejo de los compuestos de interés farmacológico. Este modelo facilita la realización de estudios in vitro con independencia de los factores climatológicos que afectan las condiciones de producción de los compuestos a nivel del desarrollo fenológico de las plantas. Además bajo esta técnica, los compuestos de interés presentes bajo estas condiciones “celulares” pueden ser identificados, estudiados y cuantificados, con el apoyo de técnicas cromatográficas y espectrofotométricas sin la interrupción o ruido químico que representa la clorofila y los demás componentes propios de una planta.
Para el caso específico de P. major y P. lanceolata, ambas son especies empleadas en el tratamiento de cicatrización de heridas, abscesos y acnés; internamente para el tratamiento de la diabetes, infecciones urinarias, cáncer, infecciones virales, entre otras. En general, el género Plantago sp. se caracteriza por su actividad antitumoral, antiinflamatoria, antifúngica, antibacteriana, analgésica, antiespasmódica, antiviral y hepatoprotector. Las propiedades mencionadas podrían aprovecharse para combatir uno de los principales problemas de salud actuales, el cáncer, que se define como una proliferación celular incontrolada, y que, como se mencionó, es una enfermedad grave que amenaza a la salud humana con una morbilidad y mortalidad considerables, razón por la cual, las investigaciones sobre los compuestos antioxidantes con potencial para tratar este mal adquieren gran relevancia [4].
Este trabajo tuvo por objetivo generar una exploración inicial y sistematizada en el estudio y detección de los compuestos bioactivos de P. major por medio del establecimiento de un sistema de callogénesis somática. Así mismo se logró la implementación de una metodología estandarizada para la preparación de extractos a partir de callos liofilizados de P. major en los cuales se pueda detectar la presencia de los principales compuestos bioactivos con propiedades cicatrizantes y antimicrobianas.
Metodología
Germinación de semillas provenientes de campo: Las semillas requeridas para la introducción in vitro del material fueron facilitadas por Laboratorios Lisan, a partir del material de campo con el que cuentan para su Departamento de Investigación y Desarrollo. El protocolo de desinfección de semillas se estableció a partir del elaborado por Garro y Alvarenga [3] y consistió en los siguientes pasos: Se extrajeron las semillas de la cubierta externa, se lavaron con agua destilada y 2 gotas del producto comercial Tween 20, durante 15 minutos en agitación; posteriormente se colocaron en una solución de Agrymicin® y Benlate® en concentración de 1 g/l de cada uno, durante 30 minutos en agitación; en cámara de flujo laminar se lavó las semillas con agua destilada estéril para ser trasladadas a una solución de hiploclorito de sodio (3.5% i.a.) al 85% durante 40 minutos en agitación, finalmente se lavaron con agua destilada estéril y se introdujeron en un medio de cultivo semisólido con sales y vitaminas M&S [5] al 50%, suplementado con 3% m/v de sacarosa y pH 5,7. Por otra parte, el medio de multiplicación también semisólido se compuso de sales y vitaminas M&S [5] al 100 %, con 3% m/v de sacarosa y pH 5,7.
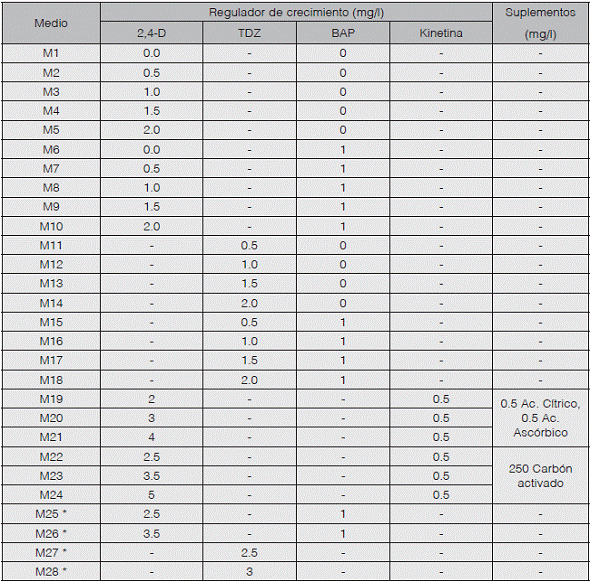
Establecimiento de cultivos celulares: El establecimiento de cultivos celulares de P. major se realizó a partir de explantes de 1 cm2 de hoja in vitro joven, colocando el envés de la hoja en contacto directo con el medio. El medio de inducción de callogénesis contuvo una base de sales y vitaminas M&S [5] al 100 %, suplementado con 3% m/v de sacarosa y pH 5,7, excepto para los medios 25, 26, 27 y 28. En total se elaboraron 28 medios de cultivo diferentes en los que la principal modificación fue el uso de los reguladores de crecimiento 2,4-D y tidiazurón (TDZ) en diferentes concentraciones (cuadro 1). Los explantes fueron colocados a una temperatura de 22°C y en condiciones de oscuridad durante 3 semanas.
El crecimiento celular indiferenciado fue evaluado de acuerdo con las variables cualitativas de color, porcentaje de formación de callo y friabilidad. Se excluyó la evaluación de las variables cualitativas de peso seco y fresco debido a la pérdida de material in vitro que esto suponía, principalmente ante el requerimiento de material para la elaboración de extractos crudos. Una vez alcanzada la desdiferenciación celular, los callos fueron subcultivados en el mismo medio de inducción, pero suplementado con 250 mg/l de carbón activado.
Cuantificación de metabolitos secundarios: El personal de Laboratorios Lisan trabajó en el desarrollo de una metodología para la selección de un marcador químico apropiado para ser utilizado en la cuantificación de extractos de P. major, basados en la técnica de HPLC. Todos los protocolos ejecutados en esta sección de la investigación son propiedad exclusiva de Lisan S.A. Se ejecutaron análisis de dos estándares para comprobar su efectividad como marcadores químicos para la cuantificación de verbascósidos e iridoides con base en aucubina en P. major. Como segundo paso, se realizaron las cuantificaciones de los analitos mencionados, en muestras liofilizadas de callo. Los extractos hidro-alcohólicos crudos de P. major, elaborados por Laboratorios Lisan, se prepararon en una concentración de 10% p/v utilizando etanol al 95 %.
Resultados
Germinación in vitro de semillas provenientes de campo
El porcentaje de germinación promedio en el laboratorio, para las semillas de P. major fue de 98%. En la Figura 1 se presentan fotografías del desarrollo in vitro de las plántulas.
Establecimiento de callogénesis somática
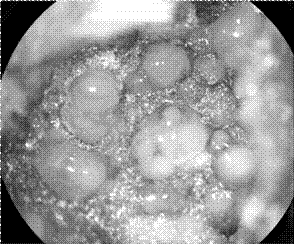
Los resultados más favorables para la inducción de callo en P. major se generaron con los medios M14, M27 y M28 (Cuadro 2). En las Figuras 2 y 3 se presentan fotografías del proceso de desdiferenciación celular obtenido.
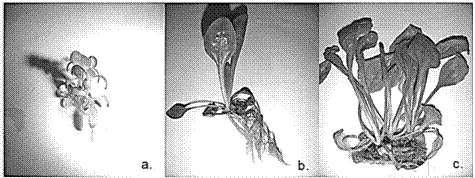
Figura 1: Plántulas in vitro de Plantago major en diferentes estadíos: a. Introducción, b. Micropropagación, c. Aclimatación.
Cuadro 2 Evaluación de medios de cultivo utilizados en la inducción de callogenésis en Plantago major.
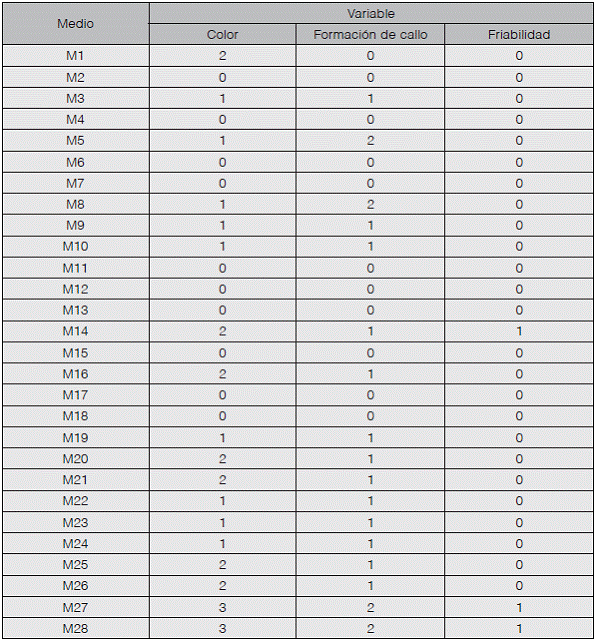
Donde
Color: 3 - Amarillo cremoso Formación de callo: 3 - 100% callo formado Friabilidad: 1 - Sí
2 - Amarillo verdoso 2 - 50% callo formado 0 - No
1 - Café amarillo 1 - Inicio de callo
0 - Café 0 - Ausencia de callo:

Figura 2: Inducción de callogénesis en Plantago major: a. Subcultivo de callo, b. Estructuras en forma de torpedo evidenciando el proceso de Embriogénesis somática
Cuantificación de metabolitos secundarios
Cuantificación de Cinamatos. Estándar: Verbáscosido
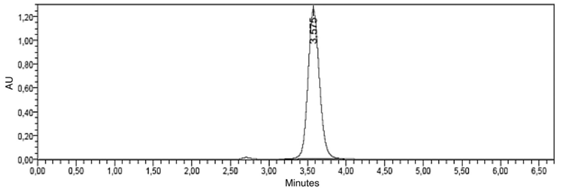
A partir del estándar se dio una buena resolución en el cromatograma y se tuvo una línea base estable además de una buena señal (Figura 4); por tanto, se continuó con la cuantificación de cinamatos en muestras liofilizadas de cultivos celulares de llantén (Figura 5).
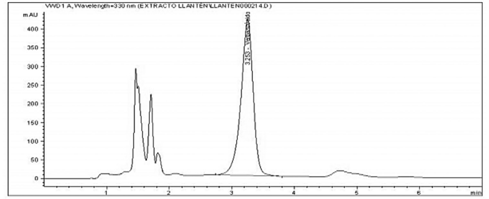
Figura 5: Análisis de Cinamatos en el día de la extracción a partir de muestra de extracto de callo liofilizado de P. major.
Cuantificación de Iridoides. Estándar: Aucubina
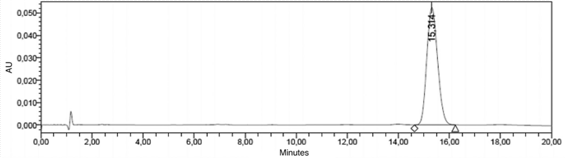
Se obtuvo una señal con línea base estable y buena resolución. Sin embargo, como se puede observar en la figura 5, el tiempo de retención es alto, por lo que la duración de cada una de las inyecciones debe ser de 20 min como mínimo (Figura 6); se continuó con la cuantificación de iridoides en muestras liofilizadas de cultivos celulares de llantén (Figura 7).
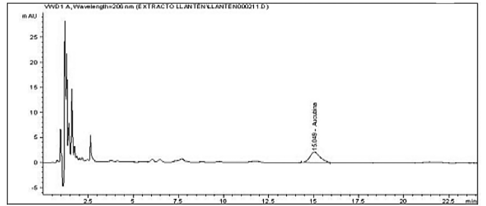
Figura 7: Análisis de Iridoides en el día de la extracción a partir de muestra de extracto de callo liofilizado de P. major.
Como se puede observar en los resultados de las figuras 6 y 7 se logró detectar en niveles apreciables o significativos la presencia de los metabolitos secundarios tales como verbascósidos e iridoides (aucubina) con importancia biológica reportados en la planta y a los cuales se les atribuye el mayor potencial como cicatrizantes y antimicrobianos respectivamente. No obstante, la cuantificación fue efectiva únicamente el día de la extracción ya que los cromatogramas de cuantificaciones en días posteriores, mostraron una degradación progresiva de los metabolitos de interés.
Discusión
Plantago major es una planta medicinal que ha sido catalogada como de crecimiento espontáneo. Estas plantas se caracterizan por un rápido crecimiento y adaptabilidad a su hábitat que le permiten sobrevivir aún en condiciones ambientales poco favorables [6]. La razón anterior es quizás la que más benefició el rápido establecimiento in vitro del material, el cual prácticamente subsiste con un medio basal, como lo es el M&S [5], sin necesidad de añadir ningún otro regulador de crecimiento. Se considera que un porcentaje de germinación in vitro de semillas del 98% es sumamente prometedor, tanto en términos de viabilidad de la semilla como de éxito con el protocolo de desinfección propuesto.
En campo, Laboratorios Lisan ha logrado establecer una cultivo de esta planta en condiciones favorables y con conocimiento sobre las variables que influyen directamente en su desarrollo, incluyendo la composición del suelo [7] . Por lo anterior, se determinó que este sería un buen semillero para la colecta de material para la introducción in vitro.
Así mismo, el establecimiento del material multiplicado fue sencillo, ya que la planta regenerada no presentó requerimientos nutricionales extra, y su traslado a nuevo medio pudo realizarse de manera mensual, con el fin de mantener un lote de material joven para ser utilizado en la etapa de inducción de callogénesis.
Los cultivos celulares de llantén fueron establecidos en un medio basal M&S [5] al 50%, lo que nos indica que los requerimientos de sales y vitaminas se ve disminuido con respecto a la etapa de multiplicación. El medio de callogénesis 14 fue suplementado con el regulador 2,4-.D, auxina comúnmente empleada para este fin [8], mientras que los medios de cultivo 27 y 28 fueron suplementados con TDZ (citocinina), el mismo ha sido reportado en diversas publicaciones científicas relacionadas con el cultivo de tejidos vegetales para la inducción de callogénesis a través de la promoción de la proliferación celular [9]. Lo anterior respalda el éxito en esta etapa.
El cambio a un pH más neutral evitó en gran manera la oxidación de los explantes, de esto se puede inferir que probablemente durante el proceso de desdiferenciación se generan ácidos que ocasionan una disminución del pH, el cual al inicio de las pruebas se mantenía en 5,7, o bien, el empleo de derivados de úrea como el TDZ promovió también la acidificación del medio de cultivo.
Se conoce que el grado de acidez o alcalinidad en el medio de cultivo es específico para cada planta, y va a incidir tanto en el aprovechamiento de los compuesto como en la liberación de compuestos fenólicos; el rango de pH normal para el crecimiento de plantas está entre los 4,5 y 7, por lo que es necesario buscar su ajuste según la especie [10]. Aún así, es importante considerar la sinergia que existe entre los factores pH, temperatura y luz para la inducción de procesos de desdiferenciación celular [11].
El uso de maltosa como fuente de carbono retrasa el proceso de desdiferenciación celular en llantén, lo que resultó de utilidad para evitar una rápida oxidación en cortos períodos y en sí, una formación de callo mayor y más efectiva. El uso de carbohidratos en los medios de cultivo de tejidos vegetales se da para su aprovechamiento como fuentes de carbono y también como reguladores osmóticos en el medio de cultivo; siendo los dos usos anteriores críticos para el desarrollo de callos y embriones. Se ha reportado que el remplazo de la sacarosa por maltosa es de gran utilidad no sólo en la inducción de callos, sino también, en la regeneración de plántulas a partir de los mismos [12].
Para poder definir un protocolo de cuantificación de metabolitos, primero es necesario definir el marcador químico que se empleará como referencia base para medición de los analitos de interés. En esta etapa Laboratorio Lisan, seleccionó 2 posibles marcadores, verbascósido y aucubina. La selección anterior se fundamenta en que la aucubina junto con el catalpol y el o-catalpol, son tres de los compuestos iridiodes más representativos en plantas medicinales; en cuanto al verbascósido, éste forma parte del grupo de los fenilpropanoides, por lo que puede emplearse como una medida de referencia para la presencia de los ácidos cinámicos en plantas. Además, a la explicación anterior se debe añadir que los compuestos iridoides guardan relación con propiedades antibacterianas, mientras que a los fenilpropanoides se les atribuyen efectos analgésicos, bactericidas (especialmente el verbascósido) y antidepresiva [13]- [ 14].
Con el análisis mediante HPLC para ambos marcadores se generaron señales con línea base estable y buena resolución, siendo más efectivo el de verbascósido, por lo que se continuó con las pruebas necesarias para lograr establecer un protocolo de cuantificación en callos de llantén. A pesar de las pruebas de resuspención de los extractos en distintos solventes (agua y alcohol) y fases móviles, fue evidente que los analitos de interés, en este caso, iridoides y ácidos cinámicos, no podían ser efectivamente detectados después de un día de extracción dada su degradación en la muestra. De aquí surge la urgente necesidad de establecer nuevas estrategias de extracción, a partir de una hidrólisis ácida, por ejemplo, para lograr la cuantificación de ácidos cinámicos a partir del estándar de verbascósidos. La idea sería lograr la estabilidad del extracto de manera que sus compuestos activos permanezcan viables durante un período mayor a sólo 24 horas. En este caso, se buscaría estandarizar sólo un protocolo y descartar el uso de la aucubina.
Conclusiones
La metodología implementada para la inducción de callogénesis somática fue efectiva en lograr la proliferación adecuada de los callos y promover la formación de estructuras globulares proembriogénicas. Estos resultados son relevantes pues a pesar de que no se pretende aún la regeneración de plantas, si resulta muy positivo el contar con un sistema de callogénesis que además permita la embriogénesis somática.
El estudio que ha realizado el Departamento de Investigación y Desarrollo de Laboratorios Lisan en los últimos años ha demostrado que los marcadores químicos aucubina y verbascósido no son los apropiados para el análisis de P. major, ya que estos compuestos se degradan rápidamente en los extractos. Gracias a estos resultados, se trabaja en el desarrollo de un método de ensayo basado en la hidrólisis ácida para la cuantificación de ácidos cinámicos totales.
Los extractos producidos a partir de callos somáticos de Plantago major pueden ser utilizados para detectar la presencia de los verbascósidos e iridoides relacionados con las propiedades de cicatrización de heridas y actividad antimicrobiana. Los ensayos de la actividad de los extractos sobre tejidos celulares en modelos in vitro y en vivo se realizarán en futuras investigaciones para los cuales podrá ser adecuado el ensayo con compuestos y condiciones inductoras que promuevan una mayor producción de los compuestos in vitro.