Introducción
El arándano es un arbusto de la familia de las ericáceas, género Vaccinium. Sus frutos son bayas de color oscuro, azuladas o rojizas, ricas en antocianos y minerales. Sus cualidades nutricionales y antioxidantes hacen del arándano un fruto de alto valor medicinal y nutricional.
Estudios recientes (Jiménez-Bonilla & Abdelnour-Esquivel, 2013) confirmaron el valor nutricional del arándano nativo de Costa Rica. Se compararon los índices de actividad antioxidante mostrados para arándanos comerciales (94 y 92 µM de Trolox equivalente/g muestra fresca) (Inkanatural, 2008), los cuales son menores a los arrojados por los análisis de los arándanos silvestres en el estudio (entre 550 y 650 µM). Además, los valores reportados para ciruela (73), mora (53), frambuesa (48), manzana (43) y naranja (18), entre otros (Inkanatural, 2008), también muestran valores muy inferiores a los determinados en los materiales silvestres analizados.
Desde hace algunos años, los principales supermercados de Costa Rica importan esta fruta procesada en diferentes presentaciones (jugos, mermeladas, toppings, pasteles y otros) y más recientemente como fruta congelada. PROCOMER (2012) señala que las frutas de Vaccinium se importan desde Chile, Colombia, México y Estados Unidos y que las divisas invertidas para ello han ido en aumento en los últimos años, pasando de US$48.000 en 2007 a US$215.100 en 2013, lo que muestra el incremento en el consumo nacional de estas frutas. Sin embargo, por su alto precio en el mercado nacional, es probable que su consumo esté limitado a un sector selecto de la población. Con base en estos resultados, así como en la información sobre el aumento en el consumo de arándano y las crecientes divisas que invierte el país en la importación de productos a base de esta fruta, se evidenció la necesidad de incentivar y apoyar las iniciativas de domesticar estas plantas para introducirlas en la producción comercial.
La micropropagación es una de las técnicas que permiten lograr plantas con características genéticas similares a la que les dio origen. Una de sus etapas es el establecimiento in vitro, que está limitado por la ocurrencia de contaminantes fúngicos y bacteriológicos que colonizan el explante y el medio de cultivo, ocasionando su muerte y oxidación. Este constituye uno de los problemas más serios y frecuentes, tanto al inicio del proceso como durante el mantenimiento de un tejido cultivado in vitro y se considera la mayor limitante del desarrollo de un protocolo de micropropagación. Por lo anterior, se desarrolló este estudio de establecimiento in vitro de miniestacas tomadas de material que crecía en campo, con el fin de sentar las bases del protocolo de micropropagación de esta especie.
Materiales y métodos
Recolección
Se seleccionó el material de arándano identificado previamente como “Las Torres 2”, localizado en el Cerro de la Muerte, que mostró, durante estudios previos, tener las características deseables para la producción comercial (color, tamaño y sabor) y los mayores contenidos de antioxidantes de los materiales evaluados (Cuadro 1). Se realizaron 16 giras de recolección por año. Se recolectaron tallos jóvenes poco lignificados, que se envolvieron en papel toalla humedecido con agua y se colocaron en una hielera para su traslado al laboratorio de cultivo de tejidos del Centro de Investigaciones en Biotecnología (CIB), del Instituto Tecnológico de Costa Rica.
Establecimiento in vitro
Los tallos recolectados se seccionaron en estacas que contenían de 2 a 3 nudos y se eliminaron las hojas. Posteriormente, se lavaron con agua y jabón quirúrgico en forma individual con ayuda de un cepillo suave, se enjuagaron tres veces con abundante agua y se sometieron a diferentes tratamientos con desinfectantes (Cuadro 2).
Cuadro 2 Tratamientos desinfectantes, concentraciones y tiempos de incubación de las miniestacas de arándano (Vaccinium consanguineum)
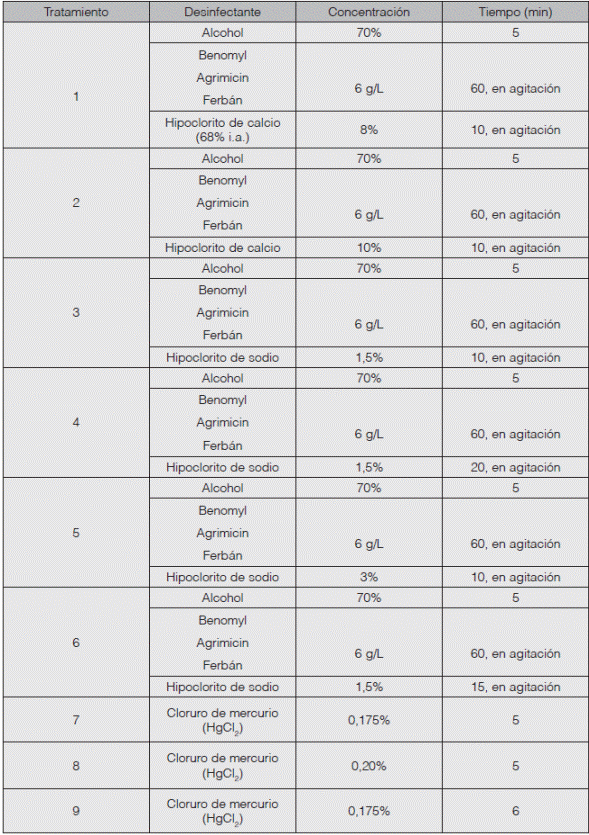
Después de cada tratamiento de desinfección se realizaron al menos tres enjuagues con agua destilada estéril en la cámara de transferencia de flujo laminar y durante la siembra en los envases de cultivo el material vegetal se mantuvo en una solución antioxidante de 500mg/l de ácido cítrico y 250 m/l de ácido ascórbico (previamente esterilizados). Se sembró un explante por envase de cultivo conteniendo 20 ml del medio descrito por Murashige y Skoog (MS) (1962) en ausencia de reguladores de crecimiento, con un pH ajustado a 5,7.
Se colocaron los explantes en el cuarto de crecimiento, con una temperatura ambiente de 21 ºC a 22 ºC en la oscuridad durante ocho días. Posteriormente, se mantuvieron en el mismo cuarto de crecimiento pero en luz directa (2000 Lux), con un fotoperiodo de 16 horas luz. También se evaluó el efecto de temperaturas mayores y menores sobre la brotación de las yemas, colocando los explantes en un cuarto de crecimiento con una temperatura de 27 ºC y dándoles un pretratamiento de frío a 5 ºC en la refrigeradora.
Cada unidad experimental consistió de un explante por envase de cultivo con 50 repeticiones y cada experimento se repitió al menos dos veces. La evaluación se realizó semanalmente durante ocho semanas, tomando en cuenta el número de explantes establecidos de manera aséptica, explantes contaminados (hongos-bacterias), oxidados y muertos.
Resultados
Establecimiento in vitro
El análisis de varianza (ANOVA) evidenció diferencias significativas entre los tratamientos. Para la desinfección, los tratamientos 1, 2, 3 y 4 resultaron estadísticamente iguales entre sí; los tratamientos 7 y 8 estadísticamente similares entre sí. Sin embargo, los tratamientos 5 y 6 presentaron diferencias significativas con respecto a los primeros mencionados; los tratamientos 7 y 8 guardan similitud entre ellos y con el tratamiento 9. El tratamiento que permitió los menores porcentajes de oxidación de explantes fue el No. 9, pero no presentó diferencia estadística significativa con respecto al tratamiento 8.
El uso de hipoclorito de calcio en las concentraciones y tiempos de incubación evaluados permitió altos porcentajes de contaminación de miniestacas, lo mismo que los tratamientos que incluyeron la incubación en hipoclorito de sodio al 1,5% i.a. durante 10 y 20 min (tratamientos 1, 2, 3 y 4) (entre 80% y 90% de contaminación). Por otra parte, al aumentar la concentración de hipoclorito de sodio al 3% y realizar la incubación por 10 y 15 min, los porcentajes de contaminación disminuyeron significativamente (55% y 50% de miniestacas contaminadas, respectivamente). El uso de cloruro de mercurio permitió la menor contaminación y el mayor porcentaje de explantes establecidos asépticamente. De acuerdo con el análisis estadístico, el mejor tratamiento consistió en la incubación en 0,2% de cloruro de mercurio durante 6 min (28% de contaminación) (Figura 1A).
También se evaluó la oxidación que presentaron las miniestacas de arándano con base en los tratamientos utilizados para la desinfección, después de ocho semanas de cultivo. La prueba de Fisher evidenció diferencias significativas entre los tratamientos. Los tratamientos 1 y 5 no presentaron diferencia estadísticamente significativa con respecto a los demás, los tratamientos 2, 3 y 4 no presentaron diferencia entre sí, los tratamientos 6, 8 y 9 tampoco mostraron diferencia significativa entre sí. Los menores porcentajes de miniestacas oxidadas se observaron en los tratamientos 7, 8 y 9 (40% de oxidación) (Figura 1B).
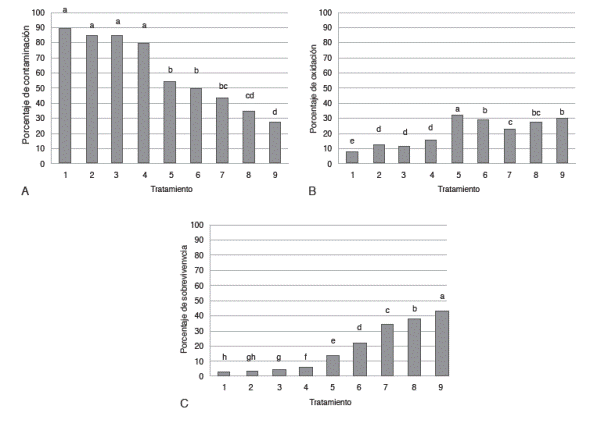
Figura 1 Contaminación (A), oxidación (B) y supervivencia (C) de miniestacas de arándano (Vaccinium consanguineum) según el tratamiento de desinfección, después de ocho semanas de cultivo.
En cuanto a la supervivencia de las miniestacas después de los tratamientos de desinfección (Figura 1C), los mayores porcentajes de explantes se observaron en los tratamientos 7, 8 y 9 (33,6%, 37,7% y 42,5%, respectivamente), aunque son estadísticamente diferentes entre sí. El tratamiento 9 permitió el mayor porcentaje de miniestacas sobrevivientes, luego de eliminar los explantes contaminados y oxidados.
Discusión
El material vegetativo obtenido directamente del campo posee en su superficie una abundante microflora que debe ser eliminada por medio de procedimientos de desinfección para cumplir con el establecimiento aséptico, el cual es la fase número uno y fundamental en cualquier metodología de propagación (George, Hall & De Klerk, 2008). En los primeros seis tratamientos de desinfección se combinó el uso de desinfectantes como biocidas de acción superficial (alcohol, hipoclorito de calcio y sodio) con dos sistémicos de amplio espectro, benomyl (Benlate®) y estreptomicina y terramicina (Agri-mycin®), tras evaluar concentraciones y tiempos de exposición que no ocasionaran daños a los tejidos. Los resultados mostraron no ser los más efectivos para la descontaminación del material (figura 1), por lo que se debe tomar en cuenta que, al ser material del campo, la probabilidad de contaminación por hongos y bacterias es grande, ya que el grado de contaminación está determinado por las condiciones climáticas de la región; es más difícil obtener explantes limpios de plantas del trópico húmedo que de las regiones frías o secas (Rathore et al., 2007).
Dado lo anterior, se recurrió al uso de cloruro de mercurio, el cual se utiliza para la eliminación exófita de microorganismos y se menciona que tiene gran acción bacteriostática y fungicida en concentraciones mayores a 0,004% (Niubóu et al., 2004). En esta investigación se determinó que, con el empleo de cloruro de mercurio al 0,02% durante 5 y 6 min, se obtuvieron bajos porcentajes de contaminación, lo que resultó muy efectivo. Tratamientos similares fueron efectivos para desinfectar propágulos de caña (Niubó et al., 2004), teca (Abdelnour & Muñoz, 2005) y amarillón (Mendez-Álvarez & Abdelnour-Esquivel, 2014), entre otros. Durante la desinfección, los explantes sufren, en mayor o menor medida, situaciones de estrés, desecación y daños mecánicos que estimulan el metabolismo de los compuestos fenólicos (López, 2004) que son tóxicos para los tejidos vegetales, provocando cese del crecimiento, oscurecimiento de los tejidos vegetales, exudados que oscurecen el medio de cultivo y en algunos casos la muerte del explante (Cáceres, 2006).
En este estudio, la oxidación fue una variable de consideración que constituyó también uno de los problemas más serios y frecuentes, provocando la muerte del material, evidenciándose en los tratamientos de desinfección utilizando desinfectantes como alcohol e hipoclorito de calcio y sodio, que aumentaron los porcentajes de oxidación. Azofeifa (2009) sugiere que los problemas de oxidación podrían reducirse con el uso de un medio líquido con carbón activado. En este estudio, los enjuagues con antioxidantes (ácido ascórbico y cítrico) y la adición de carbón activado al medio de cultivo (500mg/l) fueron efectivos para disminuir la oxidación. Sin embargo, el uso de cloruro de mercurio en bajas concentraciones y periodos cortos de contacto con el material mostró ser más efectivo, tanto para la desinfección como para la disminución de las miniestacas oxidadas, con lo que se logró disponer de material aséptico para iniciar la siguiente fase de micropropagación.














