Introducción
La Pudrición Suave del Fruto (PSF) en banano (Fruit soft rot), sinónimo de Pudrición Suave del Dedo, Pudre de Dedo y Dedo Podrido, es una enfermedad precosecha que afecta el fruto. En Centroamérica y el Caribe, en particular Costa Rica, Trinidad y Tobago, Honduras, Nicaragua y Panamá (Stover y Simmonds 1987, Guzmán y Wang 1998, Thwaites et al. 1999). Fue descrita en Costa Rica, Limón, existen registros desde 1991 aunque se reportó baja incidencia. La misma cobró importancia a partir de 1994, probablemente por la adopción de la desflora en campo y la renovación de plantaciones (Villalta et al. 2019). Se reportaron casos severos de incidencia de esta en Matina y Pococí en 1995 y 1996 (Guzmán y Wang 1998).
Se reporta como una enfermedad entre las que afectan el fruto, resultado final de las operaciones productoras de banano, una vez sometido a altas exigencias de calidad. La PSF constituye una causa importante de rechazo de fruta en las plantas empacadoras por daños desde la producción (Guzmán y Wang 1998). Se ha observado que, en plantaciones comerciales de banano, a partir del cuarto ciclo de producción, la incidencia alcanza entre 0,05 y 0,1%, que representa una pérdida entre 36 y 72 kg de fruta.ha-1.año-1. En los proyectos de renovación de plantaciones, la incidencia va desde 0,1 a 7%, equivalente a 0,3 y 1,2 Ton de fruta.ha-1.año-1. La cantidad de fruta afectada por la enfermedad asciende cuando se suman los frutos afectados indirectamente, como resultado del goteo de los exudados de las pudriciones y por el manejo operativo de las plantas empacadoras, que preventivamente rechazan fruta adyacente a los que presentan síntomas de la enfermedad por el riesgo de maduración prematura (Villalta et al. 2019).
Las pudriciones bacterianas suaves en Musáceas son causadas por especies del género Erwinia (Gowen 1995). La PSF es atribuida a Erwinia chrysanthemi (sin. Dickeya chrysanthemi) y Erwinia carotovora subsp. carotovora (Stover y Simmonds 1987, Choi et al. 1988, Samson et al. 2005, Snehalatharani y Khan 2010). En Costa Rica, antes de 1998, se había investigado esta enfermedad lo requerido, sin embargo, estudios contemporáneos a este trabajo han presentado resultados sobre los agentes causales y algunos factores que participan en el desarrollo de la enfermedad (Guzmán et al. 2017, Villalta et al. 2019). Debido a que la sintomatología de las enfermedades bacterianas es generalmente similar, se ha afirmado que varios organismos pueden coexistir en una infección de este tipo (Gowen 1995), y en otros casos, estas bacterias afectan también el pseudotallo y tejidos en descomposición de la planta de banano (Ramírez et al. 2014).
En relación con las alternativas de control de la enfermedad, las recomendaciones giran alrededor de medidas sanitarias y culturales. Por ejemplo, remover restos de la planta en descomposición, minimizar heridas en los órganos de la planta, desinfección de las herramientas que se utilizan en las labores de calidad preventiva de la fruta como apuntalar, embolsar, desmanar, desdedar, desflorar y el deschire (Agrios 2005, Martínez et al. 2000, Guzmán et al. 2017 ), además de la eliminación en campo de frutos que presentan síntomas aparentes, y la suspensión de las prácticas de calidad preventiva en campo para reducir su posible dispersión. La suma de las prácticas de control propuestas no ha logrado, hasta el momento, disminuir la incidencia de la PSF y las pérdidas económicas que genera, por lo que se hace necesario evaluar otras prácticas de control.
La evaluación in vitro de productos formulados a base de antagonistas contra la PSF es una alternativa poco estudiada en el país. En Cuba, en áreas afectadas por la pudrición del pseudotallo causada por Erwinia sp; Jiménez y Cordovés (1992), evidenciaron que especies aisladas de la rizosfera de plantas de banano tenían efecto antagonista in vitro contra aislamientos de Erwinia chrysanthemi. En esta misma línea de trabajo, se ha observado buen efecto antagonista de cepas de Bacillus subtilis (Goorani El y Hassanein 2008). También, algunas cepas de Trichoderma han sido evaluadas para el control in vitro de bacterias y patógenos de suelo que generan pudriciones (Hoyos et al. 2008). Observaciones similares fueron hechas por Nagaraj et al. (2012) quienes encontraron niveles aceptables de control sobre Erwinia con Bacillus subtilis y Pseudomonas fluorescens.
Adicionalmente, se considera que las alternativas químicas podrían constituir herramientas valiosas en un programa integrado de manejo de la PSF. Dos alternativas químicas con alto potencial, cuyo efecto in vitro no ha sido estudiado en nuestro país, son el uso de compuestos cúpricos y desinfectantes a base de yodo. El cobre ha sido descrito como uno de los fungicidas y bactericidas más antiguos. El hidróxido cúprico, oxicloruro cúprico, sulfato cúprico y el óxido cuproso han sido registrados en el control de enfermedades causadas por hongos e infecciones bacterianas (Ordax 2008, Arauz 2011). En Costa Rica, para el control de Erwinia sp. en plantaciones de mango, Coto y Wang 1995 obtuvieron buen control de este patógeno a partir del Caldo bordelés (80% Sulfato de Cobre) en aplicaciones foliares. Los productos comerciales formulados con Iodo han sido utilizados para el control de pudriciones vasculares y marchitamiento en banano y plátano, por lo que tiene un alto potencial para el control de la PSF (Gómez et al. 2001).
El objetivo general de este trabajo fue determinar los microorganismos asociados a la enfermedad conocida como pudrición suave del fruto de banano (Musa sp.). Dos objetivos específicos fueron planteados, en primer lugar, describir los síntomas de la Pudrición Suave del Fruto (PSF) y adicionalmente, determinar alternativas de control microbiológicas y químicas a nivel in vitro.
Materiales y métodos
La investigación se realizó en el 2016, en Río Frío (Latitud 10º 20' N, Longitud 83º 57' O), del cantón de Sarapiquí. Las pruebas de laboratorio se realizaron en el Laboratorio de Aguas y Ensayos Biológicos de Standard Fruit Company, en esta misma localidad, y en los laboratorios de Fitopatología y Técnicas Moleculares Aplicadas a la Fitoprotección del Centro de Investigaciones en Protección de Cultivos (CIPROC), de la Universidad de Costa Rica, Montes de Oca. Las pruebas in vitro se realizaron en el laboratorio de Microbiología Agrícola del Centro de Investigaciones Agronómicas, de la Universidad de Costa Rica, Montes de Oca, y en el laboratorio de Aguas y Ensayos Biológicos de Standard Fruit Company de Costa Rica S.A. (Dole), Río Frío, Sarapiquí, Heredia.
Identificación de los microorganismos asociados a la PSF
Recolección de la muestra.Se recolectó una muestra de 15 frutos enfermos, con el síntoma típico de la enfermedad en planta empacadora. La muestra estaba compuesta de fruta que presentaba menos del 50% de tejido necrótico. Se descartaron frutos que presentaban ruptura de cáscara para reducir las posibilidades de contaminación por patógenos secundarios.
Procesamiento de la muestra Los frutos enfermos fueron lavados con agua desionizada estéril y desinfectados con alcohol al 70% durante un minuto y cloro al 1% durante un minuto. Luego, fueron enjuagados 3 veces con agua desionizada estéril para remover restos de cloro y alcohol. Con ayuda de un bisturí esterilizado, se realizó una incisión rectangular en la cáscara, en la zona de avance de la enfermedad, para exponer la pulpa del fruto. Posteriormente, se utilizaron aproximadamente 10 g de pulpa y se maceró en 90 ml de agua desionizada estéril, en una bolsa plástica. Este macerado se incubó durante 24 horas a 26±1°C y bajo condiciones de oscuridad.
Por medio de la técnica de diluciones seriadas, se diluyó el macerado hasta 108. Cada dilución se cultivó en platos Petri, con el medio MacConkey. Finalmente, los platos Petri fueron incubados durante 24 horas a 26±1°C y bajo condiciones de oscuridad. Transcurrido este tiempo, se observó el crecimiento microbiano en cada plato.
Clasificación y purificación del crecimiento microbiano. El crecimiento microbiano fue clasificado de acuerdo con la morfología de la colonia bacteriana, por color, forma, superficie y tipo de borde. Este procedimiento fue llevado a cabo en medio Agar Tripticasa de Soya (ATS). Cada morfotipo fue separado y purificado para efectuarle las pruebas de patogenicidad e identificación.
Pruebas de patogenicidad. Este procedimiento se llevó a cabo bajo condiciones controladas de laboratorio, con fruta sana de 11 semanas de edad, proveniente de plantaciones comerciales con baja incidencia de la enfermedad. Los frutos recolectados fueron lavados con agua desionizada estéril y desinfectados con alcohol al 70% durante un minuto y cloro al 1% durante un minuto. Luego, fueron enjuagados 3 veces con agua desionizada estéril para remover restos de cloro y alcohol. Posteriormente, con ayuda de un palillo de madera, previamente esterilizado, se tomó una porción de cada morfotipo bacteriano y se inoculó en la fruta sana introduciéndolo 1 cm. La zona de inoculación fue cubierta con papel Parafilm. En total, se inocularon 10 frutos por cada morfotipo. Diez frutos fueron utilizados como testigos e inoculados con agua desionizada estéril, mediante el mismo procedimiento.
Los frutos inoculados fueron colocados en cámara húmeda a temperatura ambiente. Se realizaron inspecciones, a las 24, 48 y 120 horas después de inoculación, para determinar la aparición de los síntomas característicos de la enfermedad. Posteriormente, para la identificación, se seleccionaron los morfotipos bacterianos que manifestaron los síntomas característicos de la enfermedad.
Identificación de agentes causales de la enfermedad. La identificación de los agentes causales se llevó a cabo a partir de los aislamientos que resultaron positivos en las pruebas de patogenicidad. A estos aislamientos se les realizaron pruebas bioquímicas como la prueba de crecimiento en medio Agar Papa Dextrosa (PDA), rayado en discos de papa, prueba catalasa, prueba oxidasa, prueba TSI y tinción de Gram. Posteriormente, se realizó la identificación de las bacterias según el sistema BIOLOG GEN III y la técnica molecular de secuenciación mediante la Reacción en Cadena de la polimerasa (PCR), a partir de la región 16S del ARN.
El procedimiento para llevar a cabo la identificación mediante PCR, se realizó directamente con muestras de las colonias en el plato de cultivo, en el Laboratorio de Técnicas Moleculares aplicadas a la Fito protección del CIPROC, de la Universidad de Costa Rica (UCR), como se describe a continuación.
Extracción de ácido desoxirribonucleico (ADN). La extracción de ADN se realizó a partir de colonias frescas de las bacterias del plato de cultivo, con el método CTAB (Murray y Thompson 1985). El ADN fue cuantificado mediante un espectrofotómetro Bio Photometer Plus 6132 (Eppendorf) y se llevó a una concentración final de 80 ng.ul-1.
Reacción en Cadena de la Polimerasa y secuenciación del ADN. La Reacción en Cadena de la Polimerasa (PCR) se realizó con los cebadores específicos para el gen ribosomal 16S: 27F (5'- AGAGTTTGATCMTGGCTCAG-3') y 1492R (5'-TACGGYTACCTTGTTACGACTT-3'), descritos por Lane et al. 1985, que amplifican la secuencia total del gen.
La reacción se llevó a cabo en un volumen final de 25 μl, que consistían en 15,25 μl de agua desionizada ultra pura, 2,5 μl de Buffer 10X (1X), 2,5 μl de dNTPs (1mM), 1,25 μl de cada cebador (0,5 μM) y 0,25 μl de DreamTaq DNA Polymerase (1U/μl) (Fermentas©). Se utilizó un control negativo que consistía en una reacción sin ADN. La reacción de amplificación se llevó a cabo a partir del siguiente perfil térmico: pre-desnaturalización inicial a 96°C durante 2 minutos, seguido por 35 ciclos de desnaturalización a 96°C durante 1 minuto, anillamiento a 56ºC por 1 minuto, extensión a 72°C por 2 minutos, seguidos de una extensión final a 72°C durante 10 minutos.
El producto de PCR, de aproximadamente 1500 pares de bases (pb), se confirmó mediante electroforesis en gel de agarosa (0,8%), comparándolo con un marcador de peso molecular de 100 pb, Gene Ruler de Fermentas. El producto de PCR se digirió con una endonucleasa llamada Exonuclease I (Fermentas). La secuenciación se realizó al producto purificado de PCR a una concentración de 50 ng.μl-1 por la empresa Macrogen Inc; Corea. Se obtuvo secuencias en ambas direcciones para cada muestra generada a partir de ciclos fluorescentes, con un secuenciador modelo 3730XL (Applied Biosystems).
Alineamiento de las secuencias y análisis filogenéticos. La calidad de las secuencias se confirmó con un alineamiento bidireccional y por comparación con los cromatogramas con el programa Bio Edit (Hall 1999), se cortó las terminaciones 5' y 3' de las cadenas para facilitar el alineamiento. Además, se utilizó la herramienta informática Basic Local Alignment Search Tool (Blast) del National Center for Biotechnology Information (NCBI), por sus siglas en inglés, a partir del cual se comparó la secuencia generada frente a las secuencias de la base de datos del banco de genes (Gene Bank).
Descripción de síntomas de la PSF. Se realizaron inspecciones en planta empacadora en racimos en edad de cosecha (11 y 12 semanas) para determinar la presencia de frutos que presentaran diferentes estados de desarrollo de la enfermedad. Posteriormente, estos frutos fueron observados minuciosamente en el laboratorio para determinar las similitudes entre ellos, así como la sintomatología característica de la enfermedad. En campo, racimos de diferentes edades fueron inspeccionadas para detectar posible desarrollo de frutos enfermos en edades tempranas.
Evaluación in vitro de 13 formulaciones comerciales de microorganismos antagonistas sobre Erwinia chrysanthemi (sin. Dickeya chrysanthemi), agente asociado a la PSF. Se utilizó la metodología de doble enfrentamiento (Chérif y Benhamou 1990). Cada unidad experimental constó de un plato Petri, con 4 discos de papel filtro, 2 impregnados con el tratamiento y 2 con los controles, el positivo con agua destilada y el negativo con un antibiótico (Gentamicina 1,2 ppm). En total 13 tratamientos y 10 repeticiones por tratamiento. Los tratamientos fueron seleccionados según el posible potencial antagonista de los microorganismos incluidos en la formulación de los productos ofrecidos en el mercado y de acuerdo con la revisión de literatura (Tabla 1).
Tabla 1 Caracterización microbiológica de las formulaciones comerciales de cepas puras y mezclas de microorganismos evaluados en las pruebas de antagonismo con Erwinia sp. La dosis corresponde a la recomendación del fabricante para uso en campo. UFC.ml-1, Unidades formadoras de colonias por mililitro de producto comercial. *Información no disponible debido a que el producto está registrado para uso diferente. **Información confidencial del fabricante.
| Tratamiento | Composición (según etiqueta) | Empresa suplidora | UFC.ml-1 | Dosis (según etiqueta) | |
| T1 | Serenade® | Bacillus subtilis (cepa QST 713) | Bayer | 1,0 x 1011 | 1 L.ha-1 |
| T2 | Sonata ® | Bacillus pumilus (cepa QST 2808) | Bayer | 1,0 x 109 | 1 L.ha-1 |
| T3 | BSLIN® | Bacillus subtilis (cepa mog04) | Laboratorio Dr. Obregón | 1,0 x 109 | 14,8 L.ha-1 |
| T4 | Actinel® | Streptomyces griseoviridis | Laboratorio Dr. Obregón | 1,0 x 1010 | 16 L.ha-1 |
| T5 | Biota Max | Trichoderma (T. viridae, T. koningii, T. harzianum, T. polysporum), Bacillus (B. subtilis, B. laterosporus, B. licheniformis, B. megaterium, B. pumilus), Paenibacillus polymyxa | Tecnobac S.A. | Trichoderma 2,5 x 109 Bacillus 2,5 x 109 P. polymyxa 5 x 109 | 57 g.ha-1 |
| T6 | Environoc 401 | Trichoderma sp; Saccharomyces sp; Bacillus sp; Pseudomonas sp; Lactobacillus sp; Yarrowia sp; Rhodopseudomonas sp; Cellulomonas sp. | Biodyne Costa Rica | 1 x 108 | 1,6 L.ha-1 |
| T7 | Magic Green | Streptomyces sp; Azospirillum sp; Bacillus subtilis, Lactobacillus sp; Nitrosomonas multiformis, Streptococcus sp; Aspergillus penicilloides, Mucor sp; Trichoderma spp. | Granja Avícola Santa Marta | -* | 30 L.ha-1 |
| T8 | Bactericida Horizon | Penicillium sp. | Horizon Bioagro | 2,5 x 1012 | 2 L.ha-1 |
| T9 | Ultrazyme | Lactobacillus sp. | Cypher | 3,6 x 107 | 3 kg.ha-1 |
| T10 | Terrabiosa | Bacterias varias especies | Agrícola Piscis | 5 x 109 | 50 L.ha-1 |
| T11 | Ferbiol | Bacterias lácticas Levaduras Actinomicetos | Agrícola Piscis | 9,5 x 106 6,1 x 106 2,0 x 106 | 10 L.ha-1 |
| T12 | Fruit wash | Microorganismos benéficos | Biowish | -* | 2 kg.ha-1 |
| T13 | Environoc 501 | Bacillus sp; Candida ssp; Lactobacilus sp; Pseudomonas sp.; Sacchromyces sp; Streptomyces sp. | Biodyne Costa Rica | -** | 1,6 L.ha-1 |
Los productos comerciales formulados a base de microorganismos se enfrentaron a Erwinia chrysanthemi (sin. Dickeya chrysanthemi). Se emplearon 10 repeticiones por tratamiento. El enfrentamiento se llevó a cabo en platos Petri en medio de cultivo Agar Nutritivo (AN) para 10 productos y Agar Tripticasa de Soya (ATS) para los 2 restantes. En cada plato se rayó y distribuyó, en 4 direcciones, con hisopos estériles, una suspensión igual al estándar Mc Farland #0,5, que equivale a 1,5x108 UFC.ml-1 de E. chrysanthemi. Posteriormente, se preparó un volumen de 0,1 L de la dosis proporcionada en la etiqueta del tratamiento, del cual se tomó una alícuota de 7 (L y se colocó en los discos de papel filtro. Los platos Petri se colocaron en condiciones de oscuridad, en una incubadora (Shelton Sm 16) a 26±1°C.
Se midió el diámetro menor y mayor del anillo de inhibición de cada tratamiento, a las 24, 48 y 120 horas. El análisis de los datos se realizó mediante un análisis de variancia (ANDEVA) con una prueba LSD Fisher y una probabilidad del 5%, con el paquete estadístico InfoStat.
Evaluación in vitro de formulaciones de Iodo y cobre sobre Erwinia chrysanthemi (sin. Dickeya chrysanthemi). Se utilizó la metodología de doble enfrentamiento (Chérif y Benhamou 1990). Cada unidad experimental constó de un plato Petri, con 4 discos de papel filtro, 2 impregnados con el tratamiento y 2 con los controles, el positivo con agua destilada y el negativo con un antibiótico (Gentamicina 1,2 ppm). En total quince tratamientos y 10 repeticiones por tratamiento. Los tratamientos consistieron en formulaciones comerciales de cobre y yodo ofrecidas en el mercado (Tabla 2).
Tabla 2 Formulaciones comerciales de cobre y yodo evaluadas en las pruebas de antagonismo con Erwinia sp. La dosis corresponde a la recomendación del fabricante para uso en campo.
| Tratamiento | Descripción/dosis | Concentración | Dosis L.Ha-1 | |
| T1 | Copper speed 100% | CuSO4 | 6% P/v | 0,4 |
| T2 | Copper speed 50% | CuSO4 | 6% P/v | 0,2 |
| T3 | Copper speed 25% | CuSO4 | 6% P/v | 0,1 |
| T4 | Fulmicobre 100% | Cu3(PO3)2 | 5% p/v | 1 |
| T5 | Fulmicobre 50% | Cu3(PO3)3 | 5% p/v | 0,5 |
| T6 | Fulmicobre 25% | Cu3(PO3)4 | 5% p/v | 0,25 |
| T7 | Foliveex cobre 100% | CuSO4 | 98% p/p | 10 |
| T8 | Foliveex cobre 50% | CuSO4 | 98% p/p | 5 |
| T9 | Foliveex cobre 25% | CuSO4 | 98% p/p | 2,5 |
| T10 | Nutricop 20 100% | CuSO4 | 28,8% p/v | 4 |
| T11 | Nutricop 20 50% | CuSO4 | 28,8% p/v | 2 |
| T12 | Nutricop 20 25% | CuSO4 | 28,8% p/v | 1 |
| T13 | Vanodine 5 ml.L-1 | Iodo-Etanol | 2,5% | 0,125 |
| T14 | Vanodine 10 ml.L-1 | Iodo-Etanol | 2,5% | 0,25 |
| T15 | Vanodine 30 ml.L-1 | Iodo-Etanol | 2,5% | 0,75 |
Los productos comerciales formulados a base de yodo y cobre se enfrentaron a E. chrysanthemi. Se emplearon 10 repeticiones por tratamiento. El enfrentamiento se llevó a cabo en platos Petri en medio de cultivo Agar Nutritivo (AN) para 10 productos. En cada plato se rayó y distribuyó, en 4 direcciones, con hisopos estériles, una suspensión igual al estándar Mc Farland # 0,5, que equivale a 1,5x108 UFC.ml-1 de E. chrysanthemi. Posteriormente, se preparó un volumen de 0,1 L de la dosis proporcionada en la etiqueta de cada tratamiento, del cual se tomó una alícuota de 7 (L y se colocó en los discos de papel filtro. Los platos Petri se colocaron en condiciones de oscuridad, en una incubadora (Shelton Sm 16) a 26±1°C.
Se midió el diámetro menor y mayor del anillo de inhibición de cada tratamiento, a las 24, 48 y 120 horas. El análisis de los datos se realizó mediante un análisis de variancia (ANDEVA) con una prueba LSD Fisher y una probabilidad del 5%, con el programa estadístico InfoStat.
Resultados y Discusión
Clasificación y purificación del crecimiento microbiano. De la etapa de aislamiento de la sintomatología característica de la PSF se obtuvo como resultado 7 morfotipos bacterianos. De estos, 3 morfotipos presentaron forma irregular, bordes ondulados, superficie plana y coloración parda o café claro, en medio MacConkey, característicos de enterobacterias como Erwina, concordante con las observaciones de Guzmán y Wang (1998) en la identificación morfológica de Erwinia sp. Los 3 morfotipos fueron inoculados en fruta para probar su patogenicidad.
Identificación de los agentes asociados a la PSF. Los resultados obtenidos en las pruebas bioquímicas realizadas concuerdan con lo encontrado por varios autores para el género Erwinia (Tabla 3). Los 3 morfotipos tuvieron un resultado positivo en las pruebas de crecimiento en medio agar papa dextrosa (PDA), en agar nutritivo (AN), y en discos de papa. Estas pruebas son positivas para los géneros de bacterias pectinolíticas, osea que tienen la capacidad de producir enzimas degradadoras de la pectina, como Erwinia chrysanthemi y Erwinia carotovora, que se traduce en la degradación de tejidos suculentos en la planta (Cedeño et al. 1990,Soriano et al. 2000, Ramírez et al. 2014). Se ha documentado que estas pruebas son claves para determinar la patogenicidad de Erwinia chrysanthemi (Beaulieu et al. 1993), y al respecto, Guzmán y Wang (1998), a partir de bacterias del género Erwinia, obtuvieron resultados positivos para estas pruebas.
Tabla 3 Caracterización bioquímica de los aislamientos SFC2, SFC4 y SFC7, obtenidos del síntoma de la Pudrición Suave del Fruto (PSF).
| Prueba | Resultado |
| Catalasa | + |
| Oxidasa | - |
| Rayado en discos de papa | + desnaturaliza el tejido |
| TSI | + A/A |
| Tinción Gram | - |
| Crecimiento en PDA | + |
| Crecimiento en AN | + |
Para los 3 morfotipos, la tinción Gram fue Gram negativa, catalasa positiva, oxidasa negativa, y TSI positiva para la fermentación de azúcares. Como señala la literatura, la gran mayoría de bacterias fitopatógenas son Gram negativas (Kunstmann et al. 2006, Ramírez et al. 2014), por otra parte, en su trabajo, Ramírez et al. 2009, señalan en la caracterización bioquímica de bacterias del género Erwinia, que estas son catalasa positiva y oxidasa negativa, además, describen la capacidad de este género para fermentar azúcares, lo que resulta en el viraje del color del medio de rojo a amarillo, en la prueba TSI.
Los morfotipos fueron analizados mediante la técnica bioquímica BIOLOG GEN III y la técnica molecular de secuenciación mediante PCR. El resultado de ambas pruebas refuerza que los morfotipos SFC2, SFC4 y SFC7 corresponden a Erwinia chrysanthemi (sin. Dickeya chrysanthemi) y Erwinia carotovora (sin. Pectobacterium carotovorum) (Tabla 4).
Tabla 4 Identificación de los aislamientos SFC2, SFC4 y SFC7 mediante el sistema BIOLOG GEN III y secuenciación mediante reacción en cadena de la polimerasa (PCR), de acuerdo con la amplificación del ARN de la región 16S.
| Aislamiento | BIOLOG GEN III | Secuenciación mediante PCR |
| SFC2 | Erwinia carotovora (Pectobacterium carotovorum) | 99% similitud con Erwinia chrysanthemi |
| SFC4 | Erwinia carotovora (Pectobacterium carotovorum) | 99% similitud con Erwinia chrysanthemi y Dickeya dadantii |
| SFC7 | Erwinia sp | 99% similitud con Erwinia chrysanthemi |
Con estos resultados se puede afirmar que los agentes asociados a la PSF son Erwinia chrysanthemi (sin. Dickeya chrysanthemi y Dickeya dadantii) y Erwinia carotovora (sin. Pectobacterium carotovorum). Estos resultados concuerdan con los agentes causales de las pudriciones blandas descritos recientemente en la literatura (Guzmán et al. 2017 , Villalta et al. 2019), que señalan a Erwinia chrysanthemi (sin. Dickeya dadantii), como el agente causal de pudriciones blandas en banano. El hallazgo de Erwinia carotovora (sin. Pectobacterium carotovorum) podría sugerir la participación conjunta de este organismo, ya que siempre fue aislada de los síntomas de la enfermedad y se logró comprobar, mediante los postulados de Koch, su patogenicidad.
Descripción de los síntomas característicos de la PSF. Los síntomas de esta enfermedad se observaron en fruta verde, a partir de 6 semanas de edad y se acentuaron cuando la fruta alcanzó edad comercial alrededor de 11 semanas. Los síntomas característicos fueron manchas acuosas debajo de la epidermis del fruto, que desencadenaron áreas necrosadas a lo largo del fruto. Los síntomas iniciaron por lo general en el extremo distal, que abarcó aproximadamente 0,5 cm de radio. La enfermedad avanza paulatinamente hasta llegar al pedúnculo. Internamente, en un estado avanzado, los tejidos de la pulpa se degradan, producto de la acción enzimática de los agentes causales y presentan mal olor, que da origen al síntoma típico de una pudrición blanda (Jeger et al. 1995, Guzmán y Wang 1998, Guzman et al. 2017) (Figura 1).
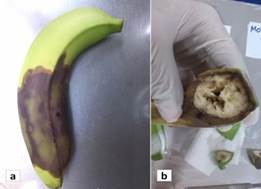
a. Necrosis externa en los tejidos de la cáscara del fruto.
b. Aspecto de los tejidos internos de la pulpa de un fruto afectado por la enfermedad.
Figura 1 Síntomas de los tejidos internos de la pulpa de un fruto afectado por la enfermedad.
La enfermedad progresa rápidamente; al término de 24 horas, la necrosis externa es evidente e internamente, la pudrición puede alcanzar entre 1 y 2 tercios del fruto (Guzmán y Wang 1998). En etapas avanzadas, los tejidos de la cáscara colapsan, producto de la pudrición interna y externa, seguido de un goteo de exudados hacia la fruta de manos inferiores y adyacentes que causa manchas, estrías y decoloraciones que convierten fruta en condiciones óptimas para ser comercializada en fruta de desecho (Figura 2).

a. Fruto integro con necrosis característica
b. Fruto colapsado en la parte superior del racimo que genera goteo de exudados sobre fruta de manos inferiores y adyacentes.
Figura 2 Síntomas característicos de la PSF en racimos de 12 semanas de edad
Pruebas de patogenicidad. Los 3 morfotipos probados, fueron denominados SFC2, SFC4 y SFC7, y reprodujeron los síntomas característicos de la PSF. Los síntomas iniciales de la enfermedad, pequeñas áreas de apariencia húmeda en la cáscara fueron observados 24 horas después de la inoculación y se extendieron hasta alcanzar la totalidad del fruto, aproximadamente 120 horas después. Guzmán y Wang (1998), en su trabajo con Erwinia sp, señalan que al cabo de 5 días de inoculación (120 h), se alcanzó un 90% del fruto necrosado, dato que refuerza la rapidez con que estos patógenos afectan el fruto.
En este trabajo también se pudo constatar lo expuesto por Guzmán y Wang 1998 y Guzmán et al. 2017, quienes señalaron que una vez observado el síntoma externo en la cascara del fruto, los tejidos internos de la pulpa se encontraron degradados y con apariencia acuosa (Figura 3).
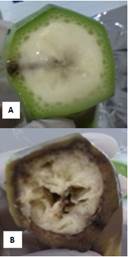
Figura 3 A. Aspecto de la pulpa de un fruto sano. B. Aspecto de la pulpa de un fruto afectado por la enfermedad.
Efecto antagonista in vitro de trece formulaciones comerciales de microorganismos antagonistas sobre Erwinia chrysanthemi (sin. Dickeya chrysanthemi). El diámetro de inhibición sobre Erwinia chrysanthemi (sin. Dickeya chrysanthemi) se observó a partir de 48 horas después de la inoculación. Como se indica en la Figura 4, el mayor diámetro de inhibición del crecimiento de la bacteria fue obtenido con Bacillus subtilis (cepa QST 713) y Bacillus pumilus (cepa QST 2808), a las 120 horas. Ambos productos lograron aproximadamente el doble del diámetro de inhibición del resto de tratamientos. Con el testigo positivo (agua destilada) y negativo (Gentamicina 1,2 ppm), el diámetro de inhibición alcanzado fue 0 cm y 2,5 cm respectivamente.
El efecto de ambos tratamientos puede deberse a que las cepas de las bacterias, B. subtillis y B. pumilus, han sido seleccionadas por su capacidad de antagonismo con patógenos de plantas causantes de múltiples enfermedades. La literatura indica que entre un 4 y 5% del genoma de ambas especies está dedicado a la producción de antibióticos. Tienen el potencial para producir más de 2 docenas de moléculas antimicrobianas diferentes, además de las enzimas líticas, celulasas, proteasas, 1,4-β-glucanasas e hidrolasas, las cuales contribuyen a la degradación de las paredes y membranas de las células del patógeno (Baysal et al. 2013).
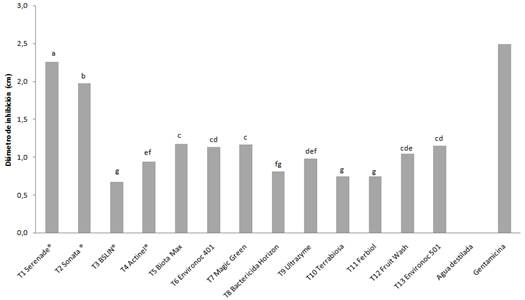
Figura 4 Inhibición del crecimiento in vitro de Erwinia chrysanthemi (sin. Dickeya chrysanthemi) debido al efecto antagonista de los tratamientos a las 120 horas. Tratamientos seguidos de una misma letra no son significativamente diferentes (LSD Fisher 0,05).
Observaciones realizadas por Sharga y Lyon (1998), Reinoso et al. (2006), Nissen et al. (2008), Goorani El y Hassanein (2008) y Matar et al. (2009), indican la efectividad de ambas bacterias en la inhibición del crecimiento in vitro de especies de Erwinia. Por otra parte, en otros cultivos, se observó efecto inhibitorio por parte de estas bacterias al probarse en el control in vitro de 2 subespecies de Erwinia carotovora subsp. atroseptica (Pectobacterium carotovorum) y Erwinia carotovora subsp. carotovora (Pectobacterium carotovorum), causantes de la pudrición suave de la papa (Cladera et al. 2006). Por otra parte, Rashid et al. 2013, lograron un diámetro de inhibición de aproximadamente 2 cm con Bacillus subtillis en pruebas de control biológico in vitro contra Erwinia sp.
Se ha observado que los compuestos producidos por Bacillus mantienen su actividad en medios de cultivo hasta 8 horas después de producidos, y su actividad in vitro aumenta luego de 24 horas de la inoculación del microorganismo, cuando este ha logrado establecerse en el medio (Bottone y Peluso 2003). Lo anterior puede explicar que el efecto inhibitorio de los 2 tratamientos comenzó a observarse después de las 24 horas de inoculación y el máximo se alcanzó a las 120 horas después, al terminar la fase de crecimiento exponencial e iniciar la fase estacionaria de estos microorganismos (Bottone y Peluso 2003).
Efecto de inhibición in vitro de fuentes comerciales de Iodo y cobre sobre Erwinia chrysanthemi (sin. Dickeya chrysanthemi). El crecimiento de E. chrysanthemi (sin. Dickeya chrysanthemi) se vio inhibido por las formulaciones de cobre y yodo. Los tratamientos que mostraron mayor efectividad fueron la dosis completa de Sulfato de Cobre 28%, media dosis de Sulfato de cobre 28% y la dosis más alta de Iodo etanol 30 ml.L-1 (Figura 5). Cabe resaltar que la dosis más alta de Iodo etanol tuvo un desempeño similar a las mejores fuentes de cobre. Los resultados obtenidos pueden deberse a que el Sulfato de Cobre (28% P/V) presenta un contenido porcentual de cobre mayor a los demás tratamientos evaluados. Por otra parte, el Sulfato de Cobre (98% P/V) no mostró un desempeño adecuado. A raíz de estos resultados, es necesario investigar la influencia de la concentración y naturaleza sólida o líquida de las fuentes de cobre en la inhibición sobre E. chrysanthemi (sin. Dickeya chrysanthemi).
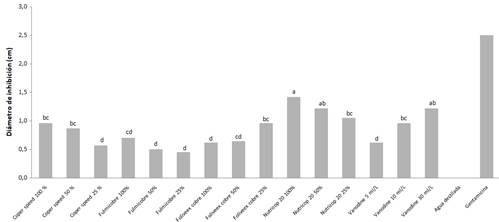
Figura 5 Inhibición del crecimiento in vitro de Erwinia chrysanthemi (sin. Dickeya chrysanthemi) debido al efecto de los tratamientos a las 48 horas. Tratamientos seguidos de una misma letra no son significativamente diferentes (LSD Fisher 0,05).
El efecto observado se debe al efecto bacteriostático y bactericida descrito por la literatura para el Iodo y el cobre (Gómez et al. 2001, Ordax 2008, Arauz 2011), sin embargo, es importante determinar su uso potencial y la posible fitotoxicidad en fruta causada por estas fuentes de cobre y Iodo.
Conclusiones y Recomendaciones
El agente asociado a la enfermedad PSF fue aislado de tejido enfermo e identificado como Erwinia chrysanthemi (sin. Dickeya chrysanthemi).
Se presume que hay una participación conjunta de Erwinia carotovora (sin. Pectobacterium carotovorum), ya que siempre fue aislada de los síntomas de la enfermedad y se logró comprobar, mediante los postulados de Koch, su patogenicidad.
El mejor efecto antagonista in vitro sobre Erwinia chrysanthemi (sin. Dickeya chrysanthemi) se obtuvo con los microorganismos Bacillus pumilus cepa QST 2808 y Bacillus subtilis cepa QST 713.
Por parte de las fuentes químicas, el mejor efecto in vitro sobre Erwinia chrysanthemi (sin. Dickeya chrysanthemi) se obtuvo con la dosis completa y media dosis de Sulfato de Cobre al 28,8%, y la dosis más alta de Iodo-Etanol al 2,5%.
Se recomienda investigar el antagonismo in vitro, a partir del incremento de formulaciones comerciales de microorganismos antagonistas y controladores biológicos, para dar énfasis a productos elaborados a partir de cepas puras.
Se recomienda investigar la influencia de más fuentes a base de cobre y yodo, de diferente concentración, de naturaleza solida o líquida sobre la inhibición de Erwinia chrysanthemi (sin. Dickeya chrysanthemi).















