Introducción
El plátano es el cuarto cultivo más importante del mundo después del arroz, el trigo y el maíz. Esta fruta constituye la base de la alimentación de muchas regiones tropicales y además representa una importante fuente de ingresos para las empresas productoras (Rodríguezet al.2018).
Aproximadamente, el 70% de la producción de plátano en Venezuela se concentra en la Zona Sur del Lago de Maracaibo, Venezuela, específicamente en los estados Zulia, Trujillo, Mérida y Táchira (Rodríguezet al.2012). El estado Zulia, por su parte, ocupa el mayor número de tierras sembradas con el cv Hartón y las más grandes unidades de producción, especialmente aquellas situadas entre los ríos Escalante, Mucujepe y en las riberas del río Chama (Gonz á lezet al.2021).
La información generada sobre la morfología de la cepa del plátano Hartón y el ciclo de las plantas está relacionada con la producción. La longitud del pseudotallo y su circunferencia están en relación directa, en primer término, con el tipo de clon y luego con el vigor de la planta producto de su estado de crecimiento. De igual modo, es un cultivar de cocción, a diferencia de los clones de banano del subgrupo Cavendish, los cuales se consumen frescos (Rodríguezet al.2018).
El número de manos por racimo, circunferencia del pseudotallo y altura del hijo de sucesión son parámetros que están altamente correlacionados con la producción o vigor de la plantación en banano o plátano (Rosaleset al.2008).
Para la búsqueda de mejoras en la productividad del cultivo y la selección de zonas realmente aptas para el óptimo desarrollo de plantas de plátano y banano, es necesario realizar estudios que contemplen la caracterización pertinente del suelo, en cuanto a propiedades o atributos del mismo, pero no tendría ningún sentido observar esto aisladamente sin que interactúe en el sistema la variable planta y su relación con el suelo (Olivareset al.2020).
La textura, resistencia a la penetración, densidad aparente e infiltración son características físicas que determinan la rigidez y la fuerza de sostenimiento, la facilidad para la penetración de las raíces, la aireación, la capacidad de drenaje y de almacenamiento de agua, la plasticidad, y la retención de nutrientes (Rodríguez y Lobo 2004, Rodríguez 2009), por lo que se considera necesario conocer dichas características físicas del suelo, para conocer en qué medida y cómo afectan en el crecimiento y desarrollo de las plantas, para mantener las mejores condiciones físicas del suelo posibles (Castañedaet al.2014). Algunas propiedades químicas como pH, conductividad eléctrica, fracciones de carbono y disponibilidad de nutrientes han sido señalados como indicadores de calidad de suelo que condicionan la expresión del desarrollo y productividad de cultivos (Martinezet al.2010, Martínezet al.2013), incluídas las musáceas (Olivareset al.2020). Complementariamente, el contenido de materia orgánica, es otro factor elemental que favorece diversas propiedades del suelo y los procesos de mineralización de nutrientes para el sustento de las plantas (Monsalveet al.2017).
Por su parte, las características biológicas forman parte de las actividades bioquímicas que se presentan en la fase sólida del suelo, por lo que son las interfaces sólido-líquido y líquido-gas los sitios de preferencia de los microorganismos. Esas características en conjunto contribuyen al diagnóstico previo de la degradación de suelos, por lo que propone que el análisis de estas, permitiría la aplicación de labores hortícolas y prácticas culturales que aumenten la sustentabilidad del recurso suelo. De la misma forma, la actividad microbiológica y la biomasa microbiana representan indicadores biológicos del suelo importantes de tener en cuenta en los sistemas productivos de cultivos (Paolini 2017).
La zona de estudio carece de investigaciones que relacionen el vigor de plantas de plátano y características del suelo, adicionalmente, existen algunas limitantes edáficas en esta región que pueden afectar el desarrollo y productividad del cultivo de plátano. Por lo tanto, se planteó como objetivo central de este estudio determinar algunas propiedades físicas, químicas y biológicas del suelo y su relación con la expresión del vigor del cultivo de plátano en fincas del Sur del Lago de Maracaibo, de la parroquia el Moralito, municipio Colón, estado Zulia, Venezuela.
Materiales y métodos
Área de estudio. La investigación se llevó a cabo en diferentes unidades de producción ubicadas entre el km 35 y el km 41 de los sectores: El Uvito, Bancada de Limones, Caño Negro y Cuatro Bocas de la parroquia el Moralito, municipio Colón del estado Zulia, Venezuela. Esta zona se encuentra a una altitud de 8 msnm y cuenta con una precipitación acumulada anual que varía de 1200 a 1500 mm, una temperatura promedio al año de 38°C y una humedad relativa máxima de 90% y media de 85%. Los suelos están clasificados como: Typic tropopsamments mixto e isohipertémico de la serie Bancham y Fluventic Eutropepts mixto e isohipertémico de la serie chama con inclusiones de la serie chamita (González 2018).
Definición de los sitios de muestreo. Se seleccionaron 7 unidades de producción de plátano, de las cuales 6 tenían una superficie de menos de 10 ha y una entre 12 y 15 ha. De acuerdo con la metodología propuesta por Rosaleset al.(2008) y Delgadoet al.(2010), en las 6 unidades de producción con menos de 10 ha se procedió a delimitar una parcela de 20 m x 50 m (1000 m2) por cada lote de vigor; mientras que en la unidad de producción entre 12 y 15 ha se procedió a demarcar 2 parcelas con la misma superficie por cada lote vigor.
Criterios para seleccionar lotes de alto y bajo vigor. La selección de lotes con plantas de alto y bajo vigor se realizó al tomar el criterio indicado por Rodríguez y Rodríguez (1998), quienes señalan que valores de circunferencia del pseudotallo de la planta madre, por encima de 76,36 cm en promedio y 7 manos por racimo, pueden ser consideradas como el biotipo ideal de planta madre con elevada productividad para el caso del clon Hartón en Venezuela y complementariamente, que dichas plantas tuvieran 16 hojas activas por hijo de sucesión y una media de 5,48 hojas con ancho de lámina foliar mayor de 10 cm. Para identificarlo se realizó una fase previa de diagnóstico en campo por medio de un pre-muestreo sistemático en cada finca evaluada en los lotes de alto y bajo vigor (AV y BV, respectivamente), de acuerdo con los criterios señalados por Rosaleset al.(2008) y Gonzálezet al.(2021).
Determinación del vigor de las plantas. En cada parcela de 1000 m2se seleccionaron 20 plantas con racimos próximos a ser cosechados (3 semanas antes del momento de cosecha) que fueron marcados con cintas, a las cuales se les determinó los siguientes parámetros de vigor: número de manos por racimo, circunferencia del pseudotallo de la planta madre y altura del hijo de sucesión, parámetros que están altamente correlacionados con la producción o vigor de la plantación (Rosaleset al.2008, Delgadoet al.2010, Loboet al.2011). La circunferencia de la planta madre se evaluó desde la base del suelo hasta los 100 cm de altura con una cinta métrica. La altura del hijo de sucesión se determinó al medir desde el nivel del suelo hasta la inserción del pecíolo de la última hoja expandida con la hoja candela. Luego de desarrollado el racimo, se procedió a contar todas las manos presentes en el mismo.
Toma de muestras de suelos. En cada parcela de 1000 m2ubicadas en los lotes de alto y bajo vigor se seleccionaron 3 puntos de muestreo al azar y en cada uno de ellos se abrieron minicalicatas de 60 cm ancho por 60 cm largo y 60 cm profundidad. Estas se ubicaron en la banda de fertilización de las plantas de plátano recién florecidas. En cada minicalicata se realizó una descripción del perfil del suelo y se separaron los horizontes genéticos, cuyo espesor dependió de las características intrínsecas de cada suelo y de cómo han actuado los factores y los procesos de formación de suelos.
En cada horizonte, se procedió a tomar las muestras de suelo para la determinación de las características físicas, químicas y biológicas del suelo en cada lote identificado. Para lograr una mejor representatividad del muestreo, se realizó un patrón de 10 submuestras por cada muestra de suelo colectadas del área adyacente al punto central de muestreo (minicalicata), las cuales se tomaron en tres profundidades (0-5; 5-15; 15-30). Las muestras fueron debidamente identificadas y transportadas a los laboratorios de Suelos de la Universidad Nacional Experimental Sur del Lago y Microbiología y Fitopatología de la Universidad Centroccidental Lisandro Alvarado para sus respectivas determinaciones.
Propiedades físicas del suelo
Textura.Se determinó mediante el método del hidrómetro de Gee y Bauder (1986).
Humedad.Se aplicó la siguiente ecuación:
% humedad = (Peso de suelo húmedo - Peso de suelo seco) / Peso de suelo seco * 100.
Densidad aparente.Se determinó con la metodología propuesta por Blake y Hartge (1986). En los 3 primeros horizontes genéticos del suelo, se tomaron muestras con el uso de los cilindros de Kopecky de 5,08 cm de diámetro por 5 cm de altura, los cuales fueron introducidos en el suelo con la ayuda de un martillo de goma. Una vez tomadas las muestras sin perturbar, se taparon con papel aluminio y se trasladaron al laboratorio, donde se pesaron y se secaron en una estufa a 105°C por 24 horas, se dejaron enfriar y se volvieron a pesar. Se determinó la relación del peso y volumen del cilindro de suelo.
Conductividad hidráulica saturada.Se determinó al utilizar valores de arena y arcilla de la muestra de suelo, mediante el empleo del programa Piras para evaluar las características hidráulicas de una muestra de suelo (Orellana 2016).
Resistencia a la penetración.Se evaluó en 3 vértices de cada minicalicata a traves del uso de un penetrómetro de profundidad por impacto (Nacci y Pla 1992).
Determinación de infiltración básica e instantánea.Se determinó, de acuerdo con el método del doble anillo propuesto por Reynoldset al.(2002), al frente del hijo de sucesión de la planta madre.
Propiedades químicas del suelo
pH.La acidez activa se determinó en extracto acuoso con una relación suelo-agua de 1:2,5, en agitación durante 2 horas (McLean 1982), mediante el uso de un medidor de pH marca Digital pH meter, modelo pH-2006.
Conductividad eléctrica.Se determinó en el mismo extracto utilizado para determinar la acidez activa, con un conductímetro marca HANNA, modelo HI 9033, calibrado previamente con una solución de KCL 0,040 mol.L-1a una temperatura de 25°C.
Contenido de materia orgánica.Se realizó al seguir el método de digestión húmeda propuesta por Walkley-Black 1934, modificado por Sims y Haby (1971).
Nitrógeno total.Se siguió el método de Kjeldahl (Fleck y Munro 1965).
Nitrógeno amoniacal.Se determinó al siguir el método propuesto por Keeney y Nelson (1982).
Amonio disponible.Se realizó al seguir la metodología de Anderson e Ingram (1993).
Fósforo total.La extracción se realizó mediante el procedimiento de digestión con ácido sulfúrico (H2SO4) concentrado y oxidación con peróxido de hidrógeno (H2O2), al utilizar el método de Tiessen y Moir (1993).
Suma de cationes.Se realizó mediante el uso de la solución extractora Mehlich 3, para determinar K, Ca, Mg y Na, en un equipo de absorción atómica modelo perkin Elmer 3110.
Sodio soluble.Se determinó por el método de fotometría de llama, a través de la metodología propuesta por Pérez y Gilabert (1997).
Porcentaje de saturación de bases. Previo a la determinación de porcentaje de saturación de bases, se determinó la capacidad de intercambio catiónico efectiva (CICE), lo cual consistió en tomar los valores finales en cmol+.kg-1de las bases de la muestra analizada por espectrofotometría de absorción atómica más el aluminio e hidrógeno retenido en las cargas del suelo (Chávez 2015).
En este sentido, la proporción de la CICE que es ocupada por cationes básicos (Ca+2+ Mg+2+ K++ Na+) se tomó en consideración en la siguiente fórmula para determinar porcentaje de saturación de bases: %SB=Suma de bases intercambiables/CICE x 100.
Propiedades biológicas del suelo
Hongos, bacterias y actinomicetos en suelo.Se utilizó la técnica de los platos de dilución (Rosaleset al.2008).
Carbono microbiano y respiración basal del suelo.El carbono asociado con la biomasa microbiana del suelo se determinó mediante la técnica de fumigación-extracción, en la cual se provoca la muerte de la microbiota del suelo con cloroformo y se extrae con una solución de sulfato de potasio (K2SO4) 0,5 N (Rosaleset al.2008). Para la respiración microbiana o respiración basal del suelo, el análisis se realizó mediante la técnica de incubaciones estáticas, donde se analiza la concentración de CO2desprendido (producto de la actividad biológica y del contenido de carbono orgánico fácilmente mineralizable presente en el suelo). El CO2es capturado en una solución alcalina (NaOH 0,2 N) durante 10 días de incubación bajo condiciones ambientales óptimas (Alef y Nannipieri 1995, Rosaleset al.2008).
Diseño experimental
El diseño de muestreo fue sistemático dirigido, este se basa en el seguimiento de un patrón geométrico específico (recorrido en zig-zag con líneas de cada 15 m dentro del área de 1000 m2para determinación de puntos de muestreo en los lotes), donde las muestras son tomadas a intervalos regulares a lo largo de ese patrón. Obtenidos los resultados de campo y laboratorio, se procedió a realizar un análisis de varianza previo cumplimiento de los supuestos. Cuando el ANOVA fue significativo (p<0,05) se aplicó una prueba de comparación de medias de Tukey, a través del programa Statistix versión 8,0. Además, se realizó un análisis correlacional lineal de Pearson entre los parámetros de vigor de plantas de plátano y las características físicas, químicas y biológicas del suelo con la finalidad de determinar cómo las características pueden influir en el vigor de las plantas de plátano.
Con el fin de identificar las relaciones entre las variables edáficas medidas con los lotes de alto y bajo vigor, se realizó un análisis multivariado por componentes principales con el apoyo del programa Infostat.
Resultados y discusión
Parámetros de vigor de plantas de plátano
En la Tabla 1, se observa que las variables de vigor estudiadas: número de manos por racimo, la circunferencia de la planta madre (cm) y la altura del hijo de sucesión (m) presentaron diferencias significativas (p<0,05) con valores más altos en lotes de plantas de plátano de alto vigor (AV) respecto a los de bajo vigor (BV). Esto indica que las variables seleccionadas son adecuadas para separar lotes con vigor contrastantes. Resultados similares con estas variables en el cultivo de banano han demostrado que pueden distinguir lotes contrastantes en cuanto a vigor se refiere (Rodríguezet al.2010a), relacionado, además, con variables edáficas que determinan la productividad del suelo (Rodríguezet al.2010b, Loboet al.2011, Olivareset al.2020).
Tabla 1 Parámetros de vigor de plantas de plátano en fincas. Sur del Lago de Maracaibo, estado Zulia, Venezuela.
| Lotes de vigor de plantas | Número de manos por racimo | Circunferencia de la planta madre (cm) | Altura del hijo de sucesión (m) |
| Alto vigor | 7,50±0,97ª* | 66,86±8,29ª | 2,56±0,53ª |
| Bajo vigor | 4,96±0,89b | 59,44± 9,16b | 2,03±0,48b |
| Probabilidad | <0,00 | <0,00 | <0,00 |
*Valor promedio ± desviación estándar seguido por letras minúsculas diferentes entre las columnas indican diferencias significativas (p<0,05) según prueba Tukey entre lotes de vigor de plantas de plátano.
Los resultados obtenidos de las variables biométricas de vigor son similares a los presentados por González-Pedrazaet al.(2014) en una finca con características de suelos relativamente similares cultivada con plátano Hartón, ubicada en el municipio Francisco Javier Pulgar del estado Zulia, Venezuela. Los lotes de alto vigor presentaron mayor número de manos por racimo, circunferencia del pseudotallo de la planta madre y altura del hijo de sucesión, que los lotes de bajo vigor.
Los valores de circunferencia de la planta madre (cm) fueron relativamente altos, en comparación con los datos reportados por Delgadoet al.(2008) en un trabajo realizado en la región central del estado Barinas, Venezuela, bajo condiciones de suelo y clima muy similares a las de este estudio, en plantaciones de plátano (MusaAAB cv. subgrupo plátano Hartón) con densidades de siembra de 1111 plantas.ha-1, los cuales señalan valores de 55,9 cm. No obstante, Rodríguez y Rodríguez (1998) presentaron datos relacionados con la biometría de plátano cv. Hartón, en la planicie del río Chama, depresión del Lago de Maracaibo, Venezuela, y encontraron que el perímetro promedio del pseudotallo de la planta madre fue de 76,36 cm. Dichos valores son superiores a los encontrados en la presente investigación. Sin embargo, para el mismo clon evaluado Rodríguezet al.(2018), se reportan valores de adecuado vigor bajo condiciones de los Llanos Orientales de Colombia, similares a los encontrados en la presente investigación.
Vigor de plantas de plátano y su relación con las propiedades físicas, químicas y biológicas en los suelos evaluados
Los resultados para cada profundidad de suelo evaluada y lotes de vigor contrastantes para las propiedades físicas, químicas y biológicas se presentan en las Tablas 2, 3 y 4.
Tabla 2 Características físicas del suelo entre lotes de plantas de plátano con diferente vigor para cada horizonte genético en fincas. Sur del Lago de Maracaibo, Venezuela.
| - | - | - | - | Características físicas del suelo | - | - | - | - |
| Vigor de plantas | Horizonte | Arcilla (%) | Limo (%) | Arena (%) | Grupo textural | Densidad aparente (g.cm3) | Humedad (%) | Conductividad hidráulica saturada (K) (cm/h-1) |
| AV | 1 | *6,56±1,29a | 77,81±16,66ª | 15,62±16,94ª | FL | 1,27± 0,10ª | 21,48±8,41ª | 3,99±0,44a |
| BV | - | 4,38±2,22b | 68,13±22,15ª | 27,50±21,04ª | FL | 1,33±0,06a | 15,33±5,39ª | 3,87±0,45a |
| AV | 2 | 3,75±1,33ª | 81,25± 16,20ª | 15,00±15,64ª | L | 1,33±0,11ª | 20,52±9,13ª | 3,96±0,42a |
| BV | - | 5,00±2,67ª | 66,25± 28,72a | 28,75±27,03ª | FL | 1,34±0,13a | 15,52±7,96ª | 3,88±0,59a |
| AV | 3 | 4,06±2,65a | 73,56±20,59ª | 22,37±21,80ª | FL | 1,34±0,12a | 18,34±7,00a | 4,14±0,55a |
| BV | - | 5,00± 2,67a | 56,25±35,22a | 38,75±33,88a | FL | 1,30±0,11ª | 15,54±7,85ª | 4,23±1,00a |
*Valor promedio ± desviación estándar seguidos por letras minúsculas diferente entre las columnas indican diferencias significativas (p<0,05) según prueba Tukey entre lotes de plantas de plátano para cada horizonte de suelo. AV: alto vigor, BV: bajo vigor, FL: franco limoso y L: limoso.
Tabla 3 Características químicas del suelo entre lotes de plantas de plátano con diferente vigor para cada horizonte genético en fincas. Sur del Lago de Maracaibo, Venezuela.
| - | - | - | - | - | Características químicas del suelo | - | - | - | - | - |
| Vigor de plantas | Horizonte | pH | CE | MO | NT | Amonio (mg N/kg suelo) | PT | SC | CICE | %SB |
| AV | 1 | *5,56±0,88ª | 0,15±0,09ª | 8,60±4,40ª | 0,02±0,01a | 251,12± 160,64ª | 637,85±382,31a | 8,82±1,96a | 8,97±1,95a | 98,26±1,59a |
| BV | - | 5,87±1,07a | 0,09±0,06a | 10,54±5,25a | 0,02± 0,01ª | 208,28± 109,16ª | 791,64±417,47a | 9,76±3,27a | 9,99±3,32a | 97,36±2,85a |
| AV | 2 | 5,90±0,56ª | 0,08±0,09ª | 5,06±1,46ª | 0,02±0,009ª | 224,76±106,10ª | 670,12±305,37a | 8,19±2,30a | 8,30±2,27a | 98,45±1,03a |
| BV | - | 6,02±0,92a | 0,09±0,09ª | 4,97±2,07ª | 0,02± 0,01ª | 290,67±226,88ª | 686,20±303,25a | 8,25±2,43a | 8,41±2,40a | 97,83±1,95a |
| AV | 3 | 6,16±0,60ª | 0,07±0,11a | 4,23±2,19ª | 0,02±0,006ª | 147,31±123,95ª | 716,84±321,91a | 8,25±2,38a | 8,36±2,36a | 98,45±1,03a |
| BV | - | 6,13±0,72ª | 0,04±0,03a | 3,17±1,43ª | 0,02±0,008a | 180,27±143,36ª | 641,20±327,18a | 7,33±1,97a | 7,44±1,96a | 98,36±0,77a |
*Valor promedio ± desviación estándar seguido por letras minúsculas diferente entre las columnas indican diferencias significativas (p<0,05) según prueba Tukey entre lotes de plantas de plátano para cada horizonte de suelo. AV= alto vigor, BV= bajo vigor, CE= conductividad eléctrica (mS/cm), MO= materia orgánica (%), NT= nitrógeno total (%); PT= fósforo total (μgP.g-1suelo); SC= suma de cationes (cmol(+).kg-1); CICE= capacidad de intercambio catiónico efectiva (cmol(+).kg-1); %SB= porcentaje de saturación de bases.
Tabla 4 Características biológicas del suelo entre lotes de plantas de plátano con diferente vigor para el primer horizonte genético en fincas. Sur del Lago de Maracaibo, Venezuela.
| - | - | Características biológicas del suelo | - | - | - |
| Vigor de plantas | UFC Hongos | UFC Bacterias | UFC Actinomicetos | PTNS | PTNR |
| AV | *1,29±0,04a | 9,74±1,27a | 0,88±0,09a | 356,58±0,51ª | 38,37±0,28b |
| BV | 1,30±0,03a | 9,93±1,18a | 0,5±0,07b | 232,58±0,39ª | 72,87±0,37a |
*Valor promedio ± desviación estándar seguidos por letras minúsculas diferente entre las columnas indican diferencias significativas (p<0,05) según prueba Tukey entre lotes de vigor de plantas de plátano. UFC= unidades formadoras de colonia. PTNS= población total de nematodos en suelos. PTNR= población total de nematodos en raíces.
Con respecto a las relaciones lineales entre variables edáficas y los parámetros de vigor del suelo, en general, se encontraron correlaciones significativas bajas para las características físicas, químicas y biológicas en los suelos (Tablas 5, 6, 7, 8, 9). De esta manera, se observa una correlación significativa y negativa entre arena y el número de manos por racimo (NMR) y la altura del hijo de sucesión (AHS); densidad aparente respecto a NMR y circunferencia de la planta madre (CPM). Por lo tanto, a medida que aumentan los porcentajes de arena y la densidad aparente, disminuyen los parámetros de vigor evaluados (Tabla 5).
Tabla 5 Relación entre el vigor de plantas de plátano y propiedades físicas del suelo en fincas. Sur del Lago de Maracaibo, Venezuela.
| Vigor de plantas/propiedades físicas del suelo | Número de manos por racimo | Circunferencia planta madre | Altura hijo de sucesión |
| ARC | *0,02ns | 0,08ns | -0,02ns |
| LIM | 0,19** | 0,02ns | 0,13* |
| ARE | -0,20** | -0,03ns | -0,13* |
| HUM | 0,15* | 0,05ns | 0,03ns |
| DA | -0,13* | -0,14* | -0,01ns |
| K | 0,01ns | -0,02ns | -0,07ns |
| RES | 0,10ns | - 0,06ns | 0,04ns |
| IB | -0,40ns | -0,11ns | -0,03ns |
| II | -0,23ns | -0,01ns | -0,12ns |
*Valor de R, acompañado de letra de significancia. ARC= arcilla. LIM= limo. ARE= arena. HUM= humedad.
DA= densidad aparente. K= conductividad hidráulica saturada. RES= resistencia a la penetración.
IBC= infiltración básica entre calles. II= infiltración instantánea. IB= infiltración básica. IIH= ns= no significativo.
*= significativo. **= altamente significativo.
Tabla 6 Relación entre el vigor de plantas de plátano y las características químicas del suelo en fincas.Sur del Lago de Maracaibo, Venezuela.
| Vigor de plantas/ | Vigor de plantas/ | Vigor de plantas/ | Vigor de plantas/ |
| pH | *0,01ns | 0,12ns | 0,01ns |
| CE | 0,22ns | 0,22ns | 0,24 ns |
| MO | 0,08ns | 0,01ns | - 0,05 ns |
| NT | -0,01ns | -0,09ns | 0,04 ns |
| AMON | 0,01ns | 0,21ns | 0,08 ns |
| PT | 0,11ns | -0,21ns | - 0,20ns |
| SC | 0,10ns | -0,07ns | 0,01ns |
| CICE | 0,09ns | -0,08ns | -0,01ns |
| SB | 0,26ns | 0,15ns | 0,02ns |
*Valor de R, acompañado de letras de significancia. CE= conductividad eléctrica. MO= materia orgánica. NT= nitrógeno total. Amon= amonio disponible. PT= fósforo total. SC= suma de cationes. CIC= capacidad de intercambio catiónico efectiva. SB= porcentaje de saturación de bases.
ns= no significativo. *= significativo. **= altamente significativo.
Tabla 7 Relación entre el vigor de plantas de plátano y la población total de fitonemátodos y géneros encontrados en raíces de plantas en fincas. Sur del Lago de Maracaibo, Venezuela.
| Vigor de plantas/características biológicas del suelo | Número de manos por racimo | Circunferencia de la planta madre | Altura del hijo de sucesión |
| PTNR | *-0,25* | -0,44* | -0,24ns |
| Aphelenchus sp. | -0,05ns | -0,07ns | -0,03ns |
| Basiria sp. | 0,07ns | -0,01ns | 0,26ns |
| Helicotylenchus sp. | -0,24* | -0,02ns | -0,28* |
| Helicotylenchus multicinctus. | 0,02ns | -0,18ns | -0,08ns |
| Meloidogyne sp. | -0,20ns | -0,24ns | -0,13ns |
| Pratylenchus sp. | -0,29* | -0,36* | -0,15ns |
| Radopholus similis. | 0,10ns | 0,19ns | 0,19ns |
| Rotylenchulus sp. | 0,01ns | -0,24ns | -0,10ns |
| Tylenchus sp. | 0,15ns | 0,07ns | 0,37* |
*Valor de R, acompañado de letra de significancia. PTNR= población total de fitonemátodos en raíces.
ns= no significativo. *= significativo. **= altamente significativo.
Tabla 8 Relación entre el vigor de plantas de plátano y la población total de bacterias y actinomicetos encontrados en suelos de fincas. Sur del Lago de Maracaibo, Venezuela.
| Vigor de plantas/características biológicas del suelo | Número de manos por racimo | Circunferencia de la planta madre | Altura del hijo de sucesión |
| PTB | *0,05ns | 0,06ns | -0,04ns |
| PTA | 0,18* | 0,08ns | 0,16* |
*Valor de R, acompañado de letra de significancia. PTB= población total de bacterias en suelos. PTA= población total de actinomicetos en suelos. ns= no significativo. *= significativo. **= altamente significativo.
Tabla 9 Relación entre el vigor de plantas de plátano y carbono microbiano y respiración basal del suelo de fincas. Sur del Lago de Maracaibo, Venezuela
| Vigor de plantas/características biológicas del suelo | Número de manos por racimo | Circunferencia de la planta madre | Altura del hijo de sucesión |
| Cmic | *0,03ns | 0,13* | 0,13* |
| RB | -0,06ns | 0,07ns | 0,05ns |
*Valor de R, acompañado de letra de significancia. Cmic= carbono microbiano en suelos. RB= respiración basal del suelo. ns= no significativo. *= significativo. **= altamente significativo.
En este sentido, se confirma que suelos con texturas arenosas no son favorables para la retención de humedad, al igual que suelos con estas características pueden favorecer pérdidas de nutrientes en procesos de lixiviación, lo cual ocasionaría un bajo vigor en las plantaciones de plátano (Loboet al.2011). En cuanto a la densidad aparente, valores altos generan procesos de compactación y dificultad de penetrar adecuadamente las raíces en capas más profundas del suelo, lo cual afecta la profundidad efectiva del sistema radical (Rodríguez 2009, Olivareset al.2020). De igual manera, valores altos de densidad aparente dificultan algunas propiedades de movimiento del agua dentro del perfil del suelo (Rodríguez y Lobo 2004, Reyet al.2009, Rodríguezet al.2010b). En tal sentido, Serrano (2002) expuso que valores de densidad aparente (Da) mayores 1,30 Mg.m-3, para suelos bananeros indican un grado de compactación moderada. De igual forma, Rodríguezet al.(2010a) señalaron valores limitantes para el desarrollo radical en banano de 1,4 Mg.m-3.
Resultados similares fueron presentados por Herreraet al.(2017) al evidenciar correlaciones negativas entre arena y la densidad aparente respecto al número de manos por racimo. Por su parte, Olivareset al.(2020) señalan que, para un índice de productividad de suelos en banano para regiones productoras de Venezuela, la compactación del suelo determinada por variables como densidad aparente y resistencia a la penetración, fueron seleccionadas dentro de los 5 indicadores que determina el modelo desarrollado por estas personas autoras.
Adicionalmente, se observa una correlación positiva y significativa entre limo y humedad con el número de manos por racimo. De esta manera, se infiere que, conforme aumenten los contenidos de limo y porcentaje de humedad, se incrementa el número de manos por racimo. Esto se encuentra asociado fundamentalmente a que ambas propiedades intervienen en la dinámica de disponibilidad de nutrientes y facilidad de intercambio de cationes en el suelo (Rodríguezet al.2010a).
Para el caso de las características químicas evaluadas, no se observaron correlaciones significativas respecto a las variables de vigor (Tabla 6). Al respecto, en investigaciones desarrolladas en banano relacionadas con índices de salud y calidad de suelo e índices de productividad de suelos en Venezuela, se ha identificado que la proporción de variables químicas que funcionan como indicadores ha sido menor comparado con las propiedades físicas y biológicas (Reyet al.2009, Delgadoet al.2010, Olivareset al.2020). Los resultados encontrados en la presente investigación no permitieron correlacionar variables químicas del suelo con los parámetros de vigor de las plantas de plátano en los suelos estudiados. Al respecto, las variables químicas en los lotes evaluados obtuvieron valores muy homogéneos, tal y como se evidencia en la Tabla 4. Por otra parte, Castañedaet al.(2014) encontraron en un estudio de variabilidad espacial de suelo y determinación de variables edáficas relacionadas con la producción de banano en suelos de Urabá, Colombia, una mayor proporción de propiedades químicas del suelo para identificar las variables con mayor potencial para la implementación en un programa de manejo por sitio específico.
Adicionalmente, se encontró una correlación significativa y negativa entre la población total de fitonemátodos en raíces (PTNR) y las variables de vigor estudiadas (número de manos por racimo y circunferencia de la planta madre). En cuanto a los géneros de los nemátodos, se determinó una correlación negativa entreHelicotylenchussp, y el NMR y la AHS; entrePratylenchussp y el NMR y la CPM; lo que significa que conforme aumente la PTNR y los géneros de fitonemátodos indicados, disminuirán las características de vigor en el cultivo de plátano (Tabla 7).
Los principales fitonemátodos que causan pérdidas económicas en el cultivo del banano y plátano son los endoparásitos migratoriosRadopholus similisyPratylenchus coffeae, el ectoparásito migratorioHelicotylenchus multicinctusy el endoparásito sedentarioMeloidogynespp (Torrado y Castaño 2009). Por su parte, Guzmán (2011) señala que en banano y plátano, generalmente, se encuentran comunidades poli específicas, compuestas por los 4 principales fitonemátodos, anteriormente mencionados y que la importancia económica se presenta en el siguiente orden:R. similis>Helicotylenchusspp. >Meloidogynespp. >Pratylenchusspp.
En estudios de salud y calidad de suelos en banano para 2 regiones productivas de Venezuela, se determinó que unos de los indicadores que aportaba al índice de salud y calidad del suelo eran nematodos de vida libre totales y bacteriófagos, aunque estos no son patogénicos, son importantes a tener en cuenta cuando se desee evaluar aspectos de la salud del suelo (Delgadoet al.2010). De igual modo, Olivareset al.(2020) en un estudio de relación de propiedades del suelo con parámetros de vigor y productividad de banano en Venezuela, propone como parte del índice de productividad de suelo los nemátodos omnívoros de vida libre. Por otra parte, los nemátodos fitoparásitos son determinantes en la salud del sistema radical en plantas de banano y plátano (Rodríguez 2009).
Los resultados de poblaciones totales de bacterias no presentan correlaciones significativas (Tabla 8), lo que implica que las poblaciones microbianas sobreviven con el aporte de nutrimentos añadidos por los fertilizantes (Meena y Meena 2017, Horwarth 2017). Sin embargo, para actinomicetos, se observaron correlaciones positivas y significativas respecto a NMR y AHS. En tal sentido, estos microorganismos son conocidos por desarrollar diversas actividades en el ecosistema, tales como el mejoramiento de la estructura del suelo y producción de compuestos bioactivos con actividad antagonista contra microorganismos patógenos, por lo que son los principales productores de antibióticos. Otros estudios han descrito actividades que pueden catalogar a los actinomicetos como rizobacterias promotoras del crecimiento (Franco-Correa 2009). Además, tienen gran importancia en la participación de la degradación de materia orgánica, intervienen en interacciones entre planta-microorganismo, que permiten desarrollar una autentica micorrizosfera que promueve el crecimiento y nutrición de las plantas (Chaurasiaet al.2018, Vurukondaet al.2018).
De igual manera, se observó que no hay correlación lineal entre carbono microbiano y NMR, pero sí una correlación positiva y significativa entre esta variable y CPM y AHS. En cuanto a la respiración basal del suelo, no se determinó una correlación con respecto a alguna de las variables de vigor estudiadas (Tabla 9). Al respecto, estudios de variables de vigor y productividad en banano enfocados en índice de salud y calidad del suelo (Reyet al.2009, Delgadoet al.2010) y para índices de productividad del suelo (Olivareset al.2020) han considerado variables biológicas, como respiración microbiana total y biomasa de la materia orgánica, como indicadores importantes en cuanto a la parte biológica del suelo.
El carbono microbiano ha sido frecuentemente estudiado por su alta y rápida sensibilidad a los cambios que se producen en el sistema y, además, porque es uno de los pocos que controla parte de los procesos que involucran la transformación y el ciclado de nutrientes, así como la macroagregación, lo cual favorece la retención de agua y la aireación del suelo (Pérezet al.2017, Renet al.2019). Variables como carbono microbiano están asociadas a la cantidad y actividad de los microorganismos del suelo (Velmourougane 2016, Yanget al.2017, Vurukondaet al.2018). En tal sentido en lotes de alto vigor, el carbono microbiano se encontró con valores más altos.
Morocho y Leiva (2019) señalaron que los microorganismos pueden promover el reciclaje de nutrientes en el suelo, así como incrementar la disponibilidad de nutrientes para las plantas, lo cual implica una mejor respuesta en el desarrollo de los cultivos. De igual modo, podrían presentarse a partir de la diversidad de microorganismos identificados, otros beneficios como promoción de crecimiento como biofertilizantes (Waliaet al.2013, Beltrán 2014), estimulación en la formación de raíces y mejora en la nutrición de las plantas (Aunget al.2018), solubilización de fósforo (Satyaprakashet al.2017), fijación de nitrógeno (Grajoet al.2017, Kakraliya y Singh 2018), solubilización de hierro o producción de sideróforos (Aguado-Sánchezet al.2012) y actividad antagonista frente a patógenos (Chaurasiaet al.2018).
Con respecto a la diversidad de hongos encontrados en la Figura 1, se presentan los resultados en lotes de vigor contrastantes. La biodiversidad fúngica predominante en suelos cultivados con plátano en la zona Sur del Lago estuvo representada por 4 hongos que se identificaron como:Aspergillussp,Fusariumspp,Penicilliumsp yTrichodermasp. Así, de los hongos identificados, no se observaron diferencias estadísticas entre los suelos cultivados con plantas de plátano de diferente vigor para UFC deFusariumspp.,Penicilliumsp. Micelio estéril yTrichodermasp. Sin embargo, en el lote de AV se evidenció un valor más elevado de UFC paraTrichoderma. Por otra parte, se identificaron mayor UFC deAspergillussp. en suelos con lotes de BV respecto a los de AV.
En ese sentido,Trichodermase incluye entre los hongos con capacidades de bioestimulación, ya que promueven el crecimiento y el vigor en las plantas por la habilidad que poseen para hacer que las raíces sean más robustas, aspecto que favorece mayor profundidad, porque son más resistentes a las sequías y pueden absorber más nutrientes (Donosoet al.2008, Valdés 2014, Santana y Castellanos 2018).
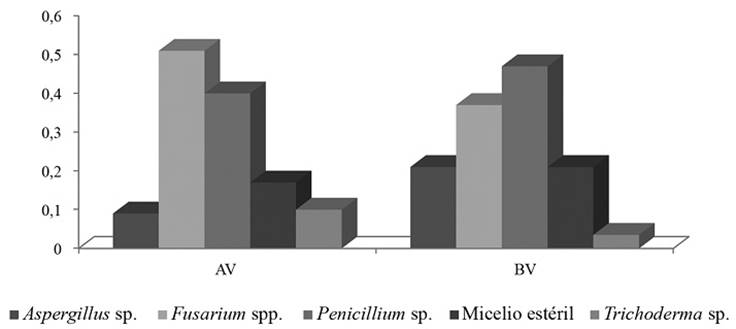
Columnas acompañadas por letras distintas señalan diferencias estadísticas entre lotes de plantas de plátano (p<0,05).
Cada barra representa el total de unidades formadoras de colonia de los hongos aislados en suelos cultivados con plátano. AV= lotes plantas de plátano de alto vigor. BV= lotes de plantas de plátano de bajo vigor.
Figura 1 Unidades formadoras de colonias de hongos aislados en suelos cultivados con plantas de plátano de diferente vigor. Sur del Lago de Maracaibo, Venezuela.
Análisis multivariado
Para buscar relaciones no lineales entre todas las variables edáficas evaluadas y los parámetros de vigor en plantas de plátano, se realizó un análisis de los componentes principales de los cuales los 3 primeros explicaron el 62% de la variabilidad encontrada, porcentaje que coincide con lo reportado por Yanet al.(2000).
Para adoptar una decisión definitiva en la selección de las variables, fue necesario examinar los vectores propios entre las variables originales y los componentes principales, aspecto que indica que las variables con los valores más altos en los componentes seleccionados serán las de mayor importancia (Pla 1986). En este sentido, al evaluar los vectores propios de la matriz correlación de las 20 variables edáficas evaluadas, se observaron altos valores para 15 de ellas (conductividad eléctrica, materia orgánica, carbono microbiano, respiración basal a los 4, 7 y 10 días, fósforo disponible, capacidad de intercambio catiónico, densidad aparente, población total de hongos, bacterias y actinomicetos, % de arena y limo, coeficiente metabólico). Con base en estas variables, se realizó el biplot multivariado para evaluar las interrelaciones entre las variables y los lotes de alto y bajo vigor del cultivo de plátano.
Yanet al.(2000) señalan que en los biplot de análisis multivariado, cuando los ángulos entre los vectores son de 180°, las relaciones son inversas; si el ángulo es 0°, el coeficiente es positivo aspecto que expone que hay relaciones importantes entre las variables, mientras que para ángulos de 90° no hay relaciones entre las mismas, situación que permite la posibilidad de detectar relaciones entre variables y fincas, de tal forma que se puedan identificar aquellas que estén positiva o negativamente relacionadas.
Seguidamente, se analizaron las correlaciones de las variables con mayor aporte en cada componente (Tabla 10) y se pudo determinar que las características del suelo que prioritariamente definen a cada componente son la biomasa y la actividad microbiana, la capacidad de intercambio catiónico y textura (componente 1; 38%), materia orgánica y diversidad de microorganismos (componente 2; 12%) y densidad aparente, así como la conductividad eléctrica (componente 3; 11%). De esta forma los análisis confirman la significancia de las variables analizadas en forma de correlaciones lineales, que afectaron la expresión del vigor de plantas de plátano. Adicionalmente, permitió observar en forma conjunta, variables que se pueden asociar a propiedades funcionales del suelo, más allá de la interpretación de los resultados de variables individuales.
Tabla 10 Correlaciones con las variables originales, pare determinar aquellas mayormente relacionadas con los componentes definidos en el análisis multivariado.
| Variables | CP 1 | CP 2 | CP 3 |
| CE | -0,75 | -0,25 | -0,46 |
| MO | -0,57 | 0,72 | -0,01 |
| CM | -0,45 | -0,14 | 0,53 |
| RB4 | 0,55 | -0,05 | 0,47 |
| RB7 | 0,81 | -0,33 | 0,23 |
| Pdisp | -0,67 | 0,53 | 0,01 |
| SC | -0,8 | 0,3 | 0,45 |
| CIC | -0,81 | 0,29 | 0,43 |
| DA | 0,2 | -0,16 | 0,64 |
| k | 0,25 | 0,32 | -0,2 |
| TBACT | 0,46 | 0,68 | -0,26 |
| TACTI | -0,21 | -0,43 | -0,59 |
| THONG | -0,24 | 0,36 | -0,14 |
| ARE | 0,69 | 0,32 | -0,13 |
| HUM | -0,68 | -0,08 | -0,16 |
| LIM | -0,68 | -0,34 | 0,14 |
| AMON | -0,68 | -0,13 | -0,36 |
| RB10 | 0,71 | 0,05 | -0,05 |
| CmicCOT | 0,86 | 0,09 | -0,09 |
| qCO2 | -0,56 | -0,37 | 0,04 |
| Correlación cofenética= 0,911 |
CE= conductividad eléctrica; MO= materia orgánica; CM= carbono microbiano; RB 4, 7, 10= respiración basal a los 4, 7 y 10 días; Pdisp= fósforo disponible; SC= suma de cationes; CIC= capacidad de intercambio catiónico; DA= densidad aparente; K= conductividad hidráulica saturada; TBACT= total de baterías; TACT= total de actinomicetos; THONG= total de hongos; ARE= % de arena; HUM= contenido de humedad; LIM= % de limo; AMON= contenido de amonio; CmicCOT= relación carbono microbiano= carbono orgánico total; qCO2= coeficiente metabólico.
Los lotes de vigor evaluados en puntos 1 al 8 alto vigor y 9 al 16 bajo vigor se relacionaron con los vectores representados por las variables que presentaron mayor peso, para explicar la variabilidad existente así se evidenciaron los lotes de alto vigor asociados a las variables contenido de actinomicetos y hongos, materia orgánica, coeficiente metabólico y aspectos de fertilidad (CIC, fósforo y amonio), los cuales se observan en la parte izquierda de la gráfica, mientras que los lotes de bajo vigor se asocian predominantemente con variables como respiración basal, carbono microbiano y densidad aparente (Figura 2).
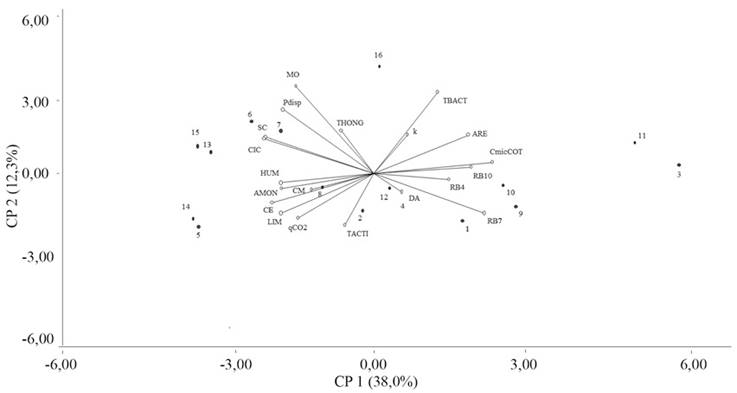
Figura 2 Biplot multivariado por componentes principales en 16 lotes de plátano (1-8 alto vigor) y (9-16 bajo vigor) en las 20 variables evaluadas.
Se identificaron variables edáficas asociadas a las respuestas del cultivo de plátano en términos de vigor, que se deberán considerar para diseñar estrategias de manejo como, la preparación de suelo, enmiendas orgánicas, fertilización y riego en función de la dinámica las propiedades físicas, químicas y biológicas.
Conclusiones
Los parámetros del cultivo tales como número de manos por racimo, circunferencia de la planta madre y la altura del hijo de sucesión fueron adecuados para separar lotes de vigor contrastantes.
Los lotes de AV y BV expusieron correlaciones significativas con variables de física de suelos como % de arena, % de limo y densidad aparente. En cuanto a las variables químicas, el contenido de P disponible y la CIC presentaron un mayor peso en la respuesta del vigor del cultivo. Finalmente, en cuanto a las propiedades biológicas, el carbono microbiano y respiración basal, fueron las variables que se relacionaron en mayor medida con los lotes de bajo vigor.
El conocimiento de las variables edáficas que mayormente inciden sobre los parámetros del vigor del cultivo de plátano aportan información valiosa para el diseño de prácticas de manejo para mejorar condiciones de desarrollo y productividad del cultivo de plátano en las condiciones de los suelos evaluados.















