Introducción
El cultivo de vitro plantas es una técnica comúnmente utilizada en la agricultura para propagar material vegetal de alta calidad agronómica, el cual, a su vez, debe estar libre de plagas y enfermedades, principalmente de virus. De esta forma, los laboratorios dedicados a la producción in vitro seleccionan y producen plantas en masa a las que se les proporciona las condiciones necesarias de luz y nutrimentos para su desarrollo. Una vez listas las plantas, se aclimatan y trasladan al campo para ser cultivadas (Roca y Mroginski 1993, Sriskandarajah 2006, Conger 2018). Esta técnica se ha vuelto esencial para la reproducción de plantas por parte de varias empresas agrícolas dedicadas a la producción de raíces, tubérculos, frutas como piña y banano, forestales y ornamentales, lo cual aumenta las exportaciones de vitro plantas desde Costa Rica hacia países como Tailandia, Estados Unidos, México, Venezuela, Chile, algunos países de Centroamérica y de Europa (Cabezas 2006, El Financiero 2016, Summa 2016, Agribio 2019, Agrovitro 2019).
El cultivo de tejidos vegetales se realiza en un medio artificial con condiciones asépticas (Leifert et al. 1991, Loyola-Vargas y Ochoa-Alejo 2018), las cuales se alcanzan mediante el empleo de protocolos de desinfección del material a introducir, conocido como explante, así como la realización de rutinas de limpieza en las instalaciones, para así, evitar el ingreso de contaminantes ambientales a los frascos donde crecen las plantas (Cassells 2000, Sriskandarajah 2006). Durante la etapa de establecimiento, el material vegetal es considerado la principal fuente de contaminación, debido a la presencia endógena y exógena de hongos, levaduras y bacterias, los cuales se pueden desarrollar en los medios de cultivo, especialmente durante los primeros 2 meses. Sin embargo, posterior a este tiempo, los explantes pueden presentar contaminantes provenientes del ambiente o debido a la manipulación de los cultivos dentro del laboratorio (Cassells 1991, Leifert et al. 1994, Leifert y Cassells 2001, Odutayo et al. 2007, González y Hernández 2010, Cassells 2012).
A pesar de que se toman varias medidas para evitar contaminación en las plantas cultivadas in vitro, la presencia de microorganismos causa grandes pérdidas en la producción, las cuales pueden ir desde un 3% hasta un 55% (Boxus y Terzi 1987, Leifert et al. 1994, Gamborg y Phillips 1995). Así, aquellos laboratorios que presentan altos niveles de contaminación deben realizar diariamente control de calidad de los frascos en los cuartos de crecimiento, lo cual conlleva a un aumento significativo en los costos de producción, ya que esta práctica demanda gran cantidad de tiempo del personal que trabaja en los laboratorios (Fontúrbel 2001, González y Hernández 2010). Asimismo, estas empresas deben diseñar estrategias de desinfección y combate más efectivas en el manejo de contaminantes lo cual encarecería aún más sus costos.
Muchas veces la aparición súbita y exponencial de contaminantes, fúngicos o bacterias en los explantes, está asociada con la presencia de plagas artrópodas, como los ácaros, quienes están estrechamente relacionados a estos microorganismos debido a que en la mayoría de los casos, se alimentan de los hongos que crecen dentro de los frascos (Jong 1987, Pype et al. 1997, Hubert et al. 2003, Sriskandarajah 2006, González y Hernández 2010).
Las infestaciones de estos artrópodos son difíciles de manejar, al ser organismos microscópicos con alta capacidad para ingresar o salir de los frascos y de difícil detección. Una vez que los ácaros llegan al laboratorio, pueden migrar de un frasco a otro y distribuirse fácilmente; por esta razón, son considerados una plaga en cultivo de tejidos de plantas, pues ocasionan pérdidas en la producción (Pype et al. 1997, Duek et al. 2001). Aunque los ácaros usualmente causan un daño mínimo a los explantes, conforme estos migran pueden transportar en su cuerpo bacterias y esporas de hongos a nuevos sustratos (Pype et al. 1997, Hubert et al. 2004), que crecen en el medio de cultivo y son tomados por el ácaro como fuente de alimento.
Los laboratorios de cultivo in vitro han realizado esfuerzos por mantener bajos los niveles de contaminación; sin embargo, varias personas autoras mencionan que el 50% de los laboratorios han tenido problemas de contaminación en algún momento a causa de los ácaros y, en otros casos, han causado pérdidas totales del material vegetal (Blake 1988, Pype et al. 1997, Van Epenhuijsen y Koolaard 2004a).
Actualmente, las empresas cuentan con pocas herramientas para enfrentar esta problemática, pues no se han estudiado estos organismos bajo condiciones in vitro. En la mayoría de los casos, el manejo se efectúa al descartar los frascos infestados y por medio de fumigaciones con acaricidas en el laboratorio (West y Preece 2006). Para el manejo de los ácaros, hongos y bacterias asociados como contaminantes, es necesario realizar una adecuada identificación de las especies involucradas y estudiar las interacciones que ocurren entre estos organismos, ya que algunos ácaros requieren de especies de hongos específicas para su sobrevivencia.
Según el incremento de problemas ocasionados por los ácaros bajo condiciones in vitro en el país, su difícil detección y escasa información, se identificaron las principales especies de ácaros encontrados en algunos laboratorios comerciales de cultivo de tejidos vegetales del Valle Central.
Materiales y métodos
Recolección e identificación de ácaros
Debido a la presencia súbita de microorganismos como hongos y bacterias en los medios de cultivo, de 7 laboratorios ubicados en el Valle Central del país (Tabla 1), los cuales están dedicados a la producción in vitro de plantas, que fueron recibidos en el Laboratorio de Acarología, se inició con la búsqueda de posibles artrópodos como los ácaros, que pudieran estar asociados con el incremento de contaminación percibido por estas empresas.
De acuerdo con la cantidad de material in vitro encontrado con contaminantes en cada laboratorio, se seleccionó una submuestra (de un 30% hasta un 50%), por lo que se recolectaron en total unos 600 frascos (9 x5 cm) con varios tipos de vitro plantas. Dichas muestras contenían explantes de Dieffenbachia sp., Spathiphyllum sp., Calathea sp., Ficus sp., Xanthosoma sp., Phalaenopsis sp., Anthurium sp., Musa acuminata y Dianthus caryophyllus (Tabla 1). Los frascos se llevaron al Laboratorio de Acarología del Centro de Investigación en Protección de Cultivos de la Universidad de Costa Rica, donde se comprobó la presencia y frecuencia de estos artrópodos en las vitro plantas.
Tabla 1 Tipo de material vegetal, lugar de procedencia, número total de frascos procesados y fecha de recolección de las muestras provenientes de diferentes laboratorios de cultivo de tejidos.
| Laboratorio | Material vegetal in vitro | Provincia de procedencia | Número de frascos | Fecha |
| 1 | Spathiphyllum sp. | Heredia | 20 | 1/IX/05 |
| 1 | Anthurium sp. | Heredia | 15 | 1/IX/05 |
| 1 | Spathiphyllum sp. | Heredia | 12 | 19/X/05 |
| 1 | Spathiphyllum sp. | Heredia | 5 | 17/V/06 |
| 2 | Anthurium sp. | Alajuela | 30 | 19/X/05 |
| 2 | Diffenbachia sp. | Alajuela | 41 | 16/XI/05 |
| 2 | Spathiphyllum sp. | Alajuela | 36 | 16/XI/05 |
| 2 | Calathea sp. | Alajuela | 5 | 16/XI/05 |
| 2 | Anthurium sp. | Alajuela | 23 | 28/II/06 |
| 2 | Diffenbachia sp. | Alajuela | 15 | 8/III/06 |
| 2 | Anthurium sp. | Alajuela | 20 | 8/III/06 |
| 2 | Calathea sp. | Alajuela | 45 | 8/III/06 |
| 2 | Ficus elastica | Alajuela | 19 | 14/III/06 |
| 2 | Calathea sp. | Alajuela | 38 | 13/IX/06 |
| 2 | Anthurium sp. | Alajuela | 41 | 25/VIII/08 |
| 2 | Anthurium sp. | Alajuela | 24 | 12/XI/08 |
| 3 | Phalaenopsis sp. | Alajuela | 12 | 28/II/06 |
| 3 | Phalaenopsis sp. | Alajuela | 15 | 20/VII/06 |
| 3 | Phalaenopsis sp. | Alajuela | 30 | 29/VIII/07 |
| 4 | Xanthosoma sp. | San José | 5 | 21/XI/06 |
| 5 | Phalaenopsis sp. | Alajuela | 20 | 06/IX/08 |
| 5 | Phalaenopsis sp. | Alajuela | 15 | 13/IX/08 |
| 5 | Phalaenopsis sp. | Alajuela | 32 | 20/VII/10 |
| 5 | Phalaenopsis sp. | Alajuela | 10 | 07/VIII/10 |
| 5 | Phalaenopsis sp. | Alajuela | 12 | 21/I/11 |
| 5 | Phalaenopsis sp. | Alajuela | 25 | 23/VI/11 |
| 6 | Ficus eximia | Heredia | 10 | 20/IV/10 |
| 6 | Dianthus caryophyllus | Heredia | 5 | 20/IV/10 |
| 7 | Musa acuminata | Cartago | 20 | 31/V/10 |
El material se observó con ayuda de un estereoscopio marca Nikon modelo SMZ-645. Los ácaros encontrados fueron recolectados en un frasco con etanol al 70%. Una vez obtenidos los especímenes, se realizaron los montajes respectivos en portaobjetos con medio de Hoyer (Walter y Krantz 2009) y se cubrieron con cubreobjetos circulares (18mm); luego se colocaron en una estufa (40oC-45oC) por al menos 3 días. Finalmente, se procedió a sellar las láminas con barniz para pisos, poliuretano brillante.
Posteriormente, los ácaros se observaron bajo el microscopio de luz (Olympus BX51 con contraste de fases) y se realizaron los respectivos estudios taxonómicos para su identificación por medio de las claves taxonómicas de Hughes (1976), Fan y Zhang (2007) y Kaliszewski (1987).
El material identificado se encuentra depositado en la colección de referencia de ácaros de importancia agrícola en el Laboratorio de Acarología.
Identificación de los hongos
Se realizaron aislamientos de los hongos, encontrados en asociación, con los ácaros hallados en los frascos provenientes de cada laboratorio. Los aislamientos se llevaron a cabo en una cámara de flujo laminar en el Laboratorio de Acarología.
Los hongos encontrados se cultivaron en cajas petri (100 mm x 15 mm) en medio de cultivo Papa Dextrosa Agar (PDA) acidificado. En cada plato se colocaron segmentos del micelio de cada hongo, los cuales se mantuvieron a temperatura ambiente (22oC-26oC) durante cuatro días para permitir que el micelio cubriera el medio de PDA. Luego, se procedió con la identificación morfológica de los hongos aislados por medio de las claves taxonómicas especializadas de Barnett y Hunter (1972).
Resultados
Especies de ácaros encontradas y frecuencia de aparición
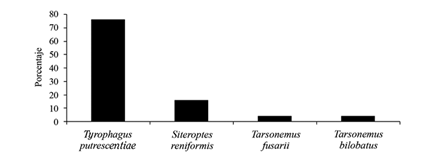
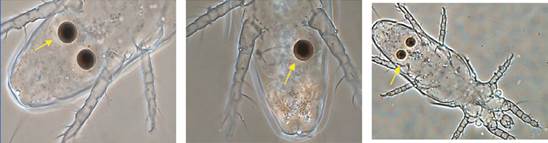
Los ácaros encontrados en los frascos fueron identificados como: Siteroptes reniformis Krantz (Acari: Siteroptidae) (Figura 1), Tyrophagus putrescentiae Schrank (Acari: Acaridae) (Figura 2), Tarsonemus bilobatus Suski (Figura 3A) y T. fusarii Cooreman (Acari: Tarsonemidae) (Figura 3B).

Figura 1. Siteroptesreniformis (A) en plantas in vitro; (B) en hojas de plantas in vitro; (C) vista dorsal de hembra.

Figura 2 Tyrophagus putrescentiae (A) en plantas in vitro; (B) alimentándose de hifas en frascos de cultivo de tejidos; (C) vista dorsal de hembra.
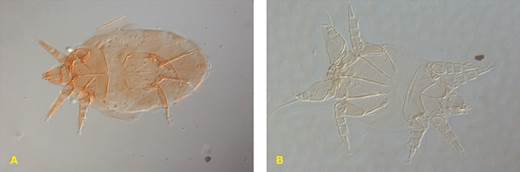
Figura 3 (A) Hembra de Tarsonemus bilobatus (vista ventral) (B) Macho de Tarsonemus fusarii (vista ventral).
Además, se comprobó que T. putrescentiae es la principal especie de ácaro encontrada en los laboratorios puesto que se halló en un 76% de las muestras analizadas (Figura 4). Asimismo, se encontró la especie S. reniformis en un 16% de los frascos y, en menor frecuencia, las especies T. bilobatus y T. fusarii, ambas representadas en un 4% de las muestras.
Asociación de los ácaros con los hongos.
La mayor parte del material examinado en el laboratorio presentaba problemas de contaminación causado por hongos, los cuales se desarrollaron principalmente sobre el medio de cultivo (Figura 5). Al observar los frascos al estereoscopio, también se encontró la presencia de ácaros asociados con los hongos.
Los hongos encontrados y aislados de los explantes fueron identificados como Mucor spp., Penicillium spp., Leptosphaerulina spp. y Cladosporium spp., los cuales estuvieron relacionados con el ácaro T. putrescentiae; mientras que Nigrospora oryzae (Berk. & Broome) Petch fue el único hongo asociado con el ácaro S. reniformis (Tabla 2). Por otra parte, se observó que esas especies de ácaros tienen la capacidad de transportar los hongos hasta un nuevo sustrato, ya sea al llevar las esporas sobre la superficie de su cuerpo, como en el caso de T. putrescentiae (Figura 6), o por medio de unas estructuras especializadas llamadas esporotecas (Figura 7), como en el caso de la especie S. reniformis.
Tabla 2 Principales ácaros encontrados en los diferentes laboratorios de cultivo de tejidos y su asociación con hongos.
| Familia de ácaro | Especie | Hongo asociado |
| Acaridae | Tyrophagus putrescentiae | Cladosporium spp. Penicillium spp. Leptosphaerulina spp. |
| Siteroptidae | Siteroptes reniformis | Nigrospora oryzae |
Discusión
Las especies de ácaros, localizadas en los explantes de vitro plantas, fueron detectadas en la mayoría de los casos por parte del personal que trabaja en los laboratorios, al percibir un aumento en los niveles de contaminación causado principalmente por hongos. El medio de cultivo que se utiliza para la propagación de plantas en los laboratorios (alto en azúcares), así como las condiciones que se crean dentro de los frascos (alta humedad relativa y temperatura estable), conforman un ambiente propicio para la proliferación de microorganismos como hongos y bacterias; asimismo, para el establecimiento de artrópodos pequeños como los ácaros (Blake 1988, Leifert y Cassells 2001, Cassells 2012).
Aunque la presencia de muchos de estos hongos a nivel de campo no representa un daño significativo para la planta, bajo condiciones in vitro (óptimas en nutrimentos y azúcar), se desarrollan rápidamente y resultan letales para los explantes en un corto periodo de tiempo. En este caso, los microorganismos, que se desarrollan dentro de los frascos, contaminan el medio de cultivo y compiten con las plántulas, principalmente por espacio y nutrimentos (Roca y Mroginski 1993, Leifert et al.1994, Fontúrbel 2001, Odutayo et al. 2007, Kane et al. 2011). De esta forma, los ácaros que ingresan a los frascos son los principales responsables de dispersar los hongos y bacterias de un lugar a otro, que disparan los niveles de contaminación en los laboratorios.
Durante esta investigación, se encontró a T. putrescentiae (Acari: Acaridae) y S. reniformis (Acari: Siteroptidae) como las principales especies recuperadas en los laboratorios del país (Figura 4), las cuales ocasionan pérdidas en la producción de vitro plantas. En otros países, estas 2 especies han sido reportadas como los principales contaminantes en laboratorios, así como las especies Siteroptes graminis Krczal, S. avenae Müller, Tyrophagus neiswanderi Johnston y Bruce, T. perniciosus Zachvatkin (Acari: Acaridae), Tarsonemus bilobatus Suski, Phytonemus pallidus Banks (Acari: Tarsonemidae), y algunos ácaros depredadores como Amblyseius sp. (Acari: Phytoseiidae) (Blake 1988, Vargas y Ochoa 1990, Pype et al. 1997, Van Epenhuijsen y Koolaard 2004b).
Se evidenció que estas 2 especies tienen una alta capacidad para diseminar hongos ya sea sobre la superficie del cuerpo o en las setas, como en el caso de T. putrescentiae (Figura 6), o al utilizar estructuras especializadas para el transporte de esporas (Figura 7), como en S. reniformis (Van Epenhuijsen y Koolaard 2004b, Terras et al. 1991), desde donde son distribuidas rápidamente en el sustrato y causan problemas de contaminación (Hughes 1976, Krantz y Lindquist 1979, Jong 1987, Abdel-Sater et al. 1995, Van Asselt 1999, Duek et al. 2001, Leifert y Cassells 2001, Hubert et al. 2004).
De estas 2 especies, T. putrescentiae no solo se encontró con mayor frecuencia en las muestras, sino que se vinculó con varios hongos (Tabla 2). Este ácaro usualmente opta por alimentos con un alto contenido en grasa y proteína como jamón, tocino, harina de trigo, queso, leche seca, semillas y otros productos almacenados (Hughes 1976, Flechtmann 1986, Van Asselt 1999, Duek et al. 2001, Zhang 2003, Fan y Zhang 2007, Erban et al. 2015, 2016, Rybanska et al. 2015, da Silva et al. 2018). Sin embargo, estos ácaros también pueden sobrevivir en sustratos no tan ricos en grasas y se ha reportado que se alimentan de hifas y esporas de múltiples hongos (Terras et al. 1991, Hughes 1976, Abdel-Sater et al. 1995, Hubert et al. 2004, Murillo 2011, da Silva et al. 2019).
Así, en el presente trabajo se encontró a T. putrescentiae dentro de los frascos in vitro alimentándose de hongos como Penicillium spp., Cladosporium spp., Mucor spp. y Leptosphaerulina spp., lo cual confirmó la gran plasticidad de esta especie. Varias personas autoras mencionan que esta plasticidad está relacionada con la presencia y actividad de lizoenzimas y bacterias en el tracto digestivo de este ácaro, lo que les permite sobrevivir en distintos sustratos (Duek et al. 2001, Smrž 2003, Hubert et al. 2004, Erban y Hubert 2008, Erban et al. 2016). Asimismo, Erban et al. (2016) encontraron que la microbiota presente en las poblaciones de T. putrescentiae influye con la capacidad de este ácaro para digerir alimentos.
El ácaro Tyrophagus juega un rol importante como contaminante en laboratorios de cultivo de tejidos, así como en colonias de insectos y hongos, al tener una gran capacidad para migrar y reproducirse (Krantz y Lindquist 1979, Jong 1987, Blake 1988, Smrž y Jungová 1989, Fan y Zhang 2007, Murillo 2011, Murillo et al. 2018, da Silva et al. 2019). Esta especie cosmopolita usualmente se introduce en los laboratorios por medio de material infestado, o logra ingresar por las aberturas de los frascos, donde la población se incrementa en pocos días al tener las condiciones propicias para su desarrollo (Jong 1987, Van Epenhuijsen y Koolaard 2004a, Murillo 2011, Silva et al. 2018).
Además, de T. putrescentiae, se encontró en menor proporción la especie S. reniformis (Figura 4), la cual se alimenta exclusivamente del hongo N. oryzae (Tabla 2) (Aguilar et al. 2006). Los ácaros de este género, a diferencia de Tyrophagus, son estrictamente fungívoros y mantienen una relación simbiótica con la especie de hongo de la cual se alimentan (Laemmlen y Hall 1973, Khaustova y Ermilov 2011). En el caso particular de S. reniformis, tiene la capacidad de acarrear e inocular el hongo N. oryzae en un ambiente favorable para su desarrollo, ya sea a nivel de laboratorio o de campo donde ha sido encontrado en plantaciones de sorgo, maíz y algodón, siempre asociado a este hongo (Terras et al. 1991, Laemmlen y Hall 1973, Palmateer y Mc Lean 2003).
Esta especie en particular, posee unas estructuras en forma de “sacos” llamadas esporotecas, localizadas en la base del último par de patas (pata IV), en la parte ventral del histerosoma. Las esporotecas le permiten a S. reniformis portar solamente una o 2 esporas del hongo N. oryzae (Figura 7), hasta que encuentra un sustrato adecuado donde las deposita para su germinación y, de esta forma, iniciar nuevamente el ciclo (Lindquist 1985, De Lillo 1996, Terras et al. 1991).
Finalmente, se encontraron e identificaron 2 especies de ácaros del género Tarsonemus (Figura 3), también relacionados con el transporte de esporas de hongos (Ochoa et al. 1991). Vargas y Ochoa (1990) se refieren a T. bilobatus como contaminante en medios de cultivo y distinguen la presencia de esporas de Penicillium spp. y Alternaria spp. adheridas al cuerpo y detrás de las coxas II de estos ácaros. Asimismo, Ochoa et al. (1991) encontraron a T. fusarii con esporas de hongos adheridas sobre la parte dorsal del cuerpo. Sin embargo, durante la elaboración de este estudio, aunque se recolectaron a estos 2 tarsonémidos asociados con varios hongos, estos fueron localizados en las mismas muestras que T. putrescentiae y no se hallaron esporas de ningún hongo en particular, adheridas a su cuerpo.
En Costa Rica, los ácaros encontrados en los laboratorios de cultivo de tejidos están asociados con uno o varios hongos, según la especie de ácaro observado. Todas las especies de ácaros recuperados en este sistema tienen la capacidad de diseminar las hifas o esporas de los hongos, ya sea sobre la superficie de su cuerpo o por medio de estructuras especializadas. Por lo general, cuando se observa un aumento considerable en los niveles de contaminación por hongos y bacterias en los explantes cultivados in vitro, esto se deba a la presencia de ácaros en los laboratorios, por lo que se recomienda al personal que trabaja en dichos laboratorios prestar atención a los niveles de contaminación en los frascos e implementar medidas de monitoreo y control para la erradicación de estos artrópodos.