Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Ciencias Médicas
Print version ISSN 0253-2948
Rev. costarric. cienc. méd vol.28 n.1-2 San José Jun. 2007
Patrones Indeterminados de Western Blot en sueros reactivos por anticuerpos contra los virus linfotrópicos de células T tipo I/II (HTLV I/II) en donantes de sangre en Costa Rica
Western Blot indeterminate patterns in reactive serum by antibodies against T lynphotropic virus I/II (HTLV I/II) in blood donors in Costa Rica
Ximena Cortés ¹,², Zaida García, Lorena Torres³, Lizeth Taylor¹,²
1. Departamento de Virología. Facultad de Microbiología. Universidad de Costa Rica. San José, Costa Rica.
2. Centro Internacional de Investigación y Adiestramiento Médico (ICMRT). Facultad de Microbiología. Universidad de Costa Rica. San José, Costa Rica.
3. Subárea Laboratorios Clínicos. Área Regulación y Sistematización de Servicios de Salud. Caja Costarricense de Seguro Social. San José, Costa Rica.
Resumen
Los virus linfotrópicos humanos tipo I y II (HTLV I/II) son retrovirus asociados a diferentes patologías. El HTLV I fue el primer retrovirus relacionado con enfermedad y ocasiona principalmente dos tipos de patologías: la leucemia o linfoma de células T del adulto (LTA) y la paraparesia espástica tropical (PET). El HTLV-II se ha asociado a cuadros neurológicos similares. Centroamérica, América del Sur y el Caribe se definen como áreas de alta prevalencia.
Para prevenir la transmisión de la infección de estos retrovirus, se ha implementado el tamizaje de la donación sanguínea en muchos países, incluido Costa Rica. En donadores tamizados la técnica de Western Blot (WB) ha demostrado una actividad incompleta de anticuerpos contra los antígenos virales. Estos patrones se definen como indeterminados. Entre diciembre del 2002 y marzo del 2006 se reportaron los siguientes resultados de WB al evaluar sueros reactivos por ensayo inmunoenzimático: 39 (0,02%) donantes positivos, 254 (0,14%) indeterminados y 113 (0,06%) negativos. Se seleccionaron 42 muestras indeterminadas y 25 positivas para ser analizadas por un sistema comercial (HTLV I/II Blot 2.4); las positivas se clasificaron como: 15 HTLV I, 8 HTLV II y dos muestras indeterminadas. Del grupo de indeterminados se presentaron 4 resultados no concordantes: 1 HTLV II, 1 HTLV y 2 negativos. Se demostró que, en muestras nacionales, patro-nes positivos débiles pueden estar relacionados a WB indeterminados o a reactividad parcial de infección por HTLV II.
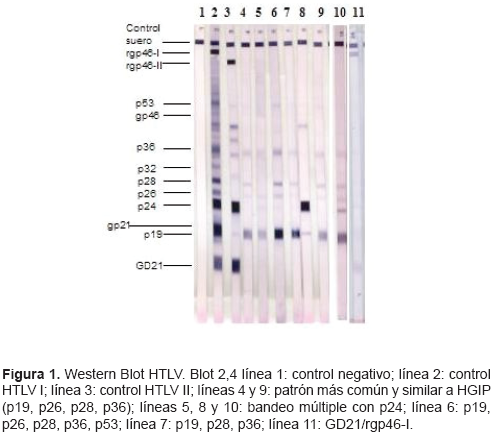
El patrón indeterminado más descrito se denomina HGIP (HTLV-gag inde-terminate profile pattern) y es definido como un perfil de proteínas específicas donde se presentan las bandas p19, p26, p28, p32, p36 y p53 sin la presencia de la banda p24 o alguna de las glicoproteínas del gen de la envoltura (gp 46, gp 61/68). En las muestras nacionales se observó que 22 presentaron un patrón similar, sin la p24. Sin embargo, se observaron 6 muestras con patrones diversos que incluyen la p24.
Este primer análisis de muestras nacionales señala la necesidad de realizar un estudio molecular para determinar el estado real de infección por HTLV en donadores nacionales que presenten el perfil indeterminado en la técnica de WB. Esta información permitirá establecer asociaciones con casos verdaderos positivos o con reacciones inespecíficas.
Palabras clave: HTLV I / HTLV II, donantes, Western Blot, patrones indeterminados.
Abstract
Human T lymphotropic virus type I and II (HTLV I/II) are retroviruses associated with different clinical manifestations. HTLV I was the first retrovirus associated to human disease, and it is the etiological agent of two main pathologies: adult`s T-cell leukemia (ATL) and myelopathy/tropical spastic paraparesis (HAM/TSP). HTLV-II has been related to similar neurological disorders. Central America, South America and the Caribbean are areas of high prevalence.
In many countries, including Costa Rica, blood screening has been implemented to prevent retroviral blood transmission. Applying the Western Blot (WB) technique, screening for HTLV I/II in blood donors has shown incomplete antibody reactivity against viral antigens, which has been classified as an indeterminate pattern. Between december 2002 and march 2006, enzyme immunoassay (ELISA) reactive samples were reported as 39 (0,02%) positive, 254 (0,14%) indeterminate and 113 (0,06%) negative. For further study with the commercial system (HTLV I/II Blot 2.4), there were selected 42 indeterminate samples and 25 positive ones. The results for the positive group were: 15 HTLV-I, 8 HTLV-II and 2 indeterminate. In the indeterminate group we found 4 discordant results: 1 HTLV II, 1 HTLV and 2 negative samples. In this research, using national serum samples, it is weak show positive patterns can be related to indeterminate WB or to partial reactivity of HTLV II infected donors.
The most characteristic indeterminate pattern is the HTLV-I gag indeterminate (HGIP), which has been defined as a protein profile which includes p19, p26, p28, p32, p36 and p53, but excludes p24 or envelope glycoproteins (gp 46, gp 61/68). In the present study, a similar pattern was observed in 22 samples. However, there were 6 samples with patterns that include p24.
This first analysis of indeterminate patterns in national samples demonstrates the importance of molecular studies to establishing the HTLV infection status in national blood donors with this WB profile. This information will enable identify true positives cases and unspecific reactions.
Key words: HTLV I / HTLV II, blood donors, Western Blot, indeterminate patterns.
Introducción
Los virus linfotrópicos humanos tipo I y II (HTLV I/II) son retrovirus asociados a diferentes patologías. El HTLV I fue el primer retrovirus relacionado con enfermedad y ocasiona principalmente dos tipos de patologías: la leucemia o linfoma de células T del adulto (LTA) (ATL, del inglés adult T-cell leucemia) (1, 2) y la paraparesia espástica tropical (PET) (TSP del inglés tropical spastic paraparesis) (3). El HTLV-I además se ha vinculado a cuadros como uveitis, dermatitis, artritis y otros desórdenes autoinmunes (4). El HTLV-II se ha asociado a cuadros neurológicos similares a los inducidos por el tipo I, pero no se cuenta con la evidencia epidemiológica suficiente para confirmar su papel como agente etiológico (5). La distribución geográfica del HTLV es mundial, y Centroamérica, América del Sur y el Caribe se definen como áreas de alta prevalencia, con conglomerados de personas infectadas (6).
Para prevenir la transmisión de la infección por sangre de estos retrovirus se ha implementado el tamizaje de la donación sanguínea en muchos países y Costa Rica no ha sido la excepción. En todo el mundo, en donadores de sangre tamizados para HTLV I/II se ha demostrado una actividad incompleta de anticuerpos contra los antígenos virales; en la técnica de Western Blot (WB) estos patrones se definen como indeterminados (7-10). En Costa Rica entre diciembre del 2002 y diciembre del 2004 los patrones indeterminados representaron un 0,12% del total de donantes tamizados, y se obtuvo un 0,02% de positivos y un 0,06% de negativos (11).
El patrón indeterminado más común se ha definido como un perfil de proteínas específicas de grupo donde se presentan las bandas p19, p26, p28, p32, p36 y p53, sin la presencia de la banda p24 o alguna de las glicoproteínas correspondientes al gen de la envoltura (gp 46, gp 61/68) (7, 8). Este perfil se ha denominado HGIP (por sus siglas en inglés, HTLV-gag Indeterminate Profile Pattern) y se ha descrito principalmente en zonas tropicales endémicas (8, 12, 13).
En el estudio previo, utilizando un sistema de WB implementado en el laboratorio del Centro Internacional de Investigación y Adiestramiento Médico (ICMRT: International Center for Medical Research Training), no se observó una alta frecuencia de este patrón; por el contrario, se obtuvieron patrones con bandeo múltiple que presentaban la proteína 24 y/o alguna banda del gen de la envoltura (11).
En el presente trabajo se pretende obtener mayor información con respecto al patrón de bandas indeterminado observado en muestras nacionales, caracterizar muestras positivas con patrones de bandeo débil y comparar el WB implementado en el laboratorio (in house) con el sistema comercial.
Materiales y métodos
Población de estudio
La población original comprende 174.667 muestras de suero de donantes de sangre de todo el territorio nacional, que asistieron a los bancos de sangre de los laboratorios clínicos de la Caja Costarricense de Seguro Social (CCSS) entre diciembre del 2002 y marzo del 2006. Estas muestras fueron analizadas por diferentes pruebas para detectar agentes infecciosos transmitidos por transfusión sanguínea, para Virus Hepatitis C (VHC), Virus Hepatitis B (VHB), Virus Inmunodeficiencia Humana (VIH), contra el Trypanosoma cruzi (enfermedad de Chagas), contra el Treponema pallidum (sífilis) y anticuerpos tipo IgG contra los virus HTLV I/II. De esta población general se seleccionaron 42 muestras indeterminadas y 25 positivas.
Muestras
Las muestras fueron enviadas y transportadas como se describió de previo (11), y el suero fue almacenado a -20 °C. Cada muestra se descongeló para realizar la técnica de WB "in house" y WB comercial.
Western Blot
El WB "in house" se realizó como se describió anteriormente (11). Por este sistema las muestras fueron procesadas por duplicado. Según criterio del Centro de Control de Enfermedades de Atlanta de Estados Unidos (14), una muestra es negativa si no presenta bandas, positiva si reacciona contra la proteína 24 del gen Gag (p24) y con una o mas proteínas del gen de la envoltura (ENV) gp46 y/o gp 61/68; si no se cumple el criterio anterior se considera una muestra indeterminada.
Para el WB comercial se utilizó el sistema HTLV Blot 2.4, de Genelabs® Diagnostics, siguiendo las especificaciones de la casa comercial. En este sistema una muestra se considera HTLV-I positiva si reacciona con las proteínas centrales (del core) p19 con o sin p24 y con 2 proteínas de la envoltura, que son la recombinante específica para HTLV-I (rgp46-I) y la recombinante específica para HTLV I y HTLV-II, la GD21. Una muestra se considera HTLV-II positiva si reacciona con la proteína central p24 con o sin p19 y las 2 proteínas de la envoltura, la recombinante específica para el tipo II (rgp46-II) y la GD21. Finalmente, si una muestra sólo reacciona con la p19, la p24 y la GD21 se interpretan como positivos para HTLV, sin definir a cual tipo pertenece.
Resultados
Del total de donantes tamizados (174.667) se procesaron las muestras reactivas por ensayo immunoenzimático (EIA); con la prueba confirmatoria de WB se obtuvieron los siguientes resultados: 39 (0,02%) donantes positivos, 254 (0,14%) donantes indeterminados y 113 (0,06%) con resultado negativo.
A todas las muestras con resultado de EIA positivo se les realizó el WB "in house"; de las interpretadas como positivas en este sistema, a 25 que contaban con suficiente suero se les realizó el WB comercial. De estas muestras se clasificaron 15 como HTLV I, 8 como HTLV II y 2 muestras como indeterminadas. Al comparar estos resultados se observó que en el sistema "in house" los bandeos débiles, aún con las bandas de criterio diagnóstico, se relacionaron con un resultado indeterminado.
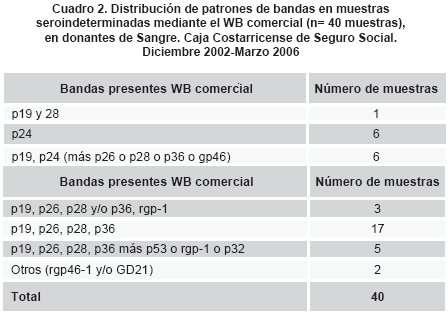
En las muestras indeterminadas se observó una amplia variedad de patrones con bandas individuales (p15, p19, p24, p28, p46, p53, p68) o patrones de dos bandas que incluyeron: p15 y p28, p19 y p28 o p32, p24 y 15 ó 10, 28, 46 ó 53. Igualmente, se obtuvieron patrones con bandeo múltiple (3 o más) (cuadro 1). De este segundo grupo se seleccionaron 42 muestras que fueron analizadas por el sistema comercial. De dichas muestras 4 no fueron concordantes y se identificaron como 1 HTLV II, 1 HTLV y 2 negativas. Las muestras restantes fueron concordantes con un patrón indeterminado. Una de las muestras indeterminadas por el sistema "in house" se negativizó en la segunda y tercera muestra en el mismo sistema, reduciendo a 3 las muestras no concordantes.
En las muestras procesadas por el sistema comercial se observó que 17 presentaron el perfil de p19, p26, p28 y p36 (figura 1) y 5 más presentaron un patrón similar. Este patrón es semejante al HGIP descrito, que incluye p19, p26, p28, p32, p36 y p53 sin la p24. Sin embargo, también se observaron 6 muestras con patrones diversos que incluyen la banda p24 (cuadro 2).
Discusión
Actualmente no se ha determinado la importancia clínica de patrones de WB indeterminados. El tamizaje de donantes nacionales ha señalado que la prevalencia de patrones indeterminados es mayor a la de muestras positivas y negativas, 0,13% vs 0,02 y 0,06%, respectivamente (11).
Conocer el significado de estos resultados indeterminados es de suma importancia para el seguimiento integral de los casos. Se ha postulado que los pacientes con perfiles indeterminados HGIP no se asocian a infección por este virus; sin embargo, diferentes estudios han demostrado que patrones indeterminados pueden presentar reacciones en cadena de la polimerasa positivas (13, 15) y en algunos casos se han relacionado con la presencia de la banda GD21 (16, 17). En este estudio se detectó una muestra indeterminada que presentó la banda GD21 (figura 1).
Por otra parte, se han propuesto diversas hipótesis para la presencia de WB indeterminados, por ejemplo, presencia de secuencias provirales (16), cargas virales bajas (18), o presencia de HTLV-defectuoso (19). Recientemente se describió el HTLV-3 que presenta homología parcial con los anteriores y podría producir reacciones cruzadas (20). En el presente estudio el sistema comercial detectó una muestra que no se pudo clasificar como HTLV I o II, solamente como HTLV. Este resultado podría estar relacionado con alguna de las causas expuestas anteriormente.
La comparación de las muestras positivas e indeterminadas entre ambos WB mostró una buena concordancia (índice Kappa: 0,8687). Las discrepancias de los resultados indeterminados se podrían explicar como: una muestra negativa asociada a un resultado inespecífico del sistema "in house"; una muestra con reactividad parcial que tampoco fue asignada en forma definitiva por el sistema comercial (HTLV) o bien, clasificada como HTLV-II, que fue detectada por las proteínas recombinantes específicas del sistema comercial.
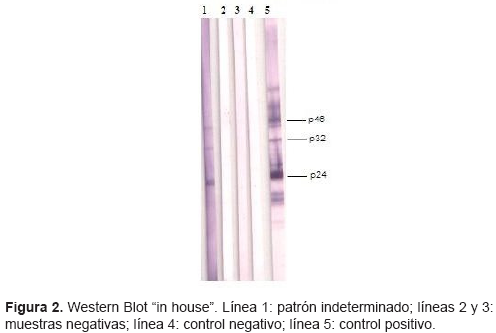
HTLV II puede presentar patrones no completos de reactividad que no permite clasificarlos por el sistema "in house" (figura 2). Este resultado concuerda con lo reportado en la literatura, donde se señala que individuos infectados por HTLV II pueden presentar reactividad indeterminada en WB o INNO-LIA (21).
A pesar de que en el sistema comercial el mayor patrón detectado (42,5%) fue semejante al HGIP, en ambos sistemas se detectaron diversidad de patrones inespecíficos y de patrones individuales que deben considerarse en el control y seguimiento de donadores indeterminados.
Los resultados serológicos indeterminados de la prueba confirmatoria de WB no constituyen un problema aislado, ya que son comunes en estos retrovirus, así como en el virus de la inmunodeficiencia humana (VIH), especialmente en poblaciones de bajo riesgo. Las causas de estas reacciones son muy diversas y pueden estar asociadas a características propias de determinadas poblaciones y zonas geográficas. Actualmente, en el país no se conoce cuáles factores virales o ambientales podrían estar relacionados.
No obstante, es bien entendido que las reacciones de muestras indeterminadas deben ser rechazadas para uso en el banco de sangre. A consecuencia de esto, el manejo del donante de sangre con un resultado indeterminado es complicado tanto para él mismo como para el personal que da la consejería, debido a que amerita un seguimiento prolongado.
El WB es necesario en el estudio de HTLV I / II; sin embargo, la alta prevalencia de indeterminados en la población nacional resalta la necesidad de un criterio diagnóstico más específico. La reacción en cadena de la polimerasa (PCR) podría ser una herramienta útil para resolver casos indeterminados en un plazo corto.
En la actualidad no se dispone de una cura para la LTM o la M/PTE, por lo que la transmisión de estas enfermedades puede acarrear costos sociales y económicos a largo plazo. Este es el primer análisis de patrones indeterminados de muestras nacionales que señala la necesidad de realizar un estudio molecular para poder determinar el estado real de infección por retrovirus en donadores nacionales que presenten patrones indeterminados, de manera que se establezcan asociaciones con casos verdaderos positivos o con reacciones inespecíficas.
Agradecimiento
Los autores agradecen al Dr. José Luis Salas Oviedo de la Dirección Desarrollo Servicios de Salud, Área de Regulación y Sistematización, Subárea de Laboratorios Clínicos-CCSS y a todos los funcionarios que conforman la Red de Laboratorios Clínicos y Bancos de Sangre. Al Señor Marvin Aguilar (ICMRT) por la asistencia técnica y al Dr. Cesar Vega de la O por la colaboración brindada.
Referencias
1. Poiesz BJ, Ruscetti FW, Gadzar AF, Bunn PA, Minna JD, Gallo RC. Detection and isolation of type c retrovirus particles from fresh and cultured lymphocytes of a patient with cutaneous T-cell lymphoma. Proc Natl Acad Sci 1980; 77:7415-7419. [ Links ]
2. Blattner WA, Takatsuki K, Gallo RC. Human T-cell leukemia-lymphoma virus and adult T-cell leukemia. JAMA 1983; 250:1074-1080. [ Links ]
3. Gessain A, Barin E, Vernant JC, et al. Antibodies to human T-lymphotropic virus type-1 in patients with tropical spastic paraparesis. Lancet 1985; ii: 407-410. [ Links ]
4. Proietti FA, Carneiro-Proietti AB, Catalan-Soares BC, Murphy EL. Global epidemiology of HTLV-1 infection and associated diseases. Oncogene 2005; 24: 6058-6068. [ Links ]
5. Feuer G, Green PL. Comparative biology of human T-cell lymphotropic virus type 1 (HTLV-1) and HTLV-2. Oncogene 2005; 24: 5996-6004. [ Links ]
6. Carneiro-Proietti AB, Catalan-Soares BC, Castro-Costa CM, et al. HTLV in the Americas: challenges and perspectives. Rev Panam Salud Públ 2006 Jan; 19: 44-53. [ Links ]
7. Mauclere P, Le Hesran JY, Mahieux R, Salla R, et al. Demographic, ethnic, and geographic differences between human T cell lymphotropic virus (HTLV) type I-seropositive carriers and persons with HTLV-I Gag-indeterminate Western Blots in Central Africa. J Infect Dis 1997 Aug; 176(2):505-9. [ Links ]
8. Rouet F, Meertens L, Courouble G, Rouet F, Hermann - Storck C, et al. Serological, epidemiological, and molecular differences between human T-cell lymphotropic virus Type 1 (HTLV-1)-seropositive healthy carriers and persons with HTLV-I Gag indeterminate Western blot patterns from the Caribbean. J Clin Microbiol 2001 Apr; 39 (4): 1247-53. [ Links ]
9. Yao K, Hisada M, Maloney E, et al. Human T lymphotropic virus types I and II western blot seroindeterminate status and its association with exposure to prototype HTLV-I. J Infect Dis 2006 Feb; 193: 427-437. [ Links ]
10. Martínez-Nieto O, Isaza Ruget M, Rangel-Espinoza N, Morales-Reyes OL. Seropreva-lencia de anticuerpos para virus linfotrópicos humanos (HTLV I/II) en donantes de sangre de una clínica de Bogotá, Colombia. 1999-2004. Rev salud pública 2007 Mayo; 9(2): 253-261. [ Links ]
11. García Z, Cortés X, Torres L, Araúz P, Pacheco E, Taylor L. Detección de anticuerpos contra los virus linfotrópicos de células T tipo I/II (HTLV I/II) como medida de seguridad sanguínea en donantes de sangre en Costa Rica. Mayo del 2002 a diciembre del 2004. Rev Costarric Cienc Med 2006 Junio; 27: 11-29. [ Links ]
12. Mahieux R, Horal P, Mauclere P, Mercereau-Puijalon O, et al. A human T-cell lymphotropic virus type 1 gag indeterminate western blot patterns in Central Africa: relationship to Plasmodium falciparum infection. J Clin Microbiol 2000 Nov; 38(11):4049-57. [ Links ]
13. Teixeira Santos TJ, de Castro Costa CM, Goubau P, Vandamme AM, et al. Western Blot seroindeterminate individuals for Human T Lymphotropic Virus 1/2 in Fortaleza (Brazil): A serological and molecular diagnostic and epidemiological Approach. Braz J Infect Dis 2003; 7(3): 202-209. [ Links ]
14. Center for Disease Control and Prevention. Recommendations for Counseling Persons Infected with HumanT-Lymphotrophic Virus, Types I and II. USA.MMWR 1993; 42/RR-9:1-13. [ Links ]
15. Leon G, Quirós AM, López JL, Hung M, Díaz AM, Goncalves J, et al. Seropositividad al virus linfotrópico de células T humanas tipos I y II en donantes del Banco Municipal de Sangre de Caracas y factores de riesgo asociados. Rev Panam Salud Públ 2003; 13: 117-123. [ Links ]
16. Mangano AM, Remesar M, del Pozo A, Sen L. Human T lymphotropic virus types I and II proviral sequences in argentinian blood donors with indeterminate western blot patters. J Med Virol 2004 Jun; 74: 323-327. [ Links ]
17. Jacob F, Santos-Fortuna E, Azevedo RS, Caterino-de-Araujo A. Serological patterns and temporal trends of HTLV1/2 infection in high risk populations attending Public Health Units in Sao Pablo, Brazil. J Clin Virol 2008 Jun; 42: 149-55. [ Links ]
18. Waziri A, Soldan S, Graf M, Nagle J, Jacobson S. Characterization and sequencing of prototypic human T-lymphotropic virus type 1 (HTLV-1) from an HTLV 1/2 seroindeterminate patient. J Virol 2000 Mar; 74: 2178-2185. [ Links ]
19. Morozov VA, Ellerbrok H, Fleisher C, Brackmann HH, Pauli G. Defective human T-Leukaemia virus type I (HTLV-1) genomes: no evidence in serologically indeterminate german blood donors but new type detected in established cell lines. J Med Virol 2002 Jan; 66: 102-6. [ Links ]
20. Calattini S, Chevalier SA, Duprez R, Bassot S, Froment A, Mahieux R, et al. Discovery of a new human T-cell lymphotrophic virus (HTLV-3) in Central Africa. Retrovirology 2005 May; 2:30. [ Links ]
21. Thorstensson R, Albert J, Andersson S. Strategies for diagnosis of HTLV-I and HTLV-II. Transfusion complications 2002 June; 42: 780-791. [ Links ]