Introducción
Los océanos representan alrededor del 71% de la superficie del planeta y los estudios han demostrado que el ambiente marino contiene gran cantidad de especies bacterianas que recientemente se están caracterizando (Kola & Masilamani, 2017). Costa Rica se ubica en una de las zonas de alta diversidad de especies a nivel mundial, por ser un corredor biológico entre el norte y sur del continente americano. Posee una superficie marina de 568 054 km2, de las cuales se han identificado cerca de 7000 especies marinas, que representan un 6.5% de las especies registradas a nivel internacional, es uno de los países con más diversidad por Km2 (Wehrtmann et al., 2009; Cortés, 2017). La costa Pacífica posee más del doble de especies marinas que las reportadas en el Caribe; sin embargo, esta estimación no comprende a la comunidad de microorganismos (Wehrtmann et al., 2009; Alvarado, Herrera, Corrales, Asch, & Paaby, 2011; Cortés, 2012, Cortés, 2016a, Cortés, 2016b). La mayoría de las investigaciones de biodiversidad se han enfocado en grandes mamíferos marinos, vertebrados como peces y algunos invertebrados como corales entre otros (Wehrtmann & Cortés, 2009). Sin embargo, a pesar de la alta diversidad de ecosistemas marinos, en el país existen vacíos en el tema de conservación a nivel de la comunidad microbiana y fitoplanctónica, estos deben ser abordados para asegurar la conservación del patrimonio natural y genético.
Dentro de las bacterias marinas existe un grupo bacterias luminiscentes, capaces de transformar la energía química en energía lumínica mediante un proceso bioquímico (Kahlke & Umbers, 2016). De 700 géneros de organismos marinos que producen bioluminiscencia, el 80% corresponden a relaciones simbióticas con bacterias y su distribución geográfica abarca desde los polos hasta aguas tropicales. Las bacterias se han reportado como organismos de vida libre, asociados a peces y cefalópodos o formando relaciones simbióticas en órganos lumínicos de organismos como el calamar Euprymna scolopes (Kola & Masilamani, 2017)y en peces como Photoblepharon sp. y Leiognathus sp.,y en medusascomo Atolla sp. (Witze, 2018). Los dinoflagelados son microalgas pertenecientes al grupo del fitoplancton, y junto a las diatomeas son uno de los grupos más importantes en el ecosistema debido a la producción de potentes toxinas. Además, estos organismos son los mayores productores de floraciones algales nocivas, siendo algunos de estos luminiscentes, incluso se hace referencia de un dinoflagelado bioluminiscente de aguas marinas tropicales (Noctiluca miliaris) (Villalobos-Solé, 1967).
En el Parque Nacional Isla del Coco (PNIC), durante una expedición científica, se analizaron muestras de fito y zooplancton, logrando reportar 75 especies de bacterias y más de 100 especies de microalgas pertenecientes al fitoplancton (Cortés-Núñez, Acuña-González, Lizano-Rodríguez, Morales-Ramírez, & Alfaro-Martínez, 2009). En Costa Rica se han realizado estudios metagenómicos dirigidos a bacterias marinas, reportándose en la columna de agua los géneros Prochlorococcus, Synechococcus, Pelagibacter, Shewanella, y Burkholderia cerca de la Isla del Coco, Roca Sucia, a una profundidad de 30 m (Rusch et al., 2007). La primera referencia sobre bacterias luminiscentes aisladas del ecosistema marino costarricense fue presentada en el VII Congreso Nacional de Biología por Vega-Corrales, Marín-Vindas y Rojas-Alfaro (2014), quienes realizaron el primer reporte nacional sobre el aislamiento de bacterias luminiscentes del Golfo de Nicoya. Destacan otros reportes como los de Marín-Vindas Vega-Corrales, Umaña-Castro y Rojas-Alfaro (2015), Marín-Vindas Vega-Corrales, Umaña-Castro y Rojas-Alfaro(2017), Marín-Vindas, Vega-Corrales y Rojas-Alfaro (2015) y Rojas-Alfaro (2016) indicando la presencia de bacterias marinas luminiscentes de los géneros Vibrio y Photobacterium en la costa del Pacífico costarricense. En Costa Rica desde 1995 se han realizado estudios sobre dinoflagelados dirigidos hacia la identificación taxonómica y en la amenaza que representan debido a la producción de las floraciones algales en las áreas marinas (Víquez & Hargraves, 1995; Vargas-Montero & Freer, 2003; Vargas-Montero, Freer, Guzmán, & Vargas, 2008). Actualmente, no hay referencias sobre dinoflagelados luminiscentes encontrados en el medio marino costarricense.
Por tanto, esta investigación tuvo como objetivo aislar e identificar por primera vez bacterias y dinoflagelados luminiscentes de agua marina superficial entre los 3 a 30 m de profundidad del Parque Nacional Isla del Coco, Costa Rica.
Materiales y métodos
Área de estudio:Para bacterias bioluminiscentes en junio del 2017 se recolectaron muestras de agua marina superficial y mediante buceo de hasta 30 m de 13 zonas del PNIC (Fig. 1). Para las colectas de agua se utilizaron botellas ámbar estériles de 100 mL. Seguidamente, las muestras de agua se almacenaron y transportaron en hielo en un lapso menor a 4 h hasta la Estación Bahía Wafer, PNIC, Costa Rica. Las muestras de fitoplancton se recolectaron en 8 zonas del PNIC, desde la superficie hasta los 30 metros de profundidad utilizando botellas Niskin de 1 L de capacidad, así como realizando buceos sobre parches de coral utilizando una red de 20 um de los de malla, fijándose inmediatamente con glutraldehído al 2% en la estación de Bahía Wafer (Vargas-Montero et al., 2008), luego fueron transportadas al Laboratorio de Fitoplancton Marino y Costero del Centro de Investigación en Estructuras Microscópicas (CIEMic), de la Universidad de Costa Rica (Tabla 1).
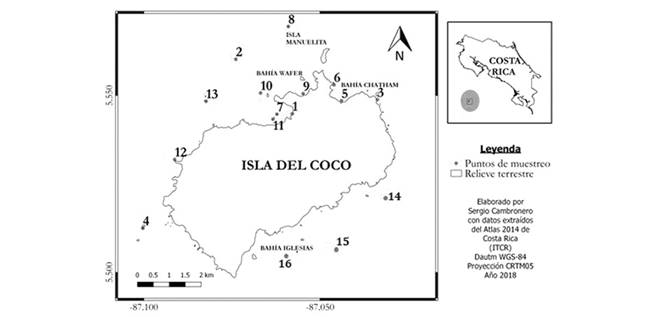
Fig. 1 Fig. 1 Mapa de la distribución de las zonas de muestreo de aislados bacterianosluminiscentes de la Isla del Coco, Costa Rica. Muestras superficiales: (1) Bahía Wafer, (2) Roca Vikinga, (3) Punta Ulloa, (5) Bahía Chatam, (6) Fondeo del barco Sea Hunter, (7) fondeo del barco Okeanos Aggressor II, (9) Bahía Weston, (10) Punta Presidio, (11) Roca Gissler. Muestras obtenidas por buceo: (4) Roca 2 amigos (20 m), (8) Manuelita profundo (20 m), (12) Punta María (20 m) y (13) Roca Sucia (30 m). Zonas de muestreo de dinoflagelados marinos luminiscentes, muestras superficiales: (4) Roca 2 amigos, (11) Roca Gissler y (12) Punta María. Muestras obtenidas por buceo: (1) Coral de Bahía Wafer (3 m), (5) Coral de Bahía Chatam (5 m), (14) Cabo Atrevido (5 m), (15) Bajo Alcyone (30 m) and (16) Bahía Iglesias (20 m). Entre paréntesis la profundidad en metros en que se recolectó la muestra. Map of the distribution of the sampling zones of luminescent bacteria from Cocos Island, Costa Rica. Surface samples:(1) Wafer Bay, (2) Viking Rock, (3) Ulloa Point, (5) Chatam Bay, (6) Anchorage of the Sea Hunter ship, (7) Anchorage of the Okeanos Agresor ship, (9) Weston Bay, (10) Presidio Point, (11) Gissler Rock. Samples obtained by diving: (4) 2 friends Rock (20 m), (8) Manuelita deep (20 m), (12) María Point (20 m) and (13) Dirty Rock (30 m). Sampling zones of marine bioluminescent dinoflagenates, Surface samples: (4) Two friends Rock, (11) Gissler Rock and (12) María Point. Diving samples: (1) Coral of Wafer Bay (3 m), (5) Coral of Chatam Bay (5 m), (14) Atrevido Cape (5 m), (15) Bajo Alcyone (30m), (16) Churches Bay (20m). In parentheses the depth in meters in which the sample was collected.
TABLA 1 TABLE 1 Sitos de muestreo de aislados bacterianos y colecta de fitoplancton en la Isla del Coco, Costa Rica Sampling sites for bacterial isolates and phytoplanckton samples from Isla del Coco, Costa Rica
| Sitios de muestreo | Ubicación GPS | |
| N | W | |
| Muestras a nivel Superficial (1 m de profundidad) | ||
| Bahía Wafer | 05°33’12’’ | 87’02’28’’ |
| Roca Vikinga | 05°32’09’’ | 87°03’86’’ |
| Punta Ulloa | 05°33’10’’ | 87°02’21’’ |
| Bahía Chatham | 05°33’01’’ | 87’02’30’’ |
| Bahía Weston | 05°33’03’’ | 87°03’02’’ |
| Punta Presidio | 05°33’12’’ | 82’02’55’’ |
| Roca Gissler | 05°32’06’’ | 87°03’07’’ |
| Fondeo Sea Hunter | 05°33’09’’ | 87’02’24’’ |
| Fondeo Okeanos Aggressor II | 05°’33’08’’ | 87’02’36’’ |
| Muestras obtenidas por buceo | ||
| Manuelita profundo (20 m) | 05°33’07’’ | 87°02’09’’ |
| Roca 2 amigos grande (20 m) | 05°30’07’’ | 87°05’10’’ |
| Punta María (20 m) | 05°31’09’’ | 87°05’06’’ |
| Roca Sucia (30 m) | 05°32’09’’ | 87°04’09’’ |
| Cabo atrevido (5m) | 05°31’99’’ | 87°01’55’’ |
| Bajo Alcyone (30 m) | 05°30’99’’ | 87°01’55’’ |
| Bahía Iglesias (30 m) | 05°30’64’’ | 87°03’92’’ |
| Coral de Bahía Wafer (3 m) | 05°33’12’’ | 87’02’28’’ |
| Coral de Bahía Chatham (5 m) | 05°33’01’’ | 87’02’30’’ |
* Entre paréntesis la profundidad en metros en que se recolectó la muestra.
Procesamiento de la muestray análisis microbiológico:Las muestras de agua marina colectadas fueron procesadas y analizadas en un cuarto adaptado para ensayos microbiológicos en la Estación Bahía Wafer, PNIC. La metodología utilizada fue la propuesta por Bagordo et al. (2012), con las siguientes modificaciones: se tomaron alícuotas de 100 mL de cada muestra y se filtraron a través de filtros de nitrato de celulosa de 0.45 μm de tamaño de poro y de 47 mm de diámetro (MiliPore®). Seguidamente, los filtros se colocaron en placas Petri con agar Zobell (Khambholja & Kalia, 2016) y se incubaron en oscuridad a temperatura ambiente local aproximada de 26-27 °C durante 24 h. Posterior al período de incubación, se seleccionaron las colonias con una luminiscencia basal de 100 %, de forma visual en la oscuridad.
Adicionalmente, se realizaron tinciones de Gram (Bagordo, et al., 2012) y posteriormente los aislados fueron identificados. Se realizó el antibiograma mediante el sistema automatizado Vitek 2 Compact (bioMerieux, Francia). Y se determinó la actividad hemolítica mediante la inoculación por estría a cultivos frescos (18 a 24 h) de agar sangre (10 %) de cada aislamiento luminiscente. Las placas fueron incubadas a 30 oC durante 24 h y fueron almacenadas en caldo BHI (Caldo infusión cerebro corazón) (OXOID®) con 20 % glicerol a -80 °C(Chunga, 2018) en el Laboratorio de Bacteriología Médica de la Facultad de Microbiología, Universidad de Costa Rica, San José, Costa Rica. La actividad hemolítica se determinó por la presencia de halos (zonas claras) según tipo alfa, beta o gamma hemólisis evidenciada alrededor de la estría (Martins, 2010).
Procesamiento de la muestra de fitoplancton: Las muestras de fitoplancton se sedimentaron y se procesaron en el laboratorio para ser analizadas en un microscopio de luz invertida, marca Olympus® equipado con una cámara DP-70. Las muestras más representativas se procesaron para ser fotografiadas utilizando un microscopio electrónico de barrido marca Hitachi, modelo S-570. El procesamiento realizado consistió en extraer aproximadamente 1 mL de la muestra sedimentada, la cual fue procesada siguiendo la metodología propuesta por Watson, Mckee & Merrel (1980) para la digestión de membranas, utilizando un detergente no iónico (Tritón X-100®). La separación de la muestra se llevó a cabo a través de gradientes de sucrosa, lo que permitió aislar los dinoflagelados de los residuos presentes en la muestra. Las muestras procesadas se fijaron en una membrana de Poli-L-Lisina de acuerdo a Mazia, Schatten & Sale (1975) y fueron cubiertas con una fina capa de oro-paladio mediante el cobertor iónico Geiko IB3, para facilitar su visualización en el microscopio de barrido del CIEMic. Una vez fotografiadas se procedió a identificar las especies con la literatura más actualizada.
Resultados
Se obtuvieron siete aislados de bacterias luminiscentes de agua marina: seis a nivel superficial y una mediante buceo de roca Dos Amigos (20 m de profundidad) de la Isla del Coco, Costa Rica (Fig. 2, Tabla 1, Tabla 2). En cuanto a la morfología macroscópica se observaron colonias blancas translúcidas pequeñas (<10 mm) redondas con borde liso y microscópicamente todas se evidenciaron como bacilo Gram negativo (BGN).

Fig. 2 Fig. 2 Fotografía de bacterias luminiscentes cultivadas en agar Zobell aisladas de la Isla del Coco, Costa Rica, observadas en oscuridad total y sin exposición de ningún tipo de fuente de luz. Fotografía por: Guillermo Blanco Segura. Photograph of luminescent bacteria cultured on Zobell agar isolated from Cocos Island, Costa Rica, observed in total darkness and without exposure of any type of light source. Photography by: Guillermo Blanco Segura.
TABLA 2 TABLE 2 Identificación bioquímica mediante Vitek 2 Compact (bioMerieux®, Francia) de las bacterias luminiscentes aisladas de la Isla del Coco, Costa Rica Biochemical identification by Vitek 2 Compact (bioMerieux®, France) of luminescent bacteria isolated from Cocos Island, Costa Rica
| Código cepa | Origen de la cepa | Identificación Vitek 2 | Nivel de confianza (%) |
| CL 1 | Sitio 1: Bahía Wafer | Vibrio alginolyticus | 98 |
| CL 2 | Sitio 2: Roca Vikinga | Vibrio parahaemolyticus | 96 |
| CL 3 | Sitio 3: Punta Ulloa | Vibrio alginolyticus | 99 |
| CL 4 | Sitio 4: Roca 2 Amigos | Vibrio parahaemolyticus | 97 |
| CL 5 | Sitio 1: Bahía Wafer | Vibrio alginolyticus | 97 |
| CL 6 | Sitio 6: Fondeo Sea Hunter | Vibrio parahaemolyticus | 99 |
| CL 7 | Sitio 7:Fondeo Okeanos Aggressor II | Vibrio parahaemolyticus | 99 |
El análisis bioquímico mediante Vitek 2 Compact (bioMerieux®, Francia) logró ubicar taxonómicamente las aislados bacterianos luminiscentes de la Isla del Coco, Costa Rica. Estas se agruparon en el género Vibrio, se identificaron dos especies: V. alginolyticus y V. parahaemolyticus. Estos resultados están respaldados por un nivel de confianza (>96 %) (Tabla 2). Los aislados fueron 100 % sensibles a los antibióticos ensayados, con excepción de la ampicilina, donde la sensibilidad fue de 57 % (4/7 aislados) (Tabla 3).
TABLA 3 TABLE 3 Antibiograma mediante Vitek 2 Compact (bioMerieux®, Francia) de las bacterias luminiscentes aisladas de la Isla del Coco, Costa Rica. CMI: Concentración mínima inhibitoria parcial (µg / ml). Interpretación: S (susceptible) y R (resistente). BLEE: betalactamasa de espectro extendido Antibiogram using Vitek 2 Compact (bioMerieux® , France) of luminescent bacteria isolated fromCocos Island Costa Rica. MIC: Minimum partial inhibitory concentration (μg / ml). Interpretation: S (susceptible) and R (resistant). ESBL: extended-spectrum beta-lactamase
| Antibiótico/Cepa | CL 1 | CL 2 | CL 3 | CL 4 | CL 5 | CL 6 | CL 7 | |||||||
| Concentración e interpretación | CMI | S/R | CMI | S/R | CMI | S/R | CMI | S/R | CMI | S/R | CMI | S/R | CMI | S/R |
| BLEE | - | - | - | - | - | - | - | - | - | - | - | - | - | - |
| Ampicilina | £2 | S | £2 | S | ³ 32 | R | ³ 32 | R | ³ 32 | R | ³ 32 | R | £2 | S |
| Ampicilina/Sulbactam | £2 | S | £2 | S | £2 | S | £2 | S | £2 | S | £2 | S | £2 | S |
| Piperacilina/ Tazobactam | £4 | S | - | - | £4 | S | - | - | £4 | S | £2 | S | £2 | S |
| Ceftazidima | £1 | S | £1 | S | £1 | S | £1 | S | £1 | S | £1 | S | £1 | S |
| Cefepima | - | - | - | - | - | - | - | - | - | - | - | - | - | - |
| Imipenem | £0.25 | S | £0.25 | S | £0.25 | S | £0.25 | S | £0.25 | S | £0.25 | S | £0.25 | S |
| Meroperem | £0.25 | S | £0.25 | S | £0.25 | S | £0.25 | S | £0.25 | S | £0.25 | S | £0.25 | S |
| Amicacina | £2 | S | £2 | S | £2 | S | £2 | S | £2 | S | £2 | S | £2 | S |
| Gentamicina | £1 | S | £1 | S | £1 | S | £1 | S | £1 | S | £1 | S | £1 | S |
| Ácidonalidíxico | £4 | S | £2 | S | £2 | S | £2 | S | £2 | S | £2 | S | £2 | S |
| Ciprofloxacino | £0.25 | S | £0.25 | S | £0.25 | S | £0.25 | S | £0.25 | S | £0.25 | S | £0.25 | S |
| Nitrofurantoína | £16 | S | £16 | S | £16 | S | £16 | S | £16 | S | £16 | S | £16 | S |
| Trimetoprima/Sulfametoxazol | £20 | S | £20 | S | £20 | S | £20 | S | £20 | S | £20 | S | £20 | S |
En cuanto a la actividad hemolítica la totalidad de los aislados bacterianos luminiscentes fueron positivos, se evidenciaron halos de hemólisis de 7 hasta 10 mm, en su mayoría los halos que rodearon a las colonias fueron totalmente transparentes, debido a la destrucción total de la membrana del eritrocito, característico de hemólisis completa (tipo beta), a diferencia de CL 3 que mostró una hemólisis parcial (tipo alfa) es decir la zona de crecimiento apareció rodeado de un halo de color verdoso producto de la lisis parcial del glóbulo rojo (Tabla 4).
TABLA 4 TABLE 4 Observaciones de la actividad hemolítica realizadas en aislados luminiscentes aisladas de la Isla del Coco, Costa Rica Observations of hemolytic activity performed on luminescent strains isolated from Cocos Island, Costa Rica
| Código de cepa | Actividad hemolítica (mm) |
| CL 1 | 7 |
| CL 2 | 10 |
| CL 3 | 7* |
| CL 4 | 10 |
| CL 5 | 9 |
| CL 6 | 10 |
| CL 7 | 16 |
* Hemólisis parcial observada cuando la zona de crecimiento aparece rodeada de un halo de color verdoso mientras que la total es un halo totalmente transparente (Martins, 2010).
En la Isla del Coco se encontraron varias familias de dinoflagelados productoras de bioluminiscencia (Fig. 3), observándose diferentes especies luminiscentes de los géneros Ornithocercus perteneciente al orden Dinophysiales, a la familia Dinophyceae y el género Ceratocorys perteneciente al orden Gonyaulacales, a la familia Ceratocoryaceae, esta última especie distinguida por no poseer cloroplastos, son heterotróficos, con la capacidad de mantener simbiontes fotosintéticos ubicados en su parte apical. Las especies encontradas fueron Ornithocercussteinii, Ornithocercus magnificus, Cerathocorysarmata y Cerathocorys horrida. El género Ornithocercus fue el más abundante en las muestras observadas.
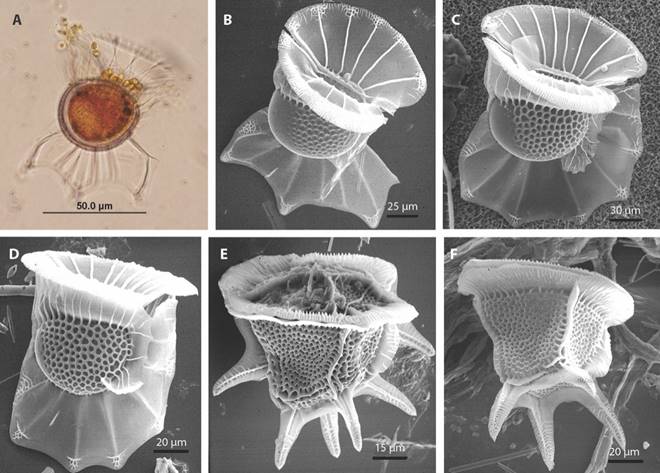
Fig. 3 Fig. 3 Especies de dinoflagelados marinos luminiscentes observados en las muestras colectadas alrededor de la Isla del Coco. (A-B) Ornithocercus magnificus, (C-D) Ornithocercus steiniiy (E-F) Ceratocorys horrida tomados con el microscopio electrónico de barrido. Species of bioluminescent marine dinoflagellates observed in samples collected around Cocos Island (A-B) Ornithocercus magnificus, (C-D) Ornithocercus steinii and (E-F) Ceratocorys horrida pictures by scanning electron microscopy.
Discusión
Estudios previos referentes al reporte, aislamiento y caracterización de bacterias luminiscentes en aguas superficiales marinas de los géneros Vibrio y Photobacterium en la costa del Pacífico (Golfo de Nicoya) costarricense, son los presentados por Rojas-Alfaro, (2016) y Marín-Vindas et al. (2017). Sin embargo, nuestros hallazgos muestran por primera vez el aislamiento e identificación bioquímica de 7 aislados bacterianos luminiscentes de agua marina de la Isla del Coco
La caracterización bioquímica de los aislados luminiscentes mediante Vitek 2 mostró un alto nivel de confianza permitiendo la identificación bacteriana de las muestras ambientales tal y como lo confirman estudios realizados en cultivos, ecosistemas dulceacuícolas, marinos y muestras ambientales de reptiles silvestres (Romeu et al., 2010; Cardak, Özbek, & Kebapçioğlu, 2015; Artavia-León et al., 2017). La identificación bioquímica indica que los aislados luminiscentes de este estudio se clasifican en el género Vibrio sp.,reportado dentro del grupo de las bacterias luminiscentes (Bagordo, et al., 2012; Yaser et al., 2014; Gómezet al., 2017).
Las aislados de V. alginolyticus y V. parahaemolyticus, no pertenecen al clado Harveyi, el cual es un complejo de bacterias que hasta el momento comprende 12 especies (V. rotiferianus, V. azureus, V. sagamiensis, V. jasicida, V. natriegens, V. mytili, V. harveyi, V. campbellii, V. owensii, V. rotiferianus,V. jasicida y V. hyugaensis). La complejidad de este grupo se debe a que los fenotipos y genotipos de esas especies son muy similares entre sí, por lo que su identificación por métodos bioquímicos y moleculares es compleja (Ke et al., 2018). Lo anterior evidencia que es necesaria una caracterizaciónbioquímica y molecular de los aislamientos obtenidos en este estudio para confirmar la identidad de los aislados luminiscentes recuperados de la Isla del Coco.
La resistencia de las bacterias es un fenómeno natural en función de la evolución, adaptación y selección de las especies (Elmahdi, DaSilva, & Parveen, 2016). La introducción de fármacos en ecosistemas acuáticos ha provocado un gran efecto secundario en el ambiente, la propagación de genes de resistencia a antibióticos (Song et al., 2016). El alto porcentaje de resistencia a la ampicilina (57%) es consistente como lo reportado por (Elmahdi et al., 2016) donde indica que V. alginolyticus y V. parahaemolyticus mostraron resistencia a este antibiótico, además la ampicilina forma parte de la lista de antibióticos que las bacterias del género Vibrio de origen marino muestran resistencia (Lee et al.,2018).
Una parte importante de la dispersión y evolución de las bacterias resistentes a los antimicrobianos depende del agua. En ecosistemas acuáticos las bacterias de diferentes orígenes (animal, humana y ambiental) son capaces de mezclarse y desarrollar mecanismos de resistencia como consecuencia de intercambios promiscuos de elementos genéticos móviles o de la recombinación de genes Asimismo, los antimicrobianos y metales pesados son liberados en el agua y sus residuos pueden ejercer presiones selectivas en comunidades acuáticas, resultando en resistencia a los agentes antimicrobianos. La resistencia no solo se adquiere por exposición al compuesto, sino también a través de mecanismos de defensa propios de la bacteria, como la bomba de flujo que expulsa la sustancia extraña, o bien la resistencia adquirida por medio de plásmidos y de betalactamasas de amplio espectro (enzimas bacterianas que hidrolizan y generan resistencia a los antibióticos de tipo β-lactámicos) (Lee et al.,2018).
El alto porcentaje de sensibilidad para los 12 antibióticos con la excepción de las aislados CL 3, CL 4, CL 5 y CL 6 que fueron resistentes a la ampicilina (Tabla 3), coincide con lo reportado por Elmahdi et al. (2016) y por Lee et al.(2018), quienes afirman que V. alginolyticus y V. parahaemolyticus y otras bacterias del género Vibrio aislados del medio marino evidenciaron sensibilidad ante dichos antibióticos.
La susceptibilidad de las demás aislados puede atribuirse a que la ampicilina es un antibiótico de tipo β-Lactámico de amplio espectro con un efecto bactericida lento, cuyo modo de acción es la inhibición de la transpeptidación, la última fase de la síntesis de la pared celular, causando un efecto letal en la bacteria (Dörr et al., 2016). Con respecto al resto de antibióticos ensayados, la alta sensibilidad es compatible con la baja exposición a drogas de uso restringido al ambiente hospitalario, de manera consistente con otros estudios similares. La determinación de la actividad hemolítica de bacterias luminiscentes del género Vibrio obtenida en este estudio (Tabla 4) concuerda con lo reportado (Cai & Zhang, 2018), indicando que uno de los efectos de la infección causada por estos microorganismos es la hemólisis en animales marinos como peces, camarones e incluso en bivalvos (Silva et al., 2018).
Las aguas alrededor de la Isla del Coco presentan el fenómeno de la bioluminiscencia, que puede ser observado por las noches, en gran parte debido a la presencia de los géneros de dinoflagelados Ornithocercus y Ceratocorys, que siempre estuvieron presentes en las muestras. Muchas de las especies observadas nunca se han reportado en aguas costeras de Costa Rica, ya que esta isla es meramente oceánica y recibe la influencia de las aguas provenientes del hemisferio sur, por lo que la mayoría de los organismos encontrados son meramente oceánicos (Vargas-Montero, Morales, &Cortés, 2012). La presencia de especies de dinoflagelados luminiscentes en las aguas alrededor de la Isla del Coco es un fenómeno que se observa en todas las épocas del año, y las especies pueden variar dependiendo de la disponibilidad de nutrimentos y de las condiciones oceanográficas, lo que refleja su estado o actividad metabólica (Sweeney, 1987). Este fenómeno se mantiene tanto con la estimulación química de los microorganismos como al estimular mecánicamente el agua, lo que aumenta aún más su visibilidad a diferentes profundidades. Estudios recientes, han demostrado que la bioluminiscencia es un factor muy importante en la determinación de la presencia de dinoflagelados tóxicos en el agua y que su actividad además de ser proporcional al número de células puede variar de acuerdo con las condiciones fisiológicas del organismo (Uribe & Montecino, 2007).
Estudios de monitoreo de luminiscencia acuática tendrían una afectación social-cultural de forma directa con los pobladores de las zonas costeras del país, ya que actualmente existen varias agencias turísticas que operan visitas a sitios de bioluminiscencia reportadas en el todo el Pacífico de Costa Rica, siendo esta una alternativa de turismo rural comunitario en miras de fortalecimiento en cuanto a capacitación y educación ambiental. En conclusión, este trabajo expone el primer registro de aislamiento y caracterización bioquímica automatizada de bacterias luminiscentes de agua marina superficial (profundidad: 1 m) y mediante buceo (profundidad: 20 m) obtenidas de la Isla del Coco, Costa Rica. Además de la relevancia en la ampliación de las zonas de estudio, aislamiento, caracterización bioquímica y molecular con el fin de explorar la diversidad que presentan los microorganismos luminiscentes en ambientes acuáticos de Costa Rica. La gran biodiversidad de especies de fitoplancton marino que se presentan en la isla, aunada a la abundancia de dinoflagelados sobre los parches de coral en las diferentes bahías, evidencian además de la utilización de mecanismos de defensa, que su población es abundante y está en crecimiento exponencial, generando un espectáculo visual que podría utilizarse para determinar cuáles especies potencialmente productoras de floraciones algales se encuentran presentes en el agua.
Declaración de ética: los autores declaran que todos están de acuerdo con esta publicación y que han hecho aportes que justifican su autoría; que no hay conflicto de interés de ningún tipo; y que han cumplido con todos los requisitos y procedimientos éticos y legales pertinentes. Todas las fuentes de financiamiento se detallan plena y claramente en la sección de agradecimientos. El respectivo documento legal firmado se encuentra en los archivos de la revista.












 uBio
uBio 

