Después de las gramíneas, las leguminosas son consideradas como la segunda familia de plantas en importancia económica. Esto debido al número de especies que proveen alimento para la población humana, forraje para el ganado, leña, diversos extractos o compuestos usados en la industria y a que ecológicamente incluyen una gran diversidad de especies y formas de vida (Lewis, 2005). Las leguminosas ocupan varios hábitats pero son particularmente dominantes en el bosque tropical estacionalmente seco (Gillespie, Grijalva, & Farris, 2000; Jacobs, 2004). Algunas de ellas tienen la capacidad de fijar N a través de una interacción con bacterias del género Rhizobium, lo que les permite influir en la conformación de las comunidades vegetales y contribuir en la restauración de suelos degradados (Gei, 2014; Menge & Chazdon, 2016).
Varias especies de leguminosas maderables del trópico americano se utilizan en plantaciones forestales debido a la alta densidad y coloración de su madera, resistencia a plagas y altas tasas de crecimiento (Piotto, Víquez, Montagnini, & Kanninen, 2004). Sin embargo, existe poca información sobre los requerimientos nutricionales de las especies más utilizadas y si esto es afectado por su capacidad de fijar nitrógeno, su tasa de crecimiento o su tolerancia a la sombra. En el presente estudio se analizan los requerimientos nutricionales de las especies cocobolo (Dalbergia retusa, subfamilia Faboideae, fijadora de N y crecimiento lento), guanacaste (Enterolobium cyclocarpum, subfamilia Mimosoideae, fijadora de N y crecimiento rápido), guapinol (Hymenaea courbaril, subfamilia Caesalpiniodeae, no fijadora y de crecimiento lento) y gallinazo (Schizolobium parahyba, subfamilia Caesalpiniodeae, no fijadora y de crecimiento rápido). Estas especies son de uso común en plantaciones para producción de madera y pueden clasificarse en pares de acuerdo a la capacidad de fijar nitrógeno y a su tasa de crecimiento (Cuadro 1).
Cuadro 1: Especies estudiadas, distribución geográfica y altitudinal, tolerancias de temperatura y precipitación, datos ecológicos y estado de conservación. Table 1: The studied species, geographical and elevation distribution, the tolerance range of temperature and precipitation, ecological data and conservation status
| Especie | Distribución geográfica | Distribución altitudinal msnm | Rango de precipitación media anual mm/año | Rango de temperatura media anual ºC | Datos ecológicos / Sucesión | Estado Conservación, UICN | Referencias |
| Dalbergia retusa Hemsl. | SE México a Panamá | 50-300 | 1 000-2 800 | 22-28 | Caducifolia; resistente al fuego; habita suelos rocosos hasta profundos, relativamente fértiles, en pendientes menores al 15 %. Es una especie de sucesión tardía con crecimiento lento. Incremento medio anual a los 10 años de 1.1 cm/año. | Vulnerable | Andrade, Brook, & Ibrahim, 2008; Jiménez, Rojas, Rojas & Rodríguez, 2011; Corrales, 2012 |
| Enterolobium cyclocarpum (Jacq.) Griseb | México hasta Brasil y las Antillas | 50-1 200 | 700-3 200 | 20-28 | Caducifolia; resistente al fuego; Crece en áreas perturbadas, remanente en bosques maduros, orillas de ríos. Es pionera de crecimiento rápido aunque persistente en bosques de sucesión avanzada. Se reporta un incremento anual de 1.2-1.8 cm/año | Preocupación mínima | Czarnowski, 2002; Ávila et al., 2010; Jiménez et al., 2011; Gei & Powers, 2013; 2014; Gei, 2014 |
| Hymenaea courbaril L. | México hasta Argentina | 0-1 300 | 800-3 000 | 20-28 | Sempervirente o caducifolia; de sucesión secundaria tardía; en terrenos con alta pendiente y suelos Oxisoles arcillosos. Frecuentemente en bancos rivereños, bien drenados, con pH de cinco a siete de ácido a neutro. EL sombreo afecta la sobrevivencia y el crecimiento inicial. Se han reportado un incremento medio de 0.57 cm/año. | Preocupación mínima | Jiménez et al. 2011; López, Villalba & M. Peña-Claros, 2012 |
| Schizolobium parahyba (Vell.) S.F. Blake | México hasta Bolivia | 0-650 (2 000) | 1 100-4 000 | 18-27, tolera heladas cortas de -2 ºC sin sufrir daños severos | Caducifolia a semi-caducifolia; resistente a sequías; pionera de vida corta, heliófila, de rápido crecimiento (2.4-4.5 cm/año). Habita bosques estacionales y húmedos con suelos arcillosos, fértiles y sujetos a compactación o en suelos de fertilidad baja con bajos niveles de pH (3.7-5.5), K y P. La plántula no telera el anegamiento, por lo que es poco frecuente en bosques ribereños inundables con baja capacidad de intercambio de cationes y niveles de saturación de Al entre 70-80 %. | Preocupación mínima | Cordero & Boshier, 2003; Piotto, Víquez, Montagnini & Kanninen, 2004; Locatelli, Melo, de Lima & Vieira, 2007 |
Los nutrimentos cumplen un papel esencial en la fisiología vegetal y cuando uno de ellos no se encuentra en las cantidades satisfactorias, su deficiencia en los tejidos promueve cambios en el metabolismo de la planta (Marschner, 1995). En su mayoría los elementos esenciales requeridos por las plantas se absorben vía raíces asociadas a micorrizas, unos en cantidades grandes a moderadas, llamados macronutrimentos (incluyendo los mesonutrimentos) como N, P, K y Ca, Mg y S. Un segundo grupo que se absorben en cantidades pequeñas y se conocen como micronutrimentos o elementos traza, entre ellos Fe, Si, Cu, Cl, Mn, B, Zn y Mo (Marschner, 1995).
Pocos valores de concentración de nutrimentos han sido reportados para hojas y madera de E. cyclocarpum y de S. parahyba (Cuadro 2). Para la especie H. courbaril, creciendo bajo condiciones de invernadero, se considera que las plántulas tienen un bajo requerimiento de P pues no responden a la adición del elemento (Resende, Neto, Muniz, Curi, & Faquin, 1999; Resende, Neto, & Curi, 2005) ni a la aplicación de K como fertilizante (Da Silva, Neto, Curi, & do Vale, 1997). Para Dalbergia retusa y Hymenaea courbaril, la información sobre los requerimientos nutricionales es prácticamente nula. En leguminosas y otras plantas se ha demostrado que la cantidad y proporción de nutrimentos en el follaje se relaciona con su disponibilidad en el suelo (Chimphango, Potgieter, & Cramer, 2015) por lo que el contenido foliar de nutrimentos se puede utilizar como un indicador de la disponibilidad de elementos que deben tener los suelos para su crecimiento óptimo. Este conocimiento podría ayudar a mejorar los proyectos de producción de especies forestales o aquellos de restauración ecológica.
Cuadro 2: Concentración de nutrimentos en distintos componentes de la planta reportados por otros autores para las especies estudiadas. Table 2: Nutrients concentration in several parts of the plant reported by other authors for the four tree species studied
| Elementos | Unidades | E. cyclocarpum | S. parahyba | |||
| Hojas | Madera | Biomasa aérea | Hojas | Hojarasca | ||
| N | % | 0.33 | 3.1 | 2.61 | 1.65 | |
| P | 0.21 | 0.01 | 0.31 | 0.16 | 0.12 | |
| K | 1.18 | 0.44 | 1.11 | 0.18 | 0.82 | |
| Ca | 0.66 | 0.21 | 0.68 | 2.14 | 1.99 | |
| Mg | 0.71 | 0.06 | 0.22 | 0.21 | 0.18 | |
| S | 0.04 | 0.135 | 0.18 | 0.11 | ||
| B | mg kg -1 | 27 | 4 | 46 | ||
| Fe | 206 | 206 | ||||
| Cu | 6 | 8 | ||||
| Zn | 16 | 35 | ||||
| Mn | 4 | 45 | ||||
| Referencias | 1 | 2 | 3 | 4 | 4 | |
1: Hunter & Stewart, 1993; 2: Tenorio, Moya, Salas & Berrocal, 2016; 3: AMATA S/A, 2009; 4: Corrêa, 2014.
Para conocer los requerimientos nutricionales de las plantas se ha utilizado el análisis de la concentración de nutrimentos en las hojas, método que se emplea con frecuencia debido a que es preciso y rápido de hacer. Además, las hojas son el punto focal donde se llevan a cabo una gran cantidad de funciones en la planta y son un indicador relativamente sensible a cambios nutricionales (Van den Driessche, 1974). Esta técnica de diagnóstico permite encontrar la proporción y cantidad de cada elemento que la planta requiere para crecer adecuadamente (Drechsel & Zech, 1991). Además, definir niveles de deficiencia o de consumo de lujo cuando una especie excluye o acumula algún nutrimento que le podría ser tóxico en grandes cantidades (Smith & Loneragan, 1997; Alvarado et al., 2015).
En el presente trabajo se tienen como objetivos definir el “rango satisfactorio” de concentración de nutrimentos a nivel foliar para cada uno de los elementos estudiados de cuatro fabáceas del bosque tropical estacionalmente seco de Guanacaste, Costa Rica. Además, estudiar el efecto de la capacidad de fijar nitrógeno y la tasa de crecimiento de las especies sobre la concentración foliar de nutrimentos esenciales. Se entenderá como “rango satisfactorio” el ámbito de valores máximos y mínimos de nutrimentos a nivel foliar que expresan la mayoría de los individuos de una especie en aparente crecimiento sin problemas nutricionales, excluyendo los valores extremos. Este rango se define como aquel en el que se ubican los datos obtenidos en el laboratorio entre el primer y el tercer cuartil después de eliminar los valores atípicos. De esta manera, se interpreta que si una muestra en particular tiene un valor cercano al inferior del rango, la posibilidad de que el árbol esté deficiente en el elemento es alta (> 95 % de probabilidad) y si se encuentra cerca del valor máximo del rango el riesgo de toxicidad es alto (> 95 % de probabilidad).
Materiales y métodos
Sitio de estudio: La investigación se realizó con muestras foliares recolectadas en diferentes localidades de la vertiente pacífica de Costa Rica (Figura 1). El 93 % del total de muestras (total: 74 muestras) se recolectó en la provincia de Guanacaste, en las localidades de Abangares, Carrillo, Hojancha, Liberia, Nadayure y Nicoya (Figura 1). Un restante 7 % de las muestras se obtuvieron en localidades más al sur de Costa Rica (Figura 1). Las muestras de Liberia fueron recolectadas en la Estación Experimental Forestal Horizontes (EEFH) y la Finca La Flor en las llanuras de la cuenca del río Tempisque. En general, la vegetación natural de la región corresponde al bosque tropical estacionalmente seco (Jiménez, Carrillo, & Kappelle, 2015). Se caracteriza en Guanacaste por la ocurrencia de dos períodos lluviosos, uno de mayo a junio y otro entre agosto y noviembre, además de dos períodos secos con humedad relativa alta, uno ventoso, largo y severo de noviembre a mayo y otro corto en julio. Los meses más calientes y secos se presentan en marzo y abril y los más fríos al final del segundo período húmedo y al inicio del primer período seco (Jiménez et al., 2015). En general, la vegetación de la región se caracteriza por formaciones de vegetación arbustiva, parches de vegetación sabanoide y pequeños parches de bosque caducifolio o siempreverde cerca de los ríos (Gómez, 1986). La geomorfología, geología, clima y cobertura vegetal de la región ha sido descrita por varios autores (Jiménez et al., 2015). En general, las muestras provienen de sitios ubicados a menos de 800 msnm, con regímenes de temperatura del suelo isohipertérmicos y de humedad údico y ústico.
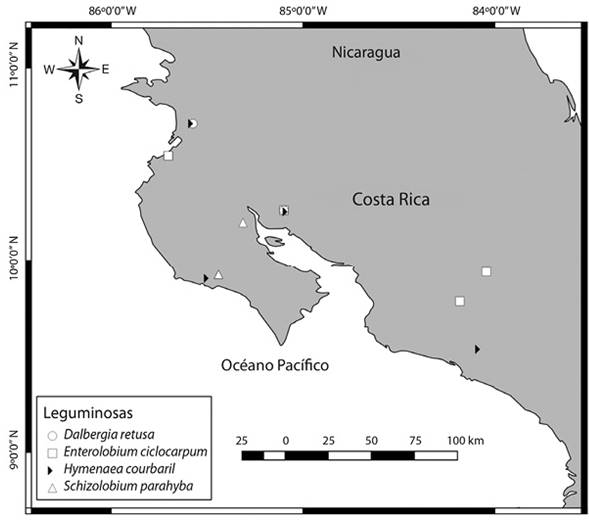
Figura 1 Ubicación de los sitios en los que se recolectaron las muestras para cada especie de árbol estudiada. Figure 1. Location of sampling sites for each tree species studied.
Recolección y análisis de las muestras: En total se contó con un total de 74 muestras consistentes de 18 de S. parahyba, 10 de D. retusa, 33 de H. courbaril y 13 de E. cyclocarpum. Una comparación detallada de estas especies se presenta en el cuadro 1. El tejido foliar utilizado se recolectó en el 2015 a partir de árboles ubicados en plantaciones y bosques de Costa Rica siguiendo los lineamientos mencionados por Bündchen et al. (2013). Con el fin de homogenizar el material vegetal se seleccionaron árboles con crecimiento vigoroso (dominantes) con alturas entre 15-20 m y distanciados por más de 20 m. Se recolectó medio kilogramo de hojas frescas maduras (color verde intenso) utilizando una podadora con barra de extensión. Las hojas estuvieron totalmente expuestas a la luz, ya fuera en la parte media y terminal de la copa. Las muestras se colocaron en bolsas de papel indicando su ubicación, el nombre de la finca, la especie y el día de muestreo. La recolección de las muestras se llevó a cabo durante el período lluvioso cuando los árboles alcanzan su máximo crecimiento anual, aproximadamente un mes después de las primeras lluvias. Con el fin de evitar pérdida del material recolectado las muestras se pusieron a secar a la sombra y se transportaron al laboratorio, donde se terminaron de secar en una estufa a 70 °C por 72 horas.
Las muestras se enviaron al Laboratorio de suelos y foliares de la Escuela de Agricultura de la Región del Trópico Húmedo (Universidad EARTH, Guácimo, Costa Rica) donde se analizaron por Ca, Mg, K, S, Fe, Mn, Cu, Zn, B y Na empleando un aparato de espectrometría de emisión siguiendo la metodología descrita por Kalra (1997) y el P por fotometría siguiendo el método del azul de molibdeno (Murphy & Riley, 1962). La concentración de N se obtuvo mediante combustión seca en un analizador de C, H, O y N por el método de Dumas en un auto-analizador con incineración a 500 ºC.
Análisis estadísticos: Se estimaron los estadísticos descriptivos de la distribución de cada nutrimento para cada especie (media, error estándar, coeficiente de variación, mínimo y máximo). Para estimar diferencias entre los contenidos de los nutrimentos foliares entre especies se realizaron pruebas de Kruskal-Wallis de una vía (α = 0.05). Se utilizaron pruebas a posteriori para las comparaciones entre pares de especies. Para caracterizar y agrupar las especies de acuerdo a las relaciones de los nutrimentos foliares se usó un análisis de componentes principales (Husson, Lê & Pagès, 2011). El análisis de componentes principales se hizo usando sólo aquellos nutrimentos en los que al menos una especie resultó diferente. Se calculó la cantidad absoluta de nutrimentos como la sumatoria de porcentajes con base a peso seco de todos los elementos en cada especie. Los rangos satisfactorios de concentración foliar para cada uno de los nutrimentos se clasificaron según los criterios previamente reportados en la literatura (Büendchen, Boeger, Reissmann, & da Silva, 2013; Metali, Salim, Tennakoon, & Burslem, 2015) como deficiente (por debajo del primer cuartil) y en riesgo de toxicidad o consumo de lujo (por encima del tercer cuartil) y posteriormente fueron mostrados en histogramas. Todos los análisis estadísticos se realizaron con el programa R (R Core Team, 2016).
Resultados
Entre las cuatro especies comparadas se encontró variación intra e inter específica en los macronutrimentos y micronutrimentos estudiados (Figura 2 y Figura 3). El coeficiente de variación fue entre 13.55 % en N de H. courbaril y 86 % en Na de E. cyclocarpum (Cuadro 3) y en general, los coeficientes de variación más altos se notaron en los micronutrimentos (Cuadro 3). Se obtuvieron diferencias en la cantidad de nutrimentos entre las especies para la mayoría de los elementos excepto en Na y Fe (Figura 3). El guanacaste, E. cyclocarpum, tuvo mayor concentración de los tres principales nutrimentos (N, P y K) en comparación con las otras especies (Figura 2).
Cuadro 3: Estadísticos descriptivos de los nutrimentos foliares para cada especie forestal estudiada, error estándar (EE), coeficiente de variación (CV), valor mínimo (Min.) y valor máximo (Max.). Las unidades de los elementos de los macronutrimentos es porcentaje masa / masa y la de los micronutrimentos (respresentados con asterisco”*”) es mg kg -1. Table 3: Descriptive statistics of the foliar nutrients for each tree species studied, standard error (EE), the coefficient of variation (CV), minimum (Min.) and maximum (Max.). The units for macronutrients elements are percentage mass/mass and for micronutrients elements (marked with asterisks “*”) is mg kg -1
| Parámetro | N | P | Ca | Mg | K | S | Na* | Fe* | Cu* | Zn* | Mn* | B* |
| % | * mg kg -1 | |||||||||||
| Dalbergia retusa (N = 10) | ||||||||||||
| Media | 2.63 | 0.09 | 1.26 | 1.18 | 0.61 | 0.21 | 70 | 146.25 | 29.9 | 53.7 | 244.8 | 29.4 |
| EE | 0.83 | 0.03 | 0.4 | 0.37 | 0.19 | 0.07 | 22.14 | 46.25 | 9.46 | 16.98 | 77.41 | 9.3 |
| CV | 23.58 | 39.95 | 37.89 | 84.67 | 76.54 | 23.8 | 35.18 | 65.73 | 36.48 | 32.86 | 60.62 | 36.64 |
| Mín. | 1.79 | 0.05 | 0.64 | 0.24 | 0.13 | 0.15 | 37 | 49 | 11 | 29 | 56 | 13 |
| Máx. | 3.67 | 0.15 | 2.07 | 2.65 | 1.39 | 0.29 | 96 | 297 | 47 | 79 | 490 | 48 |
| Enterolobium cyclocarpum (N = 13) | ||||||||||||
| Media | 3.81 | 0.17 | 0.51 | 0.98 | 1.75 | 0.19 | 38.33 | 135.31 | 6.92 | 22.92 | 55.92 | 27.38 |
| EE | 1.06 | 0.05 | 0.14 | 0.27 | 0.48 | 0.05 | 10.63 | 37.53 | 1.92 | 6.36 | 15.51 | 7.6 |
| CV | 20.12 | 36.01 | 35.55 | 25.43 | 34.28 | 24.7 | 90.08 | 47.15 | 38.43 | 84.69 | 41.34 | 54.11 |
| Mín. | 2.82 | 0.08 | 0.13 | 0.6 | 0.96 | 0.13 | 9 | 63 | 4 | 9 | 27 | 11 |
| Máx. | 5.03 | 0.25 | 0.91 | 1.42 | 2.89 | 0.28 | 120 | 264 | 11 | 74 | 98 | 57 |
| Hymenaea courbaril (N = 33) | ||||||||||||
| Media | 1.87 | 0.12 | 0.71 | 0.56 | 0.59 | 0.13 | 97.33 | 325 | 12.15 | 25.24 | 277.84 | 17.67 |
| EE | 0.32 | 0.02 | 0.12 | 0.1 | 0.1 | 0.02 | 16.94 | 56.58 | 2.12 | 4.39 | 48.37 | 3.08 |
| CV | 33 | 52.42 | 53.12 | 83.45 | 106.19 | 32.56 | 102.68 | 111.21 | 65.97 | 23.79 | 50.11 | 42.07 |
| Mín. | 1.35 | 0.06 | 0.26 | 0.08 | 0.18 | 0.06 | 20 | 40 | 5 | 15 | 59 | 7 |
| Máx. | 4.47 | 0.3 | 1.73 | 1.29 | 2.41 | 0.23 | 363 | 1699 | 42 | 43 | 763 | 33 |
| Schizolobium parahyba (N = 18) | ||||||||||||
| Media | 1.62 | 0.16 | 0.98 | 0.17 | 0.92 | 0.25 | 19.8 | 161 | 8.33 | 16.24 | 36.56 | 12.06 |
| EE | 0.38 | 0.04 | 0.23 | 0.04 | 0.22 | 0.06 | 4.67 | 37.95 | 1.96 | 3.83 | 8.62 | 2.84 |
| CV | 13.28 | 15.57 | 35.93 | 23.27 | 21.96 | 31.88 | 19.23 | 45.18 | 20.16 | 9.37 | 22.6 | 35.62 |
| Mín. | 1.3 | 0.13 | 0.45 | 0.13 | 0.66 | 0.14 | 15.4 | 72 | 7 | 13 | 26 | 8 |
| Máx. | 2.05 | 0.21 | 1.98 | 0.26 | 1.52 | 0.45 | 22 | 385 | 14 | 20 | 52 | 27 |
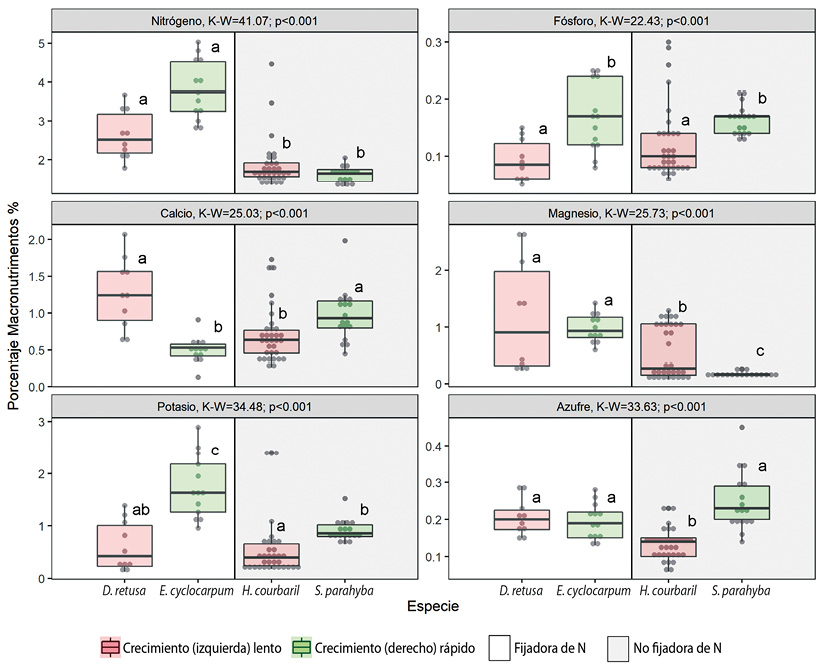
Figura 2 Distribución de los valores de concentración de macronutrimentos en las hojas (%) en cuatro especies de leguminosas en la vertiente pacífica de Costa Rica. Los puntos representan los valores observados, las cajas representan el intervalo intercuartil y la línea horizontal dentro de las cajas la mediana. El valor de K-W y p son respectivamente el valor del estadístico Kruskal-Wallis y la probabilidad con 3 grados de libertad. Las letras representan los grupos según las prueba de diferencias mínimas significativas. Figure 2. Boxplot of the foliar concentration (%) of macronutrients in four woody legumes from de Pacific slope of Costa Rica. Within each boxplot, points represent the observed values, the box represents the interquartile range and the horizontal line represents the median. K-W and p are the Kruskal-Wallis statistic and the probability with 3 degrees of freedom, respectively. Letters represent the groups according to minimum differences test.
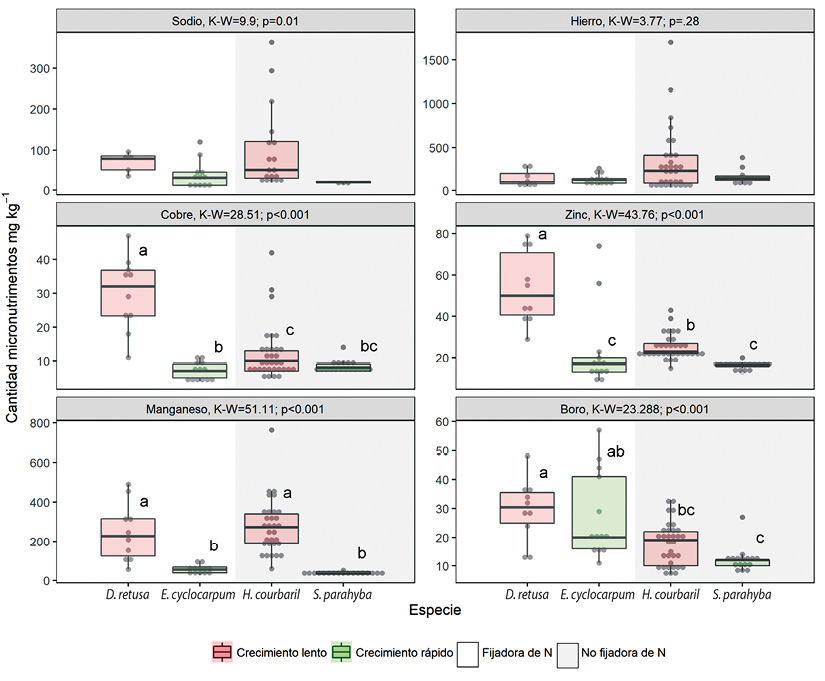
Figura 3 Distribución de los valores de concentración de micronutrimentos en las hojas (mg kg-1) en cuatro especies de leguminosas en la vertiente pacífica de Costa Rica. Los puntos representan los valores observados, las cajas representan el intervalo intercuartil y la línea horizontal dentro de las cajas la mediana. El valor de K-W y p son respectivamente el valor del estadístico Kruskal-Wallis y la probabilidad con 3 grados de libertad. Las letras representan los grupos según las prueba de diferencias mínimas significativas. Figure 3. Boxplots of the foliar concentration (mg kg-1) of micronutrients in four woody legumes from de Pacific slope of Costa Rica. Within each boxplot, points represent the observed values, the box represents the interquartile range, and the horizontal line represents the median. K-W and p are the Kruskal-Wallis statistic and the probability with 3 degrees of freedom, respectively. Letters represent the groups according to minimum differences test.
Las especies fijadoras de nitrógeno, tuvieron mayor cantidad de N, Mg (Figura 2) y de B (Figura 3) en comparación con las no fijadoras. Las especies de crecimiento rápido mostraron mayor cantidad de P y K (Figura 2) y menor cantidad de Zn y Mn (Figura 3) en comparación con las especies de crecimiento lento. El Ca, S, Na, Fe y Cu no mostraron ningún patrón específico entre especies fijadoras o no fijadoras, o entre especies de crecimiento lento o crecimiento rápido. La concentración foliar de Na y Fe no permite utilizar estos parámetros como discriminantes ya que no varían significativamente entre las especies comparadas (Figura 2 y Figura 3). Por el contrario, las concentración más elevadas de K permiten identificar a la especie E. cyclocarpum como significativamente diferente de las demás, la concentración baja de azufre separa H. courbaril de las otras especies al igual que la concentración baja de Mg separa a S. parahyba de las otras especies (Figura 2). Finalmente, la concentración alta de Zn y Cu diferencian a D. retusa con respecto a las otras especies (Figura 3).
Las cinco primeras dimensiones del análisis de componentes principales explican el 84 % de la variación de los valores de concentración foliar de todas las especies (Cuadro 4). El primer componente, que explica el 31 % de la variación, separa a las especies de crecimiento lento de las de crecimiento rápido y está correlacionado principalmente con los contenidos de Na, Fe y el K (Cuadro 4, Figura 4). El segundo componente, que explica el 20.6 % de la variancia, separa las especies fijadoras de N y las no fijadoras y está correlacionado principalmente con las concentraciones de B, Zn y N (Cuadro 4, Figura 4). Los valores de los primeros dos componentes de E. cyclocarpum tienen trasplape con los de las otras especies, que tienen valores más diferentes entre ellas (Figura 4). No obstante debido a que ambos componentes apenas incluyen sólo el 50 % de la variación, es posible que todas las especies queden separadas al incluir otros componentes (Figura 4).
Cuadro 4: Variancia explicada por el análisis de componentes principales de los valores de macronutrimentos y micronutrimentos de cuatro especies de leguminosas forestales. Table 4: Variance explained by the principal component analysis for the macro- and micronutrients of four tree legume species
| Comp. 1 | Comp. 2 | Comp. 3 | Comp. 4 | Comp. 5 | |
| Variancia | 3.744 | 2.483 | 1.645 | 1.397 | 0.781 |
| Porcentaje de variancia | 31.203 | 20.694 | 13.704 | 11.646 | 6.511 |
| Porcentaje de variancia acumulado | 31.203 | 51.897 | 65.601 | 77.247 | 83.758 |
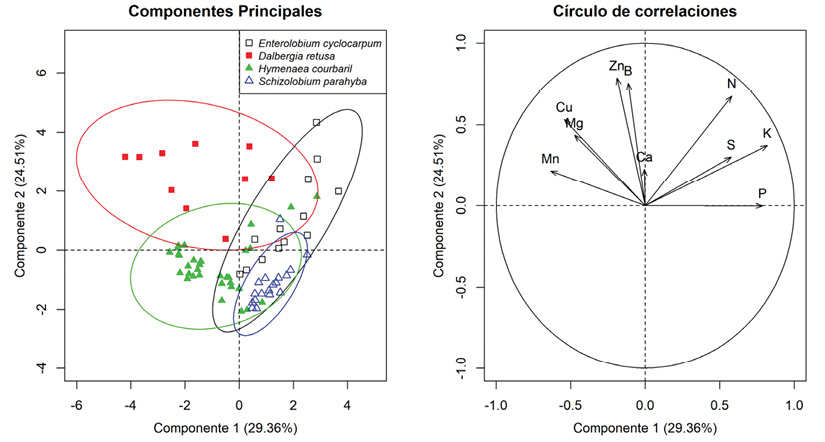
Figura 4 Componentes principales (1 y 2) y círculo de correlaciones de los macronutrimentos y micronutrimentos de cuatro especies de leguminosas forestales. Cada color representa una especie diferente, los símbolos cuadrados son especies fijadoras de nitrógeno, los símbolos triangulares son de especies no fijadoras de nitrógeno. Lo símbolos rellenos son especies de crecimiento lento, los símbolos vacíos son especies de crecimiento rápido. Los elipses encierran el 95 % de los valores. Figure 4. Principal components (1 and 2) and correlation circle of the macro- and micronutrients of four woody legumes. Colors represent the species; squares are nitrogen-fixing species, triangles the non-nitrogen-fixing species. Filled symbols are slow-growing species and empty symbols fast-growing species. Ellipses enclose the 95 % of the values.
En términos de cantidad total de concentración de macronutrimentos (sumatoria de porcentajes de todos los elementos en cada especie), esta aumenta en el orden H. courbaril (3.98 %), S. parahyba (4.10 %), D. retusa (5.98 %) y E. cyclocarpum (7.41 %) debido principalmente a la contribución del N. En el caso del E. cyclocarpum, este alcanza valores altos por las contribuciones del N y K y en el caso de D. retusa por las contribuciones del Mg y Ca. La cantidad total de macronutrimentos fue más alta en especies fijadoras que en especies no fijadoras de N y más alta en especies de crecimiento rápido que en especies de crecimiento lento (Cuadro 5).
Cuadro 5: Secuencia de los macro and micronutimentos según la concentración foliar en cuatro especies de leguminosas estudiadas en Costa Rica. Table 5: Sequence of the macro- and micronutrients according to the foliar concentration in four woody legumes species studied in Costa Rica
| Especie | Macronutrimentos (%) |
| Dalbergia retusa | N (2.63) > Ca (1.26) > Mg (1.18) > K (0.61) > S (0.21) > P (0.09) |
| Enterolobium cyclocarpum | N (3.81) > K (1.75) > Mg (0.98) > Ca (0.51) > S (0.19) > P (0.17) |
| Hymenaea courbaril | N (1.87) > Ca (0.71) > K (0.59) > Mg (0.56) > S (0.13) > P (0.12) |
| Schizolobium parahyba | N (1.62) > Ca (0.98) > K (0.92) > S (0.25) > Mg (0.17) > P (0.16) |
| Micronutrimentos (mg kg-1) | |
| Dalbergia retusa | Mn (244.8) > Fe (146.25) > Na (70) > Zn (53.7) > Cu (29.9) > B (29.4) |
| Enterolobium cyclocarpum | Fe (135.31) > Mn (55.92) > Na (38.33) > B (27.38) > Zn (22.92) > Cu (6.92) |
| Hymenaea courbaril | Fe (325) > Mn (277.84) > Na (97.33) > Zn (25.24) > B (17.67) > Cu (12.15) |
| Schizolobium parahyba | Fe (161) > Mn (36.56) > Na (19.8) > Zn (16.24) > B (12.06) > Cu (8.33) |
Los valores más elevados de concentración foliar de nutrimentos en todas las especies fueron los de N y los más bajos los del P (Cuadro 5). Según la secuencia de la concentración foliar de los diferentes elementos en orden descendente para las especies estudiadas se infiere que la concentración foliar de los macronutrimentos para la mayoría de las especies en estudio sigue el orden N > Ca > K > Mg > S ≥ P. Excepto para E. cyclocarpum cuya concentración de K es mayor a la del Ca y para S. parahayba en el que la concentración de S es mayor que la de Mg. La concentración foliar de los micronutrimentos siguió el mismo orden en las especies no fijadoras de N (H. courbarily S. parahyba). Pero el orden cambió en las otras especies aunque el Mn y Fe siempre fueron más altos que el Na y el Zn, y el Cu y B siempre fueron más bajos que el Na.
Rangos Satisfactorios (RS) de Concentración Foliar: Empleando como criterio de definición del rango satisfactorio los valores de concentración para los percentiles 25 (mínimo) y 75 (máximo), se encontró que D. retusa y H. courbaril podrían requerir menor cantidad de nutrimentos como fósforo o potasio que E. cyclocarpum y S. parahyba, que tienen más requerimientos nutricionales (Cuadro 6). Relativo a su capacidad de fijar nitrógeno D. retusa y H. courbaril también tuvieron menores concentraciones de este macronutrimento que E. cyclocarpum y S. parahyba (Cuadro 6).
Cuadro 6: Rango satisfactorio (RS) de concentración foliar de elementos (valores en los percentiles 25 y 75) en D. retusa, E. cyclocarpum, H. courbaril y S. parahyba en Guanacaste, Costa Rica. Table 6: Satisfactory range (RS) of foliar concentration of elements (interquartile range) for D. retusa, E. cyclocarpum, H. courbaril and S. parahyba in Guanacaste, Costa Rica
| Elemento | Dalbergia retusa | Enterolobium cyclocarpum | Hymenaea courbaril | Schizolobium parahyba |
| Macronutrimentos (%) | ||||
| N | 2.18 - 3.17 | 3.24 - 4.52 | 1.56 - 1.92 | 1.43 - 1.75 |
| Ca | 0.90 - 1.56 | 0.42 - 0.58 | 0.46 - 0.77 | 0.80 - 1.16 |
| K | 0.23 - 1.01 | 1.26 - 2.18 | 0.24 - 0.66 | 0.8 - 1.02 |
| Mg | 0.31 - 1.97 | 0.82 - 1.17 | 0.15 - 1.05 | 0.15 - 0.18 |
| S | 0.17 - 0.22 | 0.15 - 0.22 | 0.10 - 0.15 | 0.20 - 0.29 |
| P | 0.06 - 0.12 | 0.12 - 0.24 | 0.08 - 0.14 | 0.14 - 0.17 |
| Micronutrimentos (mg kg-1) | ||||
| Na | 52 - 86 | 12 - 46 | 31 - 121 | 19 - 22 |
| Fe | 79 - 205 | 86 - 148 | 84 - 413 | 128 - 176 |
| Mn | 124 - 316 | 39 - 67 | 191 - 340 | 31 - 45 |
| Zn | 41 - 71 | 13 - 20 | 22 - 27 | 16 - 17 |
| B | 25 - 36 | 16 - 41 | 10 - 22 | 10 - 12 |
| Cu | 23 - 37 | 5 - 9 | 7 - 13 | 7 - 9 |
Discusión
A pesar de que se considera que cierta proporción de los nutrimentos presentes en las hojas se deben a un componente genético (Masunaga, Kubota, Hotta & Wakatsuki, 1998, Masunaga et al., 1998; Fyllas et al., 2009), otros factores (p.e. edáficos) pueden afectar la concentración foliar de los nutrimentos en el follaje. Chimphango et al. (2015) encontraron que en los hábitats con especies leguminosas en suelos derivados de calizas y areniscas tienen más N total, P, K, Mg, Na y C pero solamente de C en los derivados de granito en Sudáfrica. Lo anteriormente mencionado indica empíricamente una relación entre la concentración foliar y las propiedades químicas de los suelos y que algunas especies puedan requerir suelos fértiles mientras que otras enriquecen el medio particularmente con N y Mg (Van Breugel et al., 2011).
Los altos valores en los coeficientes de variación encontrados en el presente estudio se pueden deber a un efecto de sitio y a las diferentes edades de los árboles muestreados (Letcher et al., 2015). Esto se puede observar en nutrimentos como el Fe, Mn y Na en los que no hay una diferencia entre las especies. La distribución de frecuencias para cada especie y para muchos de los elementos analizados no tiende a la normalidad (datos no incluidos), probablemente debido al tamaño de la muestra. Además, los valores de concentración foliar bajos son más abundantes que los altos (Alvarado et al., 2015), presentándose distribuciones sesgadas hacia la izquierda como ha sido reportado en bosques de Europa (Vanmechelen, Groenemans & van Ranst, 1997) y subtropicales lluviosos de Taiwan (Wu, Tsui, Hseih, Asio, & Chen, 2007).
Se observó mayor concentración de nutrimentos en las especies fijadoras que en las no fijadoras de N y además dentro de cada uno de esos grupos, que las de crecimiento rápido tenían mayor concentración de nutrimentos que las de crecimiento lento. El efecto de “dilución” de la concentración foliar puede ayudar a explicar las disminuciones en concentración foliar en especies de crecimiento rápido en las que la mayor concentración de un elemento (ej. N) resulta en un incremento de biomasa foliar mientras que al mismo tiempo la concentración los otros nutrimentos por unidad de biomasa se disminuye/reduce (Marschner, 1995). Igualmente otros factores que afectan la concentración foliar de algunos elementos son el lavado (ej. K), otras interacciones de naturaleza fisiológica que envuelven cambios en su translocación y las interacciones que ocurren en la superficie de las raíces o en su membrana celular (Van den Driessche, 1974). En el caso de S. parahyba, aunque es la única especie considerada pionera de las comparadas en el presente estudio, su contenido total de nutrimentos en el tejido foliar no es el más elevado, como sugiere la hipótesis de sucesión ecológica descrita por Broadbent et al. (2014).
Los valores más elevados de concentración foliar de nutrimentos en todas las especies fueron los de N (Cuadro 3 y Cuadro 5). En las especies D. retusa y E. cyclocarpum esto podría estar asociado a la fijación simbiótica del elemento con bacterias del género Rhizobium (Gei, 2014; Gei & Powers, 2013; 2014) mientras que las concentraciones foliares de P y Cu en las especies estudiadas son muy bajas como ha sido mencionado para un gran número de especies latifoliadas tropicales (Drechsel & Zech, 1991). Sprent (1999) discute la necesidad de P en leguminosas fijadoras y no fijadoras de N y concluye que no se comprueba que en los trópicos se tengan los altos requerimientos del elemento mencionados en regiones subtropicales, encontrándose leguminosas que pueden fijar el elemento en suelos bajos en P disponible. Büendchen et al. (2013) indican que las altas concentraciones foliares de N y las bajas de P redundan en una eficiencia inversa de uso de estos nutrimentos, es decir la del N es baja y la del P elevada. Para H. coubaril en Honduras se menciona que este hecho podría asociarse a la presencia de micorrizas ligadas a su sistema radical (Hunter & Stewart, 1993) lo que concuerda con la poca respuesta de esta especie a la adición de P en invernadero (Resende et al., 1999; Santos, Resende, Neto & Corte, 2008).
La concentración foliar de Ca observada en todas las especies está dentro de los valores del rango normal para especies tropicales latifoliadas, con una relación Ca/K mayor que la unidad (Alvarado, 2015). Lo anterior podría interpretarse como adaptación genética a ambientes tropicales estacionalmente secos en los que la disponibilidad de Ca en el suelo es elevada. Los valores de concentración foliar de los micronutrimentos se encuentran dentro de los considerados normales para Fe y Mn para otras especies forestales, al igual que sucede con las concentraciones foliares de Na, Zn y B (Stone, 1990; Reeves & Baker, 2000).
En el cuadro 5 se muestra la secuencia de la concentración foliar de los diferentes elementos en orden descendente para las especies estudiadas. Se infiere que la concentración foliar de los macronutrimentos para todas las especies sigue el orden N > Ca > Mg > K > S ≥ P es una tendencia que domina en especies forestales tropicales latifoliadas (Drechsel & Zech, 1991; Alvarado et al., 2015b). La concentración foliar de los micronutrimentos en orden descendente sigue el orden Fe > Mn > Na > B > Zn > Cu. Aunque los valores de Na, B y Zn pueden variar de posición según la especie sin que se cuente con otras experiencias similares en la literatura que permitan explicar el porqué de esta relación. En el presente trabajo se suministra información sobre Na y B elementos raras veces reportados para estas especies en la literatura.
Rangos satisfactorios de concentración foliar: El empleo del análisis foliar en el sector forestal es limitado entre otras razones por la falta de criterios de interpretación de los resultados emanados de los laboratorios de servicio (Alvarado, 2015). Empleando como criterio de definición de los rangos satisfactorios como los valores de concentración de nutrimentos entre los percentiles 25 (mínimo) y 75 (máximo), se recomienda utilizar los valores presentados en el cuadro 6 para interpretar los resultados de análisis foliares de estas especies del bosque tropical estacionalmente seco de Costa Rica. Los resultados obtenidos en el análisis de este trabajo son un aporte al conocimiento sobre las concentraciones foliares de las especies D. retusa e H. courbaril para las que no existen estudios previos que describan la concentración foliar de nutrimentos en la vertiente pacífica estacionalmente seca de Costa Rica.












 uBio
uBio 

