Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista de Biología Tropical
On-line version ISSN 0034-7744Print version ISSN 0034-7744
Rev. biol. trop vol.58 suppl.3 San José Oct. 2010
Distribución de metales pesados en los sedimentos superficiales del Saco del Golfo de Cariaco, Sucre, Venezuela
María Valentina Fuentes H.1, Luisa Rojas de Astudillo2,3, Alfredo Diaz2 & Gregorio Martínez4
1. Departamento de Bioanálisis;
2. Departamento de Química;
3. Instituto de Investigaciones en Biomedicina y Ciencias Aplicadas;
4. Instituto Oceanográfico de Venezuela, Universidad de Oriente, Cumaná, Venezuela; mariavalentinafuentesh@yahoo.com
Abstract
Key words: sequential extraction, geochemical fractions, heavy metals, Gulf of Cariaco, Venezuela.
Resumen
El Golfo de Cariaco es un ecosistema marino con mucha productividad primaria, lo que le confiere especial importancia ecológica y socioeconómica. Sin embargo, los desechos de las actividades antropogénicas son descargados directamente o arrastradas por las escorrentías. El objetivo de este estudio fue determinar la distribución de cadmio, cobre, plomo, manganeso, níquel y zinc en las fracciones geoquímica de los sedimentos superficiales, usando el método modificado de extracción secuencial de la Comunidad Europea (BCR). Las concentraciones de los metales fueron medidas por espectroscopía de absorción atómica. Además, se compararon los contenidos de metales intercambiables y asociados a los carbonatos determinados por el procedimiento BCR modificado con los determinados por el método de Campanella. La recolección de muestras se hizo en 12 estaciones del sector oriental del Golfo de Cariaco, Estado Sucre, específicamente en el sector conocido como el Saco, en junio 2007. Las metodologías aplicadas fueron evaluadas usando un material de referencia certificado de sedimentos marino (HISS - 1). Los resultados indicaron que los métodos proveen exactitud y precisión adecuadas para la extracción de metales. Las concentraciones totales (μg g-1) fueron, Cd: < límite de detección (LD)-5.0; Pb: 1.79- 60.41; Cu: no detectado (ND)-42.18; Zn: 25.13-104.57; Mn: 66.31-80.29 y Ni: 3.29-24.58. Cd, Cu, Ni y Pb excedieron en varias estaciones los límites que pueden afectar la biota, establecidos por la Guía de Evaluación de la Calidad de los Sedimentos de Canadá. El cadmio fue el metal identificado como el más móvil, teniendo las más altas concentraciones como intercambiable y asociado a las fracciones de carbonatos. Sin embargo, Pb, Cu, Mn y Zn mostraron su mayor abundancia en la fracción asociada a materia orgánica y azufre. Los métodos no presentan diferencias significativas para extraer la primera fracción. Se encontraron significantes correlaciones entre los metales pesados que sugieren su origen común.Key words: sequential extraction, geochemical fractions, heavy metals, Gulf of Cariaco, Venezuela.
Los metales pesados pueden adsorberse en aluminosilicatos, óxidos de hierro y manganeso, carbonatos de calcio y materia orgánica. figura el protocolo del Consejo Canadiense de En suelos y sedimentos, su capacidad de adsorción y liberación dependen, fundamentalmente del pH y de las condiciones redox (Filius et al. 1998). Además, su distribución en las diferentes fracciones geoquímicas está condicionada por las propiedades de cada metal, la competencia por los sitios de adsorción del sedimento, la capacidad de formar complejos y la magnitud de la contaminación de los sedimentos (Campbell 1995).
Debido a la dificultad de comparar los resultados obtenidos por diferentes investigadores y métodos distintos, la Oficina de Referencias de la Comunidad Europea (BCR) creó un protocolo para la especiación de metales pesados (Ure et al. 1993). Este procedimiento separa los metales de una muestra de suelo o sedimento, en cuatro fracciones: soluble en medio ácido, reducible, oxidable y residual o detrítica. Sin embargo, durante una certificación del BCR usando material de referencia certificado (CRM 601) mostró una variabilidad interlaboratorio significante en la extracción de la fracción reducible. Esto condujo al desarrollo de un procedimiento de extracción secuencial modificado de BCR (Rauret et al. 1999), el cual fue reevaluado usando el CRM 601 como sustrato de prueba. El BCR optimizado fue más eficiente en la disolución de los metales asociados a los oxihidróxidos de hierro y manganeso (fracción reducible) (Rauret et al. 1999, Mossop & Davidson 2003). Otro procedimiento útil para estudiar el fraccionamiento geoquímico de metales en sedimentos marinos y lacustres es el método de Campanella et al. (1995). Este método permite discriminar la fracción de los metales incorporados en los carbonatos, sustituyendo el ácido acético, reactivo de extracción del método BCR, por acetato de amonio ajustado a pH 5 con ácido acético. De esa manera, el extracto es amortiguado y la acidificación producida por la descomposición química de los carbonatos es prevenida (Baeyens et al. 2003).
El Saco del Golfo de Cariaco es una zona bordeada de manglares, con elevada productividad primaria (Ferráz 1987) y gran riqueza pesquera, socioeconómica y turística; sin embargo, en ella descargan contaminantes provenientes de los desechos domésticos de los poblados circundantes, de la actividad agrícola y del tráfico marino. Su manera de ingreso es variada: directa, transportados por las aguas del Río Carinicuao, las aguas lluvias y aguas de escorrentías y arroyos estacionales. Entre los contaminantes de mayor peligrosidad, se encuentran los metales pesados, cuyo destino final son los sedimentos (Martínez 2002).
Materiales y métodos
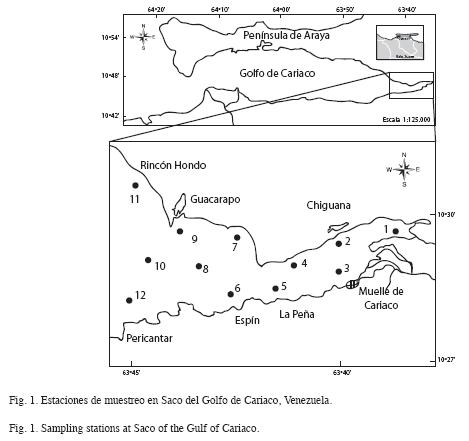
Para el estudio, las muestras de sedimentos superficiales fueron colectadas en doce estaciones, en el mes de junio de 2007 (Fig. 1), con una draga Diez Laffont de 0.02m2. Una vez obtenidas, fue extraída el agua intersticial a una fracción de ellas, mientras que otra fracción fue conservada como tal. Ambas fueron secadas al aire y tamizadas en una malla de 63μm.
Un gramo del sedimento tamizado fue secado en una estufa a 38ºC durante 48 horas. Transcurrido este tiempo, la muestra fue predigerida en 10ml de HNO3 concentrado, durante la noche, a temperatura ambiente, en un matraz Erlemeyer (Rojas et al. 2005). Para evitar pérdidas durante la digestión y mantener un reflujo constante, un pequeño embudo de vidrio fue colocado en el matraz. A continuación, la muestra fue calentada a 60oC durante dos horas, luego progresivamente fue elevada la temperatura hasta 100°C y digerida dos horas más. Una vez fría, fue filtrada (papel de filtro Whatman tipo 42) en un matraz volumétrico de 25ml y diluida hasta la marca. La cuantificación de las concentraciones de los metales fue ejecutada con un espectrofotómetro de absorción atómica a la llama, Perkin Elmer, modelo 3110, de doble haz, llama de aire-acetileno y corrector de fondo de deuterio. Todos los reactivos y patrones externos de calibración fueron grado analítico, y los análisis fueron realizados por triplicado para verificar la precisión del método de digestión y recuperación de los metales. La extracción de los metales en el sedimento total y en el sedimento después de extraída el agua intersticial (agua de poro) no mostró diferencias estadísticas significativas (p≥0 .05).
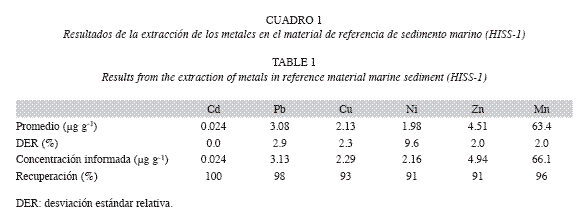
La confiabilidad de la extracción de los metales totales fue evaluada con un material de referencia certificado de sedimentos marino (HISS-1). La exactitud del método fue menor que 9% y la precisión menor que 10% (Cuadro 1). Los blancos de cada conjunto de muestras estuvieron por debajo de 1% de los valores de las muestras, la precisión de las muestras 3% y los límites de detección (LD) obtenidos de la curva de calibración (Meier & Zünd 1993) fueron: Mn (1μg g-1), Zn (3μg g-1), Ni (2μg g-1), Cu (0.07μg g-1), Cd (1μg g-1), Pb (1μg g-1).
Una vez obtenidos los resultados fue calculada la matriz de correlación de Pearson y fueron comparados mediante un análisis de varianza simple.
El índice de geoacumulación (Igeo) fue calculado con la ecuación de Müller (1979):
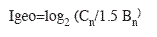
El factor de movilidad (FM) fue calculado como un índice relativo entre las concentraciones de cada metal en la fracción intercambiable y asociada con carbonatos (F1) y la sumatoria de todas las fracciones de cada metal (Salbu et al. 1988).
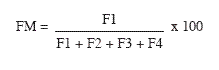
Resultados
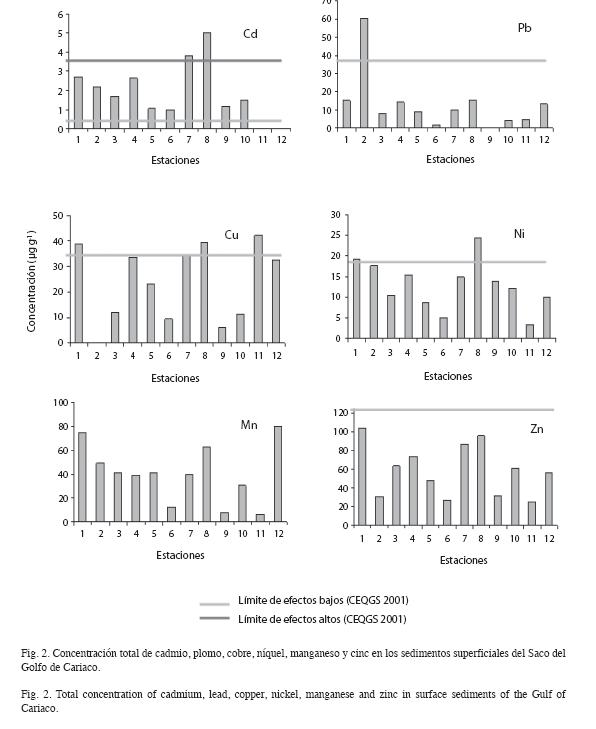
Los intervalos de concentración para cada metal fueron: Cd (<Limite de Detección (LD)- 5.00 μg g-1), Pb (1.67-60.41μg g-1), Cu (<LD-42.18 μg g-1), Ni (3.29-24.58 μg g-1), Mn (6.31-80.29 μg g-1), Zn (25.13-104.57μg g-1). En la figura 2 resaltan las distribuciones similares de Mn, Zn, Cu, Pb y Ni, aunque Pb fue diferente enfrente de Chiguana (Est 2), sitio donde alcanzó su máxima concentración.
Los coeficientes de correlación de Pearson, calculados con las concentraciones de los metales, mostraron asociación positiva entre los pares: Cd-Ni (0.84), Zn-Cd (0.75), Zn-Mn (0.68), Zn-Cu (0.58), Mn-Ni (0.57), Mn-Cu (0.37), Mn-Cd (0.36) y Mn-Pb (0.26).
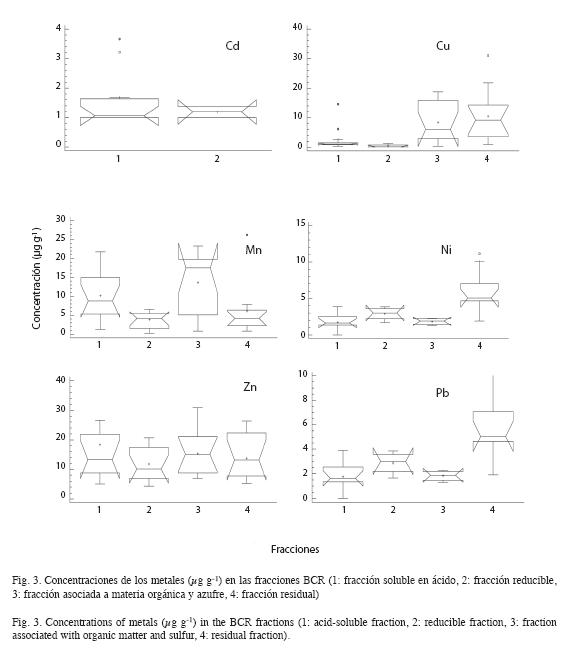
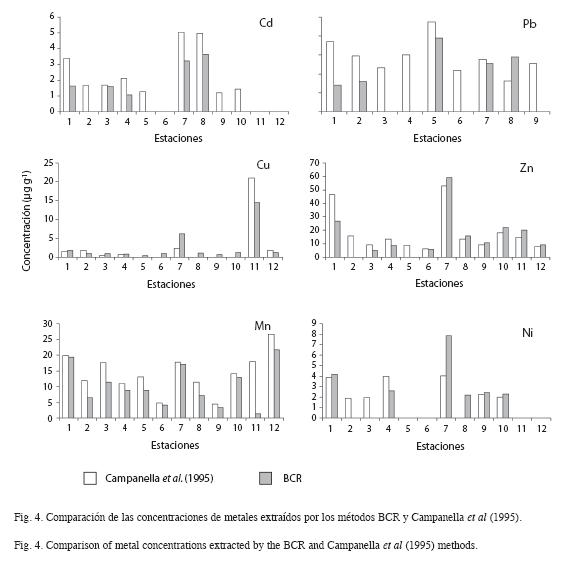
Fraccionamiento BCR. Cd predomina en la fracción más soluble (F1, 52%) (Fig. 3). Sus concentraciones más altas se encontraron al final del Saco (Est 1), en Muelle de Cariaco (Est 3), San Rafael (Est 7) y centro (Est 8). La mediana de F1 no mostró diferencias estadísticas significativas con 1 μg g-1, concentraciσn cuantificada en F2 (48%), en el centro del ecosistema (p≥0.05). Cu predominó en la F4 (48%), seguida de las fracciones F3 (38%), F1 (11%) y F2 (2%). Las medianas de F3 y F4 no mostraron diferencias significativas entre si; sin embargo, fueron diferentes a las medianas de las fracciones F1 y F2. De manera similar al Cu, el metal Ni se asoció mejor con F3 (42%) y F4 (27%), aunque sus medianas para las cuatro fracciones fueron muy diferentes entre si, especialmente entre F1 (17%) y F4.
Las especies químicas del Mn estuvieron mayoritariamente en F1 (intercambiables y formando carbonatos o adsorbidos sobre ellos) y F3 (asociado con la materia orgánica y sulfuros). En esta última fueron más abundantes. Las medianas de las fracciones F1 (33%) y F3 (41%) fueron diferentes a las medianas de F2 (11%) y F4 (15%, p<0.05). Pb predominó en la matriz sedimentaria (F4, 55%), muy diferenciada estadísticamente de las fracciones restantes, cuyas medianas fueron similares (F1: 19%, F2: 16%, F3: 10%); sin embargo el Zn se mantuvo presente en todas las fracciones proporcionalmente distribuido (F2: 22%, F3: 26%, F4: 24%), con un ligero incremento en la F1 (28%).
Discusión
En el ecosistema, las concentraciones totales de Cd superaron el límite de efectos bajos (LEB, 0.6μg g-1) de la normativa canadiense (CEQGS 2001). Además, frente a San Rafael (Est 7) y en el centro (Est 8) sobrepasaron el límite de efectos altos (LEA, 3.5μg g-1). Pb (Est 2), Cu (Ests 1, 8, 11) y Ni (Est 8) también presentaron concentraciones mayores al LEB (Pb: 35μg g-1, Cu: 35.7μg g-1, Ni: 18μg g-1), mientras que las concentraciones de Mn fueronmenores que 716μg g-1, valor reportado para la corteza terrestre (Wedepohl 1995).
La mayor acumulación en el oriente y centro del ecosistema puede estar favorecida por la textura arenolimosa y limoarenosa de sus sedimentos y por la condición hidrodinámica del golfo; sin embargo, en Chiguana (Est 2) la concentración de plomo fue alta a pesar de que los sedimentos son arenosos y contienen muchos restos calcáreos (Quintero et al. 2006). Rubio et al. (2000) señalan que gran cantidad Mn y Zn en los sedimentos de las zonas costeras son de origen litogénico, y su importancia radica en su interacción con otros metales pesados, más que por su carácter tóxico. Así, las correlaciones significativas (p<0.05) entre los pares Mn-Zn, Zn-Cd, Zn-Ni y Zn-Cu, probablemente indican que una porción importante de metales proviene del material litogénico del área; sin embargo, las correlaciones poco significativas Mn-Pb, Mn-Cd y Cu-Mn son indicios de aportes antropogénicos (MacDonald et al. 1991). La ausencia de correlación Pb-Zn parece indicar que Pb no proviene de la misma fuente que introduce Cu, Ni, Zn y Cd al ecosistema. Hung & Hsu (2004) informaron que la fuente de Pb más importante, en los ecosistemas costeros, son los residuos de combustibles liberados hacia la atmósfera por el tráfico rodante y flotante, y transportados por las escorrentías que caen en el ecosistema.
En general, los valores del Igeo, entre 0 y 1 (Müller 1979) permitieron clasificar a los sedimentos del área estudiada como muy poco contaminados, evidenciando los aportes mayoritariamente litogénicos.
Los resultados del fraccionamiento BCR expresan que la materia orgánica y el sulfuro controlan el comportamiento de los metales Mn, Cu, Zn y Ni. Generalmente, los metales pesados reaccionan con FeS y forman precipitados extremadamente insolubles, de acuerdo con la siguiente reacción:
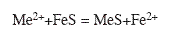
La formación de sulfuros, en los ambientes marinos, es primordialmente biogénica y está controlada por las poblaciones de bacterias que utilizan el sulfato, como aceptor de electrones, y oxidan la materia orgánica produciendo sulfuro de hidrógeno y otros compuestos sulfurados (HS-, S2- y S2 2-). Este proceso está controlado por la calidad y cantidad de materia orgánica que alcanza el régimen anaeróbico. Al mismo tiempo, los compuestos de hierro oxidado son reducidos y los iones de hierro generados pueden reaccionar con el sulfuro de hidrógeno formando una variedad de minerales, incluyendo FeS amorfo y FeS2 (Simpson et al. 2005). Es importante destacar que en el ecosistema estudiado hay minerales opacos, mayoritariamente óxidos de hierro, y cantidades reducidas de pirita en la desembocadura del río Carinicuao, el cual descarga en la zona más oriental (Quintero et al. 2006). Metales como Ni, Cu, Mn y Zn pueden incorporarse a la red cristalina de la pirita y de monosulfuros de hierro durante su precipitación (Ponce et al. 2000).
Skrabal et al. (2000) expusieron que los sedimentos son una fuente significativa de Cu acomplejado con ligandos orgánicos o formando complejos orgánicos sulfurados. Este metal puede ser ciclado activamente entre el sedimento y el agua intersticial, durante la diagénesis temprana del sedimento, y varía espacial y temporalmente, de acuerdo con los procesos biogeoquímicos y condiciones reinantes.
Los resultados indican que Cd, en el ecosistema, es el metal más fácil de solubilizar y puede presentarse como ión acuoso, mientras que Pb está muy relacionado con la matriz mineralógica del sedimento. Este planteamiento es corroborado con los resultados de la movilidad, los cuales señalan al Cd como el metal más móvil (52%). Toxicológicamente, Cd asociado con la fracción intercambiable y asociada con carbonatos es muy biodisponible y puede provocar efectos tóxicos en los organismos bentónicos, situación favorecida por el pH ácido del sistema digestivo; mientras que Pb en la fracción residual es inerte, debido a que las condiciones ambientales no afectan sus enlaces químicos (García et al. 2004).
Los bajos valores de movilidad son indicadores de la alta estabilidad de los metales Cu, Ni, Pb y Zn en los sedimentos, por lo tanto son poco lábiles y bioaccesibles (Ahumada et al. 1999). Este comportamiento depende de las especies químicas de cada metal o de la forma de asociarse a las fracciones geoquímicas del sedimento (Huang et al. 2007).
Agradecimiento
A la Dirección de Planificación de la Universidad de Oriente por el aporte financiero asignado a los proyectos POA 2.1 y POA 3.2 y al Instituto Oceanográfico de Venezuela por las facilidades prestadas.Referencias
Ahumada, I., J. Mendoza L. Ascar. 1999. Sequential extraction of heavy metals in soils irrigated with wastewater. Commun. Soil Sci. Plant Anal. 30: 1507-15181. [ Links ]
Baeyens, W., F. Monteny, M. Leermakers & S. Bouillon. 2003. Evaluation of sequential extractions on dry and wet sediments. Anal. Bioanal. Chem. 376: 890-901. [ Links ]
Breslin, V. & S. Sañudo. 1999. High spatial resolution sampling of metals in the sediment and water column in Port Jefferson harbor, New York. Estuaries 22: 669-680. [ Links ]
Campanella, L., D. D´Orazio, B. Petronio & E. Pietrantonio. 1995. Proposal for a metal speciation study in sediments. Anal. Chim. Acta 309: 387-393. [ Links ]
Carmony, M. & D. Harvey. 2007. Evaluating the effect of calcium carbonate on the BCR extraction procedure. http://www.asdlib.org/posterUploads/78_poster_ publication.pdf [ Links ]
CEQGS. 2001. Canadian sediment quality guidelines for the protection of aquatic life. http://www.ec.gc.ca/ceqgrcqe/English/Ceqg/Sediment/default t.cfm [ Links ]
CCME . 1995. Protocol for the derivation of Canadian sediment quality guidelines for the protection of aquatic life. Manitoba Statutory Publications, Ottawa. [ Links ]
Ferráz, E. 1987. Productividad primaria del Golfo de Cariaco. Bol. Inst. Oceanogr. Venezuela 26: 97-110. [ Links ]
Filgueiras, A., I. Lavilla & C. Bendicho. 2002. Chemical sequential extraction for metal partitioning in environmental solid samples. J. Environ. Monit. 4: 823-857. [ Links ]
Filius, A., T. Streck & J. Richter. 1998. Cadmium sorption and desorption in limed topsoils as influenced by pH: isotherma and simulated leaching. J. Environ. Quality 27: 12-18. [ Links ]
García, L., M. Soto, M. Jara & A. Gómez. 2004. Fracciones geoquímicas de Cd, Cu y Pb en sedimentos costeros superficiales de zonas ostrícolas del Estado de Sonora, México. Rev. Intern. Contam. Ambient. 20: 159-167. [ Links ]
González, M., L. Méndez, D. López & A. Vázquez. 2006. Evaluación de la contaminación en sedimentos del área portuaria y zona costera de Salina Cruz, Oaxaca, México. Interciencia 31: 1-23. [ Links ]
Huang J., R. Huang & J. Jiao. 2007. Speciation and mobility of heavy metals in mud in costal reclamation areas in Shenzhen, China. Environ. Geol. 53: 221-228. [ Links ]
Hung, J. & C. Hsu. 2004. Present state and historical change of trace pollution in Kaoping coastal sediment southwestern, Taiwán. Mar. Poll. Bull. 49: 986-998. [ Links ]
Jonathan, M. & V. Ram. 2003. Heavy metals in sediments of the inner shelf of the Gulf of Mannar, South East Coast of India. Mar. Poll. Bull. 46: 258-268. [ Links ]
Martínez, G. 2002. Metales pesados en sedimentos superficiales del Golfo de Cariaco, Venezuela. Bol. Inst. Oceanogr. Venezuela 41: 83-96. [ Links ]
Meier, P. & R. Zünd. 1993. Statistical methods in analytical chemistry. Wiley, Nueva York, EEUU. [ Links ]
Mossop, K. & M. Davidson. 2003. Comparison of original and modified BCR sequential extraction procedures for the fractioning of copper, iron, lead, manganese and zinc in soils and sediments. Anal. Chim. Acta 478: 111-118. [ Links ]
Müller, G. 1979. Schwermettalle in den sedimenten des Rheins-Veranderungeng seit 1971. Umschau. Wissensch. Tech. 79: 778-783. [ Links ]
Ponce, R., J. Forja & A. Gómez. 2000. Influencia de la actividad antropogénica en la distribución vertical del Zn, Cd, Pb y Cu en agua intersticial y sedimentos marinos costeros (Bahía de Cádiz, SW de España). Cienc. Mar. 26: 479-502. [ Links ]
Quintero, A., L. Caraballo, J. Bonilla, G. Terejova & R. Rivadula. 2006. Sedimentos marinocosteros del Golfo de Cariaco, Venezuela. Bol. Inst. Oceanogr. Venezuela 45: 127-139. [ Links ]
Rauret, G., J. López, A. Sahuquillo, R. Rubio, C. Davidson, A. Ure & P. Quevauviller. 2000. Indicative values for extractable contents (mass fractions) of Cd, Cr, Cu, Ni, Pb and Zn in a sewage sludge–amended soil (CRM 483) following the modified BCR sequential extraction (three step) procedure (addendum to EUr Report 17 127 EN), EUR 19503 EN. European Commission BCR, Luxemburgo. [ Links ]
Rocco, M. & M.A. Rubio. 2009. Reinterpretation of the first step of the sequential extraction proposed by the SMT. J. Chil. Chem. Soc. 3: 323-326. [ Links ]
Rubio, B., M. Nombela, F. Vilas, I. Alejo, E. García-Gil & O. Pazos. 1995. Distribución y enriquecimiento de metales pesados en sedimentos actuales de la parte interna de la Ría de Pontevedra. Thalassas 11: 35-45. [ Links ]
Sadiq, M. 1992. Toxic metal chemistry in marine environments. Marcel, Nueva York, EEUU. Salbu B., T. Krekling & D. Oughton. 1988. Characterization of radioactive particles in the environment. Analyst. 123: 843-849. [ Links ]
Skrabal, S., J. Donat & D. Burdige. 2000. Pore distributions of dissolved copper, and copper-complexing ligands in estuarine and coastal marine sediment. Geochim. Cosmochim. Acta 64: 1843-1857. [ Links ]
Sulkowski, M. & A. V. Hirner. 2006. Element fractionation by sequential extraction in a soil with high carbonate content. Appl. Geochem. 21: 16-28. [ Links ]
Ure, A., P. Quevauviller, H. Muntau & B. Griepink. 1993. Speciation of heavy metals in soil and sediment. An account of the improvement and harmonization of extraction techniques undertaken under auspicies of the BCR of the Commission of the European Community. Int. J. Environ. Anal. Chem. 52:135-151. [ Links ]
Wedepohl, K. 1995. The composition of the continental crust. Geochim. Cosmochim. Acta 59: 1217-1232. [ Links ]
Luisa Rojas de Astudillo. Departamento de Química / Instituto de Investigaciones en Biomedicina y Ciencias Aplicadas
Alfredo Diaz. Departamento de Química
Recibido 19-VII -2009. Corregido 15-I-2010. Aceptado 12-VI -2010.