Revista de Biología Tropical
versión On-line ISSN 0034-7744versión impresa ISSN 0034-7744
Rev. biol. trop vol.57 no.1-2 San José mar./jun. 2009
Jonathan A. Guzmán, Guillermo DElía & Juan Carlos Ortiz
Departamento de Zoología, Facultad de Ciencias Naturales y Oceanográficas, Universidad de Concepción. Casilla 160-C. Concepción, Chile; jonathanguzman@udec.cl
Abstract: Geographic variation of the fox Lycalopex culpaeus (Mammalia, Canidae) in Chile: taxonomic implications. We studied the geographic variation of skulls of Lycalopex culpaeus using qualitative and quantative analyses. The sampling area covered Chile, from its northern portion, to Tierra del Fuego and the neighbouring Hoste island, as well as part of Argentina. Five subespecies are currently recognized from this large area. We found two morphotypes that are segregated geographically. Both groups mostly differ by morphometric attributes, followed by qualitative features. Specimens from northern Chile (Tarapacá and Antofagasta) have small skulls, short rostrum, a liriform sagital zone, and lack the interparietal crest. The second group is formed by specimens from north-western and central Argentina, central-south Chile, Patagonia, and the austral islands of Tierra del Fuego and Hoste. This group presents a strong sagital crest, large rostrum, and a large skull. Our results agree with observed patterns of mitochondrial DNA variation. We propose to retain the name L. c. andinus for the populations of northern Chile and to synonymize L. c. magellanicus, L. c. lycoides, and L. c. smithersi under L. c. culpaeus. Rev. Biol. Trop. 57 (1-2): 421-432. Epub 2009 June 30.
Key words: Lycalopex culpaeus, Carnivora, taxonomy, geographical variation, subspecies.
Lycalopex (Burmeister, 1854) es un género de cánidos endémico de América del Sur en el que actualmente (e.g., Sillero-Zubiri et al. 2004, Zrzavý y Ricanková 2004, Wozencraft 2005) se reconocen las siguientes especies: L. culpaeus (Molina, 1782), L. griseus (Gray, 1837), L. sechurae (Thomas, 1900), L. fulvipes (Martin, 1837), L. gymnocercus (G. Fischer, 1814) y L. vetulus (Lund, 1842).
En Chile habitan las especies L. griseus, L. fulvipes y L. culpaeus (Osgood 1943, Pine et al. 1979). La última es conocida vernacularmente como zorro culpeo, zorro colorado o zorro andino (Novaro 1997). En la descripción original, de acuerdo a los estándares de la época, Molina (1782) no designó un holotipo y no hizo referencia al material estudiado, señalando que correspondía a "un perro selvático o mejor dicho un gran zorro, con una cola peluda parecida a la del perro ordinario, además su voz es débil pero similar al ladrido del perro". Este cánido se distribuye a ambos lados de los Andes desde el sur de Colombia hasta las planicies patagónicas e islas del extremo sur de América del Sur (Osgood 1943, Langguth 1975, Berta 1987). La isla Hoste, al sur del Canal Beagle, corresponde a la localidad de registro más austral (Markham 1971a, Sielfeld 1977). En esta amplia distribución, el culpeo habita una gama variada de ecosistemas, incluyendo los valles transversales del desierto de Atacama, la planicie andina (altiplano) sobre los 4 000 m de altitud, desierto de monte, estepa patagónica y áreas boscosas del oeste y sur de Sudamérica (Housse 1953, Medel y Jaksic 1988, Novaro 1997).
Cabrera (1931, 1957) y Wozencraft (2005) reconocen las siguientes subespecies de L. culpaeus: L. c. reissii (Hilzheimer), 1906 en Ecuador; L. c. andinus (Thomas, 1914) de los Andes de Perú, Bolivia, norte de Chile y Argentina; L. c. smithersi (Thomas, 1914) de la provincia de Córdoba en Argentina; L. c. culpaeus (Molina, 1782) en Chile central; L. c. magellanicus (Gray, 1837) en el extremo sur de Chile y Argentina; y L. c. lycoides (Philippi, 1896) confinada a Tierra del Fuego e islas aledañas. Durante el siglo pasado fueron varios los autores que consideraron dudosa la distinción de algunos de estos taxones (e.g., Kraglievich 1930, Osgood 1943, Crespo y de Carlo 1963, Markham 1971b), señalando que la escasez de especimenes disponible es el factor limitante para poner a prueba los niveles de diferenciación de éstos y así delimitar su distribución. Cabe destacar que estos taxones han sido erigidos, fundamentalmente, sobre la base de medidas dento-craneales y coloración del pelaje. Lycalopex c. smithersi, fue descrita por Thomas (1914b) en base a la coloración de una piel curtida. También, destaca L. c. andinus, cuya descripción se basó en tres especímenes, donde Thomas (1914a) sólo proporciona las dimensiones dento-craneales del holotipo. Similarmente, la forma nominal L. c. culpaeus no presenta un espécimen tipo y su localidad típica fue restringida a Santiago de Chile por Cabrera (1931) luego de un siglo y medio de la descripción original hecha por Molina (1782).
El objetivo de este trabajo es analizar cómo se estructura geográficamente la variación a nivel cráneo-dentario en poblaciones chilenas de L. culpaeus para así evaluar el grado de diferenciación de los distintos taxones subespecíficos actualmente reconocidos de este cánido para Chile.
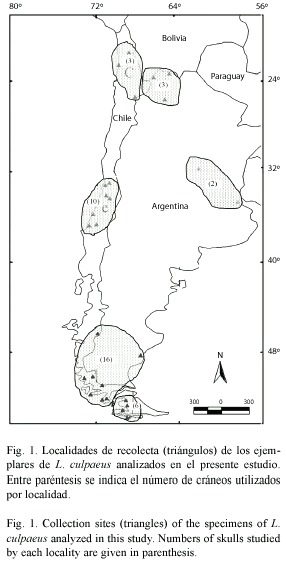
Materiales y métodos
Muestras y procedencia: Se trabajó sólo con individuos adultos. Según Zunino et al. (1995) y Prevosti y Lamas (2006) un individuo fue considerado adulto sólo cuando la sutura basioccipital/basisfenoides se encontraba fusionada. Se analizó 40 cráneos de L. culpaeus de 29 localidades que cubren en gran medida la distribución en Chile y parcialmente la de Argentina. Las muestras se agruparon con base en cercanía: 1) norte de Chile: altiplano de las regiones de Tarapacá y Antofagasta y litoral costero de Antofagasta (N =3); 2) noroeste argentino: (Jujuy) (N=3); 3) centro-sur chileno: regiones Metropolitana, valparaíso, Maule y BíoBío (N=10); 4) centro argentino: Córdoba y Buenos Aires (N=2); 5) Patagonia: Aysén y Magallanes en Chile y provincia de Santa Cruz en Argentina (N=16); y 6) islas australes: Tierra del Fuego e isla Hoste (N=6) (Fig. 1, Apéndice 1). Los cráneos examinados se encuentran depositados en las colecciones del Museo Argentino de Ciencias Naturales, Buenos Aires (MACN), Museo Nacional de Historia Natural de Chile, Santiago (MNHN), Museo de Historia Natural de Valparaíso, Valparaíso (MHNV), Museo de Zoología, Universidad de Concepción, Concepción (MZUC-UCCC) y Colección Zoológica del Instituto de la Patagonia de la Universidad de Magallanes, Punta Arenas (CZIP) (Apéndice 1).
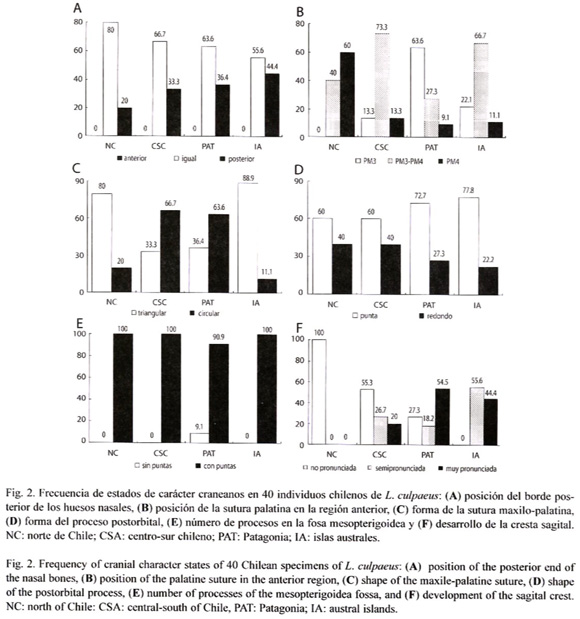
Caracteres cualitativos: Los siguientes seis caracteres cualitativos se evaluaron en los individuos de Chile: (1) forma de la sutura maxilo-palatina: a) triangular, b) redondeada; (2) posición de la sutura palatina en la región anterior: a) a la altura del PM3, b) entre PM3 – PM4, c) a nivel del PM4; (3) fosa mesopterigoidea: a) sin proceso óseo, b) con proceso óseo; (4) forma del proceso postorbital: a) en punta, b) redondeado; (5) posición del borde posterior de los huesos nasales: a) anterior al hueso maxilar, b) a nivel del hueso maxilar, c) posterior al hueso maxilar; (6) cresta sagital: a) no pronunciada, b) poco pronunciada, c) muy pronunciada. A nivel de dentición se contabilizo la cantidad de cúspides en el premolar cuatro (P4), molar uno (M1), y molar dos (M2) de la maxila y del molar uno (m1), dos (m2) y tres (m3) del dentario.
Análisis cuantitativo: Se evaluó 26 medidas dento-craneales siguiendo a Zunino et al. (1995): 1) longitud condilobasal (lcb); 2) longitud palatina (lp); 3) longitud mínima rostral (lmr); 4) longitud facial (lf); 5) longitud bular (lb); 6) longitud corona maxilar (lcm); 7) longitud desde P4 a M2; 8) altura mínima rostral (amr); 9) altura del cráneo (ac); 10) constricción interorbital (ci); 11) constricción postorbital (cp); 12) ancho rostral a nivel de los caninos (arc); 13) ancho rostral a nivel del primer molar superior (arpms); 14) ancho zigomático (az); 15) ancho mastoidal (am); 16) ancho del cráneo a la altura de los parietales (ac); 17) ancho a través de los cóndilos occipitales (aco); 18) ancho entre el proceso postglenoides (app); 19) longitud del cuarto premolar superior (lp4); 20) ancho del cuarto premolar superior (ap4); 21) longitud del primer molar superior (lm1); 22) ancho del primer molar superior (am1); 23) altura rostral a nivel de los premolares superiores 2 y 3 (arp2 -P3); 24) longitud mandibular (lm); 25) longitud de la corona mandibular (lcm); 26) longitud desde el primer al tercer molar superior (lM1-M3). Finalmente, se estimó la proporción del hocico (Thomas 1914a) dividiendo la distancia órbita-premaxilar sobre la longitud cóndilobasal del cráneo (Kraglievich 1930). Todas las mediciones se hicieron al lado izquierdo del cráneo y mandíbula con un calibre digital Mitutoyo (± 0.01).
Análisis: La normalidad de las variables dento-craneales se evaluó con la prueba de Kolmogorov-Smirnov y la homogeneidad de varianza con la prueba de Levene (Sokal y Rohlf 1995). Los datos se entregan como promedio, desviación estándar y escalas de valores por variables y población (Cuadro 1). El dimorfismo sexual se evaluó con la muestra mayor que correspondió a la localidad de Magallanes (11 cráneos) para lo cual se llevó a cabo una prueba de permutaciones con 10 000 interaciones. El estadístico no evidenció diferencias significativas (p>0.05) entre machos y hembras, lo que permitió analizar la totalidad de cráneos en su conjunto. El porcentaje de variación en la morfometria craneal se obtuvo por medio del coeficiente de variación (CV) el cual fue calculado para las muestras centro-sur de Chile, Patagonia e islas australes. Para el norte de Chile, noroeste y zona central de Argentina no fue estimado debido al bajo número de especimenes estudiados. Con las variables cuantitativas se realizó un análisis de componentes principales (ACP). La significancia de los grupos sobre los componentes I y II del ACP, se evaluó por medio de un análisis multivariado de varianza (ANMUDEVA), utilizando como datos de entrada las variables que explican la mayor parte de la varianza de los grupos. Diferencias pareadas se estimaron con el test a posteriori de Tukey. Como una forma adicional de evaluar la diferenciación de los grupos encontrados en el ACP, se realizó un análisis discriminante con todas las variables pero agrupando los datos con base en los conjuntos obtenidos del ACP. Todos los análisis estadísticos se realizaron en los programas Statistica 6.0 (StatSoft inc. 1998) y Rundom Proyects 1.1 (Jadwiszczak 2003).
Resultados
Caracteres cualitativos: Los ejemplares de Lycalopex culpaeus no mostraron diferencias en el número de cúspides molares a lo largo de su distribución chilena. Los restantes seis caracteres evaluados son variables; sin embargo, sus patrones geográficos de variación no son coincidentes (Fig. 2). Las diferencias constatadas entre grupos geográficos son, fundamentalmente, en términos de diferencias en las frecuencias de distintos estados de carácter. El grupo norte, el cual incluye menos localidades y menos especimenes, es el más uniforme al presentar individuos sin cresta interparetial, con los nasales terminando a la altura del maxilar y con el paladar terminando a la altura del PM3-PM4 o del PM4. En estos caracteres los restantes grupos presentan, aunque variando en frecuencia, todos los estados de caracteres registrados. Los grupos centro-sur, patagónico y de las islas australes presentan una tendencia a cráneos más robustos dados, fundamentalmente, por una cresta sagital más pronunciada. Cabe destacar que en dos caracteres el conjunto de las islas australes es más homogéneo que los restantes grupos; los individuos isleños presentan una sutura premaxilar con forma triangular y un proceso postorbital en punta. Los especímens de los restantes grupos además de presentar dichos estados de carácter, también muestran suturas premaxilares cuadradas y procesos postorbitrales redondeados. De la misma forma, algunos animales de Patagonia carecen de procesos en la fosa mesopterigoidea, mientras que todos los individuos de las restantes grupos presentan dichos accidentes. Tomados en su conjunto estos resultados indican la existencia de dos morfotipos principales en la muestra estudiada. Uno, constituido por el grupo norte, que se caracteriza por individuos con cráneos más gráciles; el segundo morfo-tipo, constituido por los grupos geográficos centro-sur, patagónico e islas australes, es de cráneos más robustos.
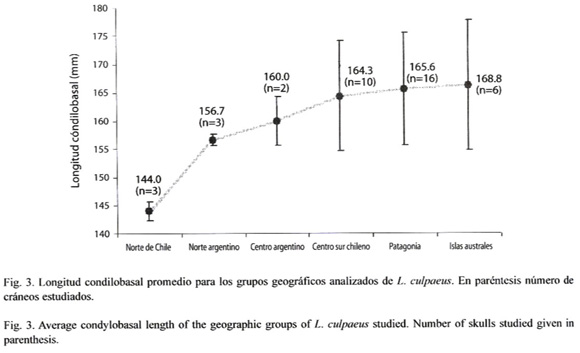
Caracteres cuantitativos: Tanto la distribución de los datos como la homogeneidad de varianza no fueron significativamente diferentes de la normalidad y homogeneidad (p < 0.05). La longitud cóndilobasal promedio de los cráneos fue de 163.2 ± 10.9 mm, evidenciándose un aumento de tamaño a latitudes mayores, donde un individuo de la zona del río Loa en el norte chileno (142.0 mm.) y otro de Tierra del Fuego (182.0 mm.), fueron los extremos de la escala de variación observado para esta variable. Para ambos extremos (norte de Chile e islas australes) la longitud condilobasal promedio fue de: 144.0 mm (± 1.7: n=3) y 168.7 mm (± 12.0: n=6) respectivamente, y entre éstos límites le siguen los individuos del noroeste argentino (156.7 ± 1.2 mm); centro argentino (160.0 ± 4.2 mm); centro sur chileno (164.3 ± 9.7 mm) y Patagonia (165.6 ± 9.9 mm) (Fig. 3, Cuadro 1). El ancho del cráneo fue la variable que menos fluctuó (CV=3.0%), mientras que la amplitud rostral a nivel de los caninos fue la más variable (CV=9.3%) (Cuadro 1). Respecto a la proporción del hocico con la longitud cóndilobasal, los mayores valores fueron 44.7% para los individuos del noroeste argentino, seguidos por los del centro-sur chileno (44.2%), Patagonia (44.1%), islas australes (43.9%) y finalmente norte chileno (43.9%) (Cuadro 2).

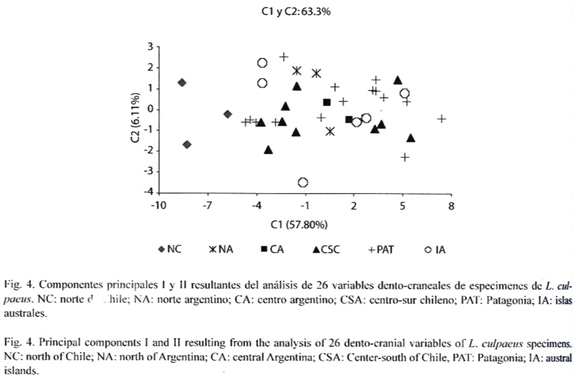
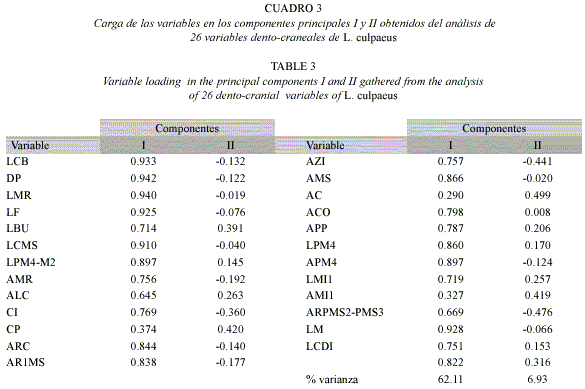
El análisis de componentes principales (ACP) revela la existencia de dos conjuntos discretos que no se solapan geográficamente (Fig. 4). Grupo A: formado por los individuos del norte chileno (regiones de Tarapacá y Antofagasta), y Grupo B: constituido por el resto de los especimenes estudiados (noroeste y centro argentino, centro-sur chileno, Patagonia e islas australes). Los Componentes 1 y 2 explican el 69.04 % de la varianza total observada. La mayoría de las variables que mejor explican la variación a lo largo del componente uno (62.11 %) son longitudes, incluyendo lcb, lp, lmr, lf, lcms, lpm4-m2, arc, ar1ms, am, lpm4, apm4, lm, lmi1-mi3 (Cuadro 3). El ANMUDEvA mostró diferencias significativas entre el grupo A y B en 11 de estas 13 variables (Lambda de Wilks=0.21; p = 0.000001); los anchos, arc y am, no fueron significativamente diferente entre los dos grupos. De forma similar, el análisis discriminante muestra diferencias significativas entre los grupos A y B (Lambda de Wilks= 0.12; p=0.011) recobrados con el ACP; más aún, ambos conjuntos (A y B) presentan un 100% de asignación correcta.
Discusión
Considerado conespecifico con L. gymnocercus (Clutton-Brock et al. 1976) y posteriormente como especie plena (Zunino et al. 1995), cincuenta y tres taxones (e.g. Canis amblyodon Philippi, 1903, C. albigula Philippi, 1903, C. ferrugineus Huber, 1925 han sido acuñados para contener a individuos que actualmente se adscriben como pertenecientes a la especie biológica nominada como Lycalopex culpaeus (Zunino et al. 1995). Esta plétora de nombres remarca la compleja historia taxonómica de esta especie (Cabrera 1931, 1958, Osgood 1943, van Gelder 1978, Muñoz-Pedreros y Yañez 2000, Díaz y Lucherini 2006). Cabrera (1931) y el "Specialist Canids Group" (2004) reconocen seis subespecies de culpeo, de las cuales cuatro habitan en Chile.
Estudios previos se han referido a la variación intra e interpoblacional del tamaño corporal y craneal del culpeo (Thomas 1914a, Kraglievich 1930, Fuentes y Jaksic 1979, Johnson y Franklin 1994a, Zunino et al. 1995). Johnson y Franklin (1994a) señalan que en el extremo sur continental de Chile (Torres del Paine, Magallanes) los machos de Lycalopex culpaeus son significativamente (p=0.007) más pesados que las hembras. Sin embargo, nuestra muestra de Magallanes no mostró diferencias significativas intersexuales asociadas al tamaño del cráneo (p>0.05), coincidiendo con lo descrito para Lycalopex griseus (Zunino et al. 1995) y L. gymnocercus (Prevosti y Lamas 2006) en Argentina, Cerdocyon thous del norte y centro-este de Sudamérica (Courtenay y Maffei 2004) y Vulpes vulpes y Canis latrans de la región Holartica (Waithman y Roest 1977, Gingerich y Winkler 1979, Gese y Bekoff 2004). La naturaleza de las diferencias entre nuestros resultados y los de Johnson y Franklin (1994a) no son por el momento claras.
En relación a la variación en tamaño, Thomas (1914a) señala que los cráneos de individuos más septentrionales son más pequeños, especialmente en la longitud rostral, que los ejemplares del sur. Este patrón fue posteriormente corroborado por Fuentes y Jaksic (1979) en relación al tamaño corporal. Nuestros resultados apuntan en la misma dirección (Fig. 3). Los individuos del norte chileno tienen cráneos menos voluminosos y más chicos, además presentan la sutura maxilo-palatina más triangular y un casi nulo desarrollo de la cresta interparietal y que en la región posterior describe una angosta y tenue área sagital "liriforme". Los restantes cráneos aquí estudiados aumentan en tamaño a medida que las localidades de su recolecta son más australes y son relativamente homogéneos cualitativamente. Éstos se caracterizan por rostros más extendidos y la fuerte cresta interparietal que finaliza en una zona "liriforme" más pronunciada. Zunino et al. (1995) sugieren que el desarrollo de la cresta interparietal se asocia al tamaño corporal de los individuos, siendo un carácter de escaso valor taxonómico. No obstante, nosotros encontramos que el desarrollo de la cresta interparietal permite diferenciar a los individuos del norte de Chile respecto a los de poblaciones más australes. Estos grupos cualitativos se ven reforzados en análisis cuantitativos que indican que las poblaciones del norte de Chile se diferencian significativamente de aquellas de Chile centro-sur, centro y noroeste de Argentina, Patagonia e islas australes. Es oportuno recordar que nuestro muestreo presenta una disyunción en la zona centro-norte de Chile (Regiones III y IV) (Fig. 1).
Los morfogrupos aquí descritos, coinciden geográficamente con filogrupos obtenidos con base en análisis de variación de ADN mitocondrial por Yahnke et al. (1996). Dicho estudio encontró que los haplotipos obtenidos en poblaciones del extremo norte de Chile (precordillera de Tarapacá, Putre) se diferencian genealógicamente de aquellos de las poblaciones del centro-sur de Chile. La congruencia en los patrones de variación morfológica y del ADN mitocondrial es relevante al reconocer la existencia de dos poblaciones de culpeos chilenos, una al norte del país (población A) y la segunda en el centro-sur y extremo sur de Chile incluyendo zonas aledañas de Argentina y las islas del extremo sur del continente (población B).
Desde el punto de vista taxonómico, nuestros resultados permiten plantear cambios formales sobre el estatus de algunos taxones, al reconocer solamente dos, y no cuatro, subespecies de culpeo en Chile. Consideramos a L. c. lycoides, L. c. magellanicus y L. c. smithersi (grupo B en este estudio) como sinónimos formales de L. c. culpaeus. Hacemos notar que las poblaciones del noroeste argentino que hasta el momento son asignadas a L. c. andinus, son indistinguibles de L. c. culpaeus, por lo que entonces son asignados a esta forma. En vista de lo anterior, tentativamente referimos a la forma del norte de Chile (grupo A) a la subespecie L. c. andinus; sin embargo, remarcamos que la pertinencia de usar este nombre taxonómico debe ser puesta a prueba mediante el estudio de más especimenes a lo largo de la distribución de este taxon, incluyendo especimenes provenientes de la localidad típica (Bolivia, Oruro, Esperanza). De la misma forma destacamos la necesidad de integrar al análisis más ejemplares, especialmente de localidades fuera de Chile, para poner a prueba la hipótesis taxonómica aquí planteada y para analizar el grado de diferenciación de la subespecie L. c. reissii que no fue incluida en este trabajo y L. c. smithersi, de la cual se examinó una muestra reducida.
Lycalopex c. culpaeus y L. c. andinus presentan diferencias en sus dietas. En Patagonia el primero consume en mayor medida carne y un escaso número de invertebrados y plantas (Medel y Jaksic 1988, Jaksic 1997); en el norte de Chile L. c. andinus consume principalmente ítemes pequeños (semillas, insectos y pequeños mamíferos) (Marquet et al. 1993, Guzmán et al. 2007).
Finalmente es de destacar que patrones similares de estructura geográfica intraespecífica al aquí reportando para L. culpaeus han sido encontrado analizando secuencias del genoma mitocondrial en Lama guanicoe (González et al. 2006) y Vicugna vicugna (Marín et al. 2007). Futuros estudios clarificaran las causas, seguramente de naturaleza histórica, atrás de la generación de patrones similares de variación geográfica en estos tres linajes codistribuidos.
Agradecimientos
Los autores agradecen a los curadores y personas que otorgaron todas las condiciones para acceder al material estudiado: Jorge Artigas y Elvira Solar del Museo zoológico de la Universidad de Concepción; Claudio Venegas, Magali Vera y Jaime Carcamo del instituto de la Patagonia en Punta Arenas; José Yánez del Museo de Historia natural de Chile; y Sergio Quiroz Jara de la sección de ciencias naturales del Museo de Historia natural de Valparaíso; y Olga Vaccaro de la división de mastozoología del Museo Argentino de ciencias naturales en Buenos Aires. También expresamos nuestra gratitud a Daniel González, Olivia Vergara y Carlos Zamora por su desinteresada colaboración durante distintas etapas de este trabajo. Finalmente y de manera muy especial reconocemos a Walter Sielfeld Kowald, quien siempre incentivó al primer autor estudiar este grupo de carnívoros.
Resumen
Mediante análisis cualitativos y cuantitativos, se estudió la variación geográfica del cráneo de Lycalopex culpaeus en Chile (desde Tarapacá a la islas australes), y de algunas poblaciones argentinas. En dicha distribución se reconocen cinco de las seis subespecies del culpeo. Los resultados muestran dos grupos morfológicos geográficamente segregados; los mismos se diferencian principalmente por atributos morfométricos, y secundariamente por caracteres cualitativos. individuos del norte chileno (Tarapacá y Antofagasta) presentan cráneos pequeños, poco desarrollados, hocico levemente corto, ausencia de cresta interparietal y una tenue zona sagital "liriforme". Por otra parte, los individuos del noroeste y centro argentino, centro sur chileno, Patagonia e islas australes (islas de Tierra del Fuego y Hoste) (grupo B), no muestran diferencias significativas en su morfometría dento-craneal. En el grupo B destacó una fuerte cresta interparietal y zona sagital, hocicos prolongados y cráneos de mayor tamaño que los del norte chileno. Nuestros resultados coinciden con estudios de patrones de variación en el ADN mitocondrial de cánidos de Chile. Por lo tanto, se propone mantener el nombre L. c. andinus para las poblaciones del norte de Chile y sinonimizar los taxones L. c. magellanicus, L. c. lycoides y L. c. smithersi bajo la forma L. c. culpaeus.
Palabras clave: Lycalopex culpaeus, Carnivora, taxonomía, subespecies, variación geográfica, culpeo.
Referencias
Berta, A. 1987. Origin, diversification and zoogeography of the South American Canidae. p. 455- 471. In B.D. Patterson, & R.M. Timm (eds). Studies in neotropical mammalogy: essays in honor of Philip Hershkovitz. Fieldiana, Zoology 39: 455- 471. [ Links ]
Crespo, J.A. & J.M. de Carlo. 1963. Estudio ecológico de una población de zorros colorados. Rev. Mus. Argent. Ienc. Nat. Bernardino Rivadavia Inst. Nac. Investig. Cienc. Nat. 1: 1-55. [ Links ]
Cabrera, A. 1931. On some South American canine genera. J. Mammalogy 12: 54-67. [ Links ]
Cabrera, A.1958. Catálogo de los Mamíferos de América del Sur. Rev. Mus. Argent. Cienc. Nat. Bernardino Rivadavia Inst. Nac. Investig. Cienc. Nat 4: 1-308. [ Links ]
Courtenay, O. & L. Maffei. 2004. Crab-eating fox Cerdocyon thous (Linnaeus, 1766), p. 32-38. ln C., Sillero-Zubiri, M., Hoffmann & D.W., McDonald (eds.). 2004. Canids: Foxes, Wolves, Jackals and Dogs. Status Survey and Conservation Action Plan. IUCN/SSC Canid Specialist Group. Gland, Suiza y Cambridge, Inglaterra. [ Links ]
Cluton-Brock, J., Corbet, & M. Hills. 1976. A review of the family Canidae, with a classification by numerical methods. Bull. Brit. Mus. (Nat. Hist.), Zoology 29: 119-199. [ Links ]
Díaz, M. & M. Lucherini. 2006. Orden Carnívora, Familia Canidae. In R.M., Barquez., M.M., Díaz & R.A., Ojeda (eds). Mamíferos de Argentina, Sistemática y Distribución. Sociedad Argentina para el Estudio de los Mamíferos. Tucumán, Argentina. [ Links ]
Fuentes, E.R. & F.M. Jaksic. 1979. Latitudinal size variation of chilean foxes: test of alternative hypotheses. Ecology 60: 43-47. [ Links ]
Gese, E.M. & M. Bekoff. 2004. Coyote Canis latrans (Say, 1823), p. 81-87 ln C., Sillero-Zubiri, M., Hoffmann & D.W., McDonald (eds.). 2004. Canids: Foxes, Wolves, Jackals and Dogs. Status Survey and Conservation Action Plan. IUCN/SSC Canid Specialist Group. Gland, Suiza y Cambridge, Inglaterra. [ Links ]
Gingerich, P.D. & D.A. Winkler. 1979. Patterns of variation and correlation in the dentition of the red fox, Vulpes vulpes. J. Mammalogy 60: 691-704. [ Links ]
González, B., E. Palma, B. Zapata & J. Marín. 2006. Taxonomic and biogeographical status of guanaco Lama guanicoe (Artiodactyla, Camelidae). Mammal Review 36: 157-178. [ Links ]
Guzmán, J. W. Sielfeld & M. Ferrú. 2007. Dieta de Lycalopex culpaeus (Mammalia; Canidae) en el extremo norte de Chile (Región de Tarapacá). Gayana 71: 1-7. [ Links ]
Housse, R. 1953. Animales salvajes de Chile en su clasificación moderna: su vida y sus costumbres. Universidad de Chile, Santiago, Chile. 189 p. [ Links ]
Jaksic, F.M. 1997. Ecología de los vertebrados de Chile. Universidad Católica, Santiago, Chile. 262 p. [ Links ]
Johnson, W.E. & W.L. Franklin. 1994a. Role of the body size in the diets of simpatric gray and culpeo foxes. J. Mammalogy 75: 163-174. [ Links ]
Jadwiszczak, P. 2003. Rundom Proyects: An aplication for randomization and bootstrap testing, version 1.1. [ Links ]
Kraglievich, L. 1930. Craneometría y clasificación de los cánidos sudamericanos, especialmente los argentinos, actuales y fósiles. Physis 10: 35-73. [ Links ]
Langguth, A. 1975. Ecology and evolution in the south american canids. p. 192- 206 In M. W. Fox (eds). The wild canids, their systematic, behavioral ecology and evolution. Van Nostrand Reinhold Co, Nueva York, EEUU. xviii + 508 pp. [ Links ]
Markham, B.J. 1971a. Presencia del "culpeo" (Dusicyon culpaeus) en la isla Hoste, Tierra del Fuego. An. Inst. Patagon. 2: 164-165. [ Links ]
Markham, B.J. 1971b. Notas sobre las subespecies del "culpeo" (Dusicyon culpaeus) en Magallanes. An. Inst. Patagon. 2: 166-169. [ Links ]
Marin, J.C., C.S., Casey, M. Kadwell, K. Yaya, D. Hoces, J. Olazabal, R. Rosadio, J. Rodriguez, A. Spotorno, M.W. Bruford & J.C. Wheeler. 2007. Mitochondrial phylogeography and demographic history of the vicuña: implications for conservations. Heredety 99: 70 – 80. [ Links ]
Marquet, P.A. L.C Contreras, J.C. Torres-Mura, S .I. Silva & F.M. Jaksik. 1993. Food habits of Pseudalopex foxes in the Atacama Desert, pre-andean rages and the high Andean plateau of the northern most Chile. Mammalia 57: 130-135 [ Links ]
Medel, R.G. & F.M. Jaksic, 1988. Ecología de los cánidos sudamericanos: una revisión. Rev. Chil. Hist. Nat. 61: 67-79. [ Links ]
Molina, G.A. 1782. Saggio sulla storia naturale del Chili. Stamperia di S. Tommaso d´ Aquino, Bologna, Italia. 367 p. [ Links ]
Muñoz-Pedreros A., J. Yañez. 2000. Mamíferos de Chile. Ediciones CEA. Valdivia, Chile. 464 P. [ Links ]
Novaro, A.J. 1997. Pseudalopex culpaeus. Mamm. Species 558: 1-8. [ Links ]
Osgood, W.H. 1943. The mammals of Chile. Field Mus. Nat. Hist., Zool. Ser. 30: 1-268. [ Links ]
Prevosti, F.J. & L. Lamas. 2006. Variation of cranial and dental measurements and dental correlations in the pampean fox (Dusicyon gymnocercus). J. Zoology 270: 636-649. [ Links ]
Pine, E.T., R.H., S.D. Miller & M.L. S.chamberger. 1976. Contributions to the mammalogy of Chile. Mammalia 43: 339-376. [ Links ]
Sielfeld, W.H. 1977. Reconocimiento macrofaunistico terrestre en el área del seno Ponsonby (isla Hoste). An. Inst. Patagon. 8: 275 -296. [ Links ]
Sillero-Zubiri, C. M. Hoffmann & D.W. McDonald, 2004. Status Survey and Conservation Action Plan Canids: Foxes, Wolves, Jackals and Dogs. IUCN/SSC Canid Specialist Group. Gland, Suiza y Cambridge, Inglaterra. [ Links ]
Sokal, R. & Rohlf F.J. 1995. Biometry: the principles an practice of Statistics in Biological Research. W. H. Freeman and Company, Nueva York, EEUU. 832 p. [ Links ]
Thomas, O. 1914a On various South-American mammals. Ann. Mag. Nat. Hist. 13: 345-363. [ Links ]
Thomas, O. 1914b. Three new S. American Mammals. Ann. Mag. Nat. Hist.8, vol XIII. [ Links ]
Van Gelder, R.G. 1978. A review of canid clasification. Am. Mus. Novitates 2646: 1-10. [ Links ]
Wayne, R.K., E. Geffen, D.J. Girman, K.P. Koepfli, L.M. Lau, & C.R. Marshall. 1997. Molecular Systematics of Canidae. Syst. Biol. 46: 622-653. [ Links ]
Waithman, J. & A. Roest, 1977. A taxonomic study of the kit fox, Vulpes macrotic. J. Mammalogy 58: 157-164. [ Links ]
Wozencraft, C. 2005 Order Carnivora, Familia Canidae, p. 573-586. In: E . Wilson, & D. Reeder. 2005. Mammal Species of the world, a taxonomy and geographic reference. Volume I and II. Johns Hopkins, Baltimore. EEUU. 2142 p. [ Links ]
Yahnke, C.J. W.E. Johnson, E. Geffen, D. Smith, F. Hertel, M.S. Roy, C.F. Bonacic, T.K. Fuller, B. Van Valkenburgh & R.K. Wayne. 1996. Darwins fox: a distinct endagered species in a vanishing habitat. Conservation Biology 10: 366-375. [ Links ]
Zrzavý, J. & V. Ricanková. 2004. Phylogeny of Recent Canidae (Mammalia, Carnivora): Relative reliability and utility morphological and molecular datasets. Zool. Scripta 33: 311-333. [ Links ]
Zunino, G.E., O.B., Vaccaro, M. Canevari & A.L. Gardner. 1995. Taxonomy of the genus Lycalopex (Carnivora: Canidae) in Argentina. Pro. Biol. Soc. Washington 108: 729-747. [ Links ]
Listado de especimenes de Lycalopex culpaeus analizados en este estudio. Los mismos se encuentran depositados en las siguientes colecciones. ARGENTINA: Museo Argentino de Ciencias Naturales, Buenos Aires (MACN). CHILE: Museo Nacional de Historia Natural de Chile, Santiago (MNHN); Museo de Historia Natural de Valparaíso, Valparaíso (MHNV); Museo Zoológico Universidad de Concepción, Concepción (MZUC -UCCC); Colección Zoológica instituto de la Patagonia de la Universidad de Magallanes, Punta Arenas (CZIP). Número de campo de Jonathan Guzmán (JG), Walter Sielfeld (WS) y Daniel González (DG). (JG, WS y DG; especimenes a ser depositados en el Museo Zoológico Universidad de Concepción, Concepción-Chile).
NOROESTE ARGENTINO: Provincia de Jujuy: Abra Blanca (MACN 38039, MACN 4041); Lizoite (MACN 41055).
CENTRO ARGENTINO: Provincia de Buenos Aires (MACN 25.128); Provincia de Córdoba, Córdoba (MACN 21.899).
NORTE DE CHILE: Región de Tarapacá, Salar del Huasco (JG-002); Región de Antofagasta, Desembocadura Río Loa (WS-001); Altiplano, Socompa (DG-002).
CENTRO-SUR CHILENO: Chile central (MHNv 298); Región de valparaíso, San Felipe (MZUC – UCCC 25308); Palmas de Ocoa (MNHN 506); Región Metropolitana, Lo Lisboa (MNHN 505); Región del Maule, Cauquenes (MZUC – UCCC 7524, MZUC – UCCC 7525; MZUC – UCCC 7526; MZUC – UCCC 7527); Región del Biobio, Provincia de Concepción, Florida (MZUC – UCCC 21745); Región del Biobio, Provincia de Ñuble, Pemuco (DG-001).
PATAGONIA: Provincia de Santa Cruz, Puerto San Julián (MACN 19221); Patagonia (MACN 3.68, MACN 7.42). Región de Aysén, Cochrane (JG-001); Región de Magallanes, Provincia de Magallanes, Estancia Palermo (CZIP 197), isla Riesco (CZIP 203, CZIP 205), Península de Brunswick (CZIP 202, CZIP 206, CZIP 207), Agua Fresca (CZIP 190), Primera Angostura (CZIP 209); Provincia de Ultima Esperanza, Cerro Castillo (CZIP 193, CZIP 195, CZIP 201), Río Serrano (CZIP 191).
ISLAS AUSTRALES: Provincia de Tierra del Fuego (Chile), Estancia Río Hondo (CZIP 210, CZIP 215), Bahía Parry (CZIP 212), Lago Blanco (CZIP 200); Provincia Antártica Continental Chilena, Isla Hoste (CZIP 213, CZIP 214).












 uBio
uBio 

