Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista de Biología Tropical
On-line version ISSN 0034-7744Print version ISSN 0034-7744
Rev. biol. trop vol.52 n.1 San José Mar. 2004
de susceptibilidad a Leishmania infantum y Leishmania mexicana
(Kinetoplastida: Trypanosomatidae)
Miguel Angel Minero1 , Misael Chinchilla2 , Olga Marta Guerrero2 & Alfredo Castro2
1 Departamento de Microbiología, Facultad de Medicina, Universidad de El Salvador. Fax: (503) 225-8822.
2 Centro de Investigación en Enfermedades Tropicales (CIET), Facultad de Microbiología, Universidad de Costa Rica. Fax: (506) 225-4384.
Recibido 28-X-2002. Corregido 18-X-2003. Aceptado 28-X-2003.
Abstract
Infection and multiplication of Leishmania infantum and L. mexicana inside of skin fibroblasts from hamsters, mice and rats was achieved. This process was demonstrated either by counting parasites inside the stained cells or by electronic microscopy studies. In addition multiplication rate differences in the cells from these rodent species were determined, for L. infantum as well as for L. mexicana. Parasite development in hamsters and mice fibroblasts was evident but there was not multiplication in rat cells showing that apparently they are refractory to Leishmania infection. These results suggest that the parasite affinity for each animal, as well as any intracellular environment resistance, could involve genetic factors in the parasite multiplication. On the other hand, presence of amastigote multiplication inside of parasitophorus vacuole, showed by electronic microscopy images, probes a true parasite transformation. Therefore it is suggested that fibroblasts could work as host cells for parasite survival and permanency in the infected animals.
Key words: Trypanosomatidae, Leishmania, cell culture, fibroblasts.
El término genérico de leishmaniasis se refiere a una parasitosis con diversas manifestaciones clínicas que se distribuyen en al menos 88 países alrededor del mundo, los cuales se ubican dentro de las zonas tropicales y subtropicales donde existe transmisión activa del agente etiológico (Grimaldi y Tesh 1993, Alvar et al. 1997). Tales manifestaciones clínicas han sido catalogadas en 3 síndromes: cutáneo, mucocutáneo y visceral, según sea el grado de compromiso de tejidos y órganos (Pearson y Queiroz-Sousa 1996). Este patrón clínico, sin embargo, tiene cada vez menos utilidad práctica pues se ha observado que factores como la inmunosupresión adquirida, la desnutrición y la constitución genética del individuo, se combinan con los factores de virulencia propios de las diferentes especies del parásito para producir cuadros clínicos que varían de persona a persona y de una zona geográfica a otra (Medrano et al. 1998, Wolday et al. 1999, Guerbouj et al. 2000).
Los parásitos del género Leishmania desarrollan su ciclo vital utilizando un insecto como vector y a un vertebrado como reservorio susceptible. Al alimentarse, el insecto inyecta formas flageladas llamadas promastigotos, los cuales penetran en macrófagos y células del sistema retículoendotelial donde se convierten en amastigotos. Estos últimos tienen la capacidad de multiplicarse y de infectar a otros tipos celulares donde pueden permanecer indefinidamente.
La capacidad de las células para inhibir la multiplicación parasitaria se ha correlacionado con diferencias en la resistencia natural de diferentes roedores, para lo cual se ha utilizado cultivos de macrófagos peritoneales como células blanco para la infección in vitro con Trypanosoma cruzi, Toxoplasma gondii y Besnoitia jellisoni (Chinchilla et al. 1995, 1996). Otras investigaciones, han informado de diferentes factores que intervienen en la multiplicación de Leishmania spp. en macrófagos peritoneales de Mesocricetus auratus (Molina y Chinchilla 1996), Mus musculus NGP (Méndez et al. 1996) y Rattus norvegicus (Bastardo et al. 1983).
Algunos investigadores han sugerido que al igual que sucede en macrófagos, el parásito puede invadir las células somáticas no inmunocompetentes del hospedero susceptible tales como los fibroblastos de la piel y sobrevivir de manera más efectiva en virtud de un medio ambiente interno menos hostil (Hervás-Rodriguez et al. 1996). No se relaciona aún a los fibroblastos dérmicos con la patología de la leishmaniasis aunque se sabe de su capacidad fagocítica (Segal 2001) y de la producción de compuestos antibacterianos luego del contacto con Interferón-g (Wang 1996).
En el presente estudio se desarrolla un modelo experimental in vitro de cultivo de fibroblastos de piel de tres especies de roedores, en contacto con promastigotos de Leishmania mexicana y L. infantum, con el fin de determinar si existen diferencias en cuanto a la susceptibilidad de infección por especies biológicamente disímiles del parásito y si aquellas se relacionan con la constitución genética de los individuos.
Material y métodos
Para estos experimentos se utilizaron animales de tres a cinco días de nacidos de las especies: hámster (Mesocricetus auratus), ratón blanco NGP (Mus musculus) y rata blanca Sprague Dowley (Rattus norvegicus), suministradas por el Laboratorio de Ensayos Biológicos (LEBi) de la Universidad de Costa Rica. Se siguió la metodología descrita por Chinchilla y Frenkel (1984), con algunas modificaciones. Brevemente, las crías se sacrificaron en cámara de éter y bajo condiciones de esterilidad se separó la piel, que a su vez fue sometida a tres ciclos de disgregación celular con tripsina al 0.25% a 37ºC y agitación mecánica por cinco a siete minutos cada vez. El sobrenadante obtenido se mezcló con el doble de volumen de Minimal
Essential Medium Eagle® (Sigma) con 10% de suero bovino fetal (MEM-10%SBF) para inactivar la tripsina. La suspensión celular se cultivó a 37ºC más 5-10% de CO2 y humedad hasta la formación de una monocapa. Una semana después, se tripsinisó por diez minutos para obtener una nueva suspensión celular que fue ajustada con hemocitómetro de Newbauer a una concentración aproximada de 1.0 x 105 fibroblastos por ml. Se colocaron 0.3 ml de esa suspensión en cada uno de cuatro cubreobjetos 22x22 mm estériles por caja de Petri y se incubaron por 24 horas a 37ºC más 5-10% de CO2 y humedad para luego lavar con solución de Hanks ® (Sigma).
Las suspensiones de promastigotos se hicieron en MEM-10% SBF a partir de cultivo en fase estacionaria en medio de Schneider ® (Sigma) a 32ºC de L. infantum aislada del primer caso humano en Costa Rica (Carrillo et al. 1999) y de L. mexicana (OCR) también aislada de una caso humano, en medio de Rugai a 25-28ºC. Los cultivos usados en estos experimentos provenían de animales infectados previamente, por los que eran de reciente aislamiento. A cada cubreobjeto se le agregó 0.1 ml de la suspensión del parásito, permaneciendo en contacto con los fibroblastos hasta 168 horas como máximo. Durante este intervalo,
se tomaron cubreobjetos a las 24, 72, 120 y 168 horas post-infección y se tiñeron con el colorante de Giemsa por siete minutos para revisar por microscopía de luz con objetivo de inmersión.
En cada uno de los cubreobjetos se contaron 500 células (CT) por sextuplicado, determinándose el número de células infectadas (CI) y el número total de amastigotos intracelulares (AT). Para obtener una correlación estadística de los datos para las células totales se dividió el cómputo de amastigotos intracelulares entre las células totales y se multiplicó por cien. Para las células infectadas se dividió el número de los amastigotos intracelulares entre las células infectadas y se multiplicó por cien. Todos estos datos se analizaron con la prueba "t" de Student en búsqueda de significancia estadística con un porcentaje de confianza del 95% ( p 0.05).
Simultáneamente se realizó un estudio ultraestructural de fibroblastos infectados, utilizando la técnica de baño de hielo y aumento de la cinética molecular de la solución por radiación del horno de microondas descrita por (Howood et al. 1990, Hernández y Guillén 2000). Del bloque de material obtenido se hicieron cortes finos para examinar al microscopio electrónico de transmisión (modelo Hitachi H7100).
Resultados
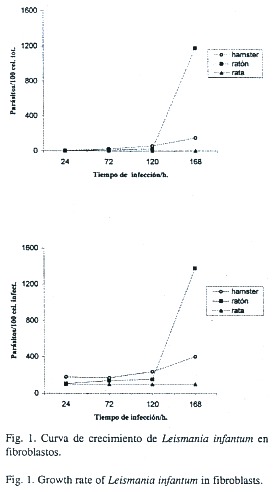
Los promastigotos de L. infantum y L. mexicana (OCR) inoculados en los cultivos de fibroblastos de piel de hámster, ratón y rata se comportaron en forma diferente con respecto a la afinidad hacia las células de los animales y la reproducción dentro de éstas a través del tiempo. El número de amastigotos de L. infantum a las 24 horas post-infección fue de 7.2, 4.0 y 0.2 en 100 fibroblastos totales de hámster, ratón y rata respectivamente. Todos los datos siguientes conservan el orden anterior a menos que se indique lo contrario. A las 72 horas fue de 24.3, 13.1 y 0.1; a las 120 fue de 57.8, 24.1 y 0.2 y a las 168 horas fue de 150.6, 1178.4 y 0.2. Para cien células infectadas el número de parásitos fue de 180.0,106.7 y 100.0 (24h); 171.8, 140.8 y 100 (72h); 238.7, 155.1 y 100.0 (120h) de 402.7, 1376.9 y 100.0 a las 168 horas (Fig. 1).
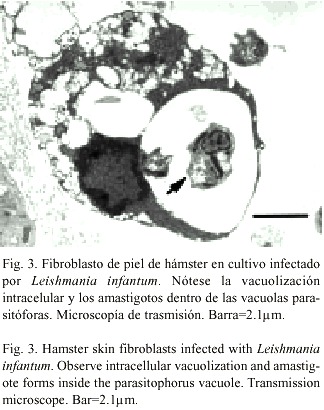
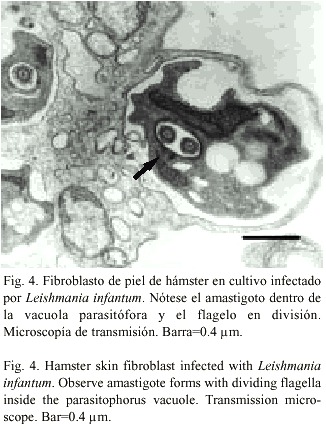
El análisis ultraestructural de fibroblastos infectados reveló una mayor vacuolización en comparación con las células sin infectar. Por otra parte, se encontraron numerosas y amplias vacuolas parasitóforas en el citoplasma y dentro de ellas, amastigotos únicos o en grupos. En ellos fue notorio el núcleo con cromatina densa y un nucleolo, el cinetoplasto alargado, los microtúbulos subpeliculares dispuestos exactamente por debajo de la membrana plasmática y la porción interna del flagelo en conformación 9+2, típico de los organismos eucariotas (Fig. 3). La reproducción de los amastigotos fue evidente por la división flagelar observada dentro de las vacuolas parasitóforas (Fig. 4), descartándose que su presencia tuviera como origen una simple transformación de promastigoto a amastigoto luego de la entrada al fibroblasto.
Discusión
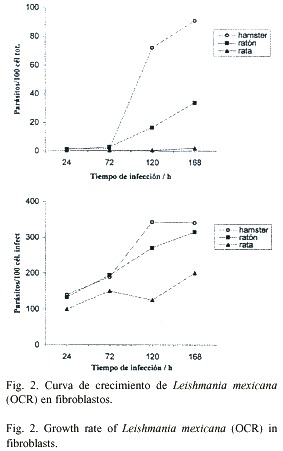
De los resultados obtenidos llama la atención que L. infantum presenta el mayor número de parásitos por cien células totales tanto en hámster como en ratón, en comparación con L. mexicana (OCR). Estos resultados contrastan con lo observado por Chang (1978) en fibroblastos de piel humana, ya que las dos especies derivadas de casos viscerales no penetraron en las células. El autor aduce diferencias en mecanismos de internalización que no se observó con las células de ratón y hamster. Sin embargo, existe una leve concordancia entre ambos experimentos, pues la cepa de origen cutáneo fue la que presentó las mayores tasas de crecimiento. A raíz de esto se puede afirmar que ambas especies presentan distinto grado, no sólo de afinidad por las células de los roedores, sino también de resistencia en el espacio intracelular. El uso de aislamientos recientes hechos a partir de lesiones en animales, permite relacionar esas características con la infectividad natural de cada uno y no a un potencial de virulencia atenuado debido a la permanencia prolongada en medios de cultivo.
En contraste con lo anterior, en los fibroblastos de rata se observaron escasas formas, incluso en los intervalos más tardíos de todos los experimentos. Los valores menores en los radios de crecimiento de L. infantum podrían indicar que se inhibe la reproducción y aunque en L. mexicana (OCR) se obtuvieron datos levemente mayores, si se comparan éstos con los de hámster y ratón, se observa una clara resistencia de los fibroblastos de rata frente al contacto con las dos especies del parásito, por lo que se concluye que en estas células es difícil la infección. Esto podría deberse a diferencias en la expresión de enzimas tales como la Mg2 + ATPasa y Ca2 + ATPasa encontradas en los procesos de adhesión e internalización de L. amazonensis en cultivos primarios de fibroblastos (Corte-Real et al. 1995). Debe recordarse que en estudios anteriores se ha demostrado la resistencia natural de este roedor frente a la infección con otros protozoarios, tales como Toxoplasma gondii (Guerrero et al. 1997, Chinchilla et al. 1981, Troyo y Chinchilla 2003) pero es la primera vez que se le relaciona con Leishmania sp.
Anteriormente se ha hecho referencia a que las especies del género, Leishmania infectan y se transforman dentro de células somáticas, entre ellas los fibroblastos de piel (Schwartzman y Pearson 1985, Hervás-Rodríguez et al. 1996), pero se duda que la reproducción intracelular sea posible (Chang 1978), por lo menos en cuanto a las infecciones en fibroblastos humanos se refiere. En concordancia con la primera aseveración, los hallazgos presentados en este estudio confirman la capacidad de la célula de albergar formas típicas de amastigotos dentro de verdaderas vacuolas parasitóforas citoplasmáticas. En contraste con lo anterior, se demuestra la multiplicación del parásito como un hecho inequívoco, evidenciado por la presencia de estructuras dobles dentro de la bolsa flagelar. Ya sea en el estadío intracelular como extracelular, es el flagelo el primero en dividirse durante la reproducción, de tal manera que puede afirmarse que las formas únicas y múltiples observadas dentro de las vacuolas, no son sólo el producto de una simple transformación de promastigoto a amastigoto sino también de un verdadero desarrollo intracelular. Esta capacidad de multiplicación de Leishmania sp. en células de piel, de por sí no fagocíticas, ha permitido sugerir a Bogdan et al. (2000) que éste podría ser un mecanismo de seguridad para el parásito que le permitiría mantenerse en las infecciones latentes, ya que así obviarían la acción fagocítica de los macrófagos presente en la mayoría de los animales crónicamente infectados (Mauel 1990).
Agradecimientos
Este trabajo fue realizado gracias al apoyo económico de la Vicerrectoría de Investigación de la Universidad de Costa Rica a través del proyecto N° 803-A0-032. Se agradece al Laboratorio de Ensayos Biológicos (LEBi) por el suministro y cuidado de los animales de laboratorio utilizados y al Centro de Investigación en Estructuras Microscópicas de la Universidad de Costa Rica, por el trabajo de gran calidad que brindó.
Resumen
En este estudio se presenta un modelo in vitro de cultivo de fibroblastos de piel de hámster, ratón y rata hecho con el propósito de determinar diferencias en cuanto a la susceptibilidad a la infección por dos especies del género Leishmania (Kinetoplastida: Trypanosomatidae). Se realizó además un estudio ultraestructural por microscopía electrónica de transmisión con el fin de establecer si las formas intracelulares observadas correspondían a multiplicación interna o a fagocitosis múltiple. Se estudió la multiplicación de los parásitos en los fibroblastos de las tres especies de roedores infectados tanto por Leishmania infantum como por L. mexicana (cepa OCR) y las diferencias entre las tres fueron estadísticamente significativas (p< 0.05). Se observó la reproducción del parásito en las células de hámster y ratón no así en las de rata, razón por la cual a este último animal se le consideró refractario a la infección. Con base en lo anterior se sugiere que la afinidad de un protozoario por las células de un individuo así como la resistencia al ambiente intracelular pueden depender de la constitución genética de este. El análisis ultraestructural demostró la reproducción de los amastigotos dentro de vacuolas parasitóforas por lo que se descarta que la presencia de estos se deba a su transformación luego de la entrada al fibroblasto. Se sugiere entonces que dichas células podrían servir para la supervivencia del parásito y la permanencia de este parásito en los animales infectados.
Referencias
Alvar, J., C. Cañavate, B. Gutierrez–Solar, M. Jiménez, F. Laguna, R. López-Velez, R. Molina & J. Moreno. 1997. Leishmania and Human Immunodeficiency Virus coinfection: the first ten years. Clin. Microbiol. Rev. 10: 298-319. [ Links ]
Bastardo, T., L. Arcay & F. Tejero. 1983. Interaction of avirulent Leishmania spp with rat peritoneal macrophages. Mem. Inst. Oswaldo Cruz. 78: 21-26. [ Links ]
Bogdan, C., N. Donhauser, R. Doring, M. Rollinghoff, A. Diefenbach & M.G. Rittig. 2000. Fibroblasts as host cells in latent leishmaniosis. J. Exp. Med. 191: 2121- 2130. [ Links ]
Carrillo, J., M.Chinchilla, B. Valverde, O. Porras & L. Mora. 1999. Visceral Leishmaniasis in Costa Rica: First Case Report. Clin. Infect. Dis. 29: 678-679. [ Links ]
Chang, K.P. 1978. Leishmania infection of human skin fibroblasts in vitro: absence of phagolysosomal fusion after induced phagocytosis of promastigotes, and their intracellular transformation. Am. J. Trop. Med. Hyg. 27: 1084-1096. [ Links ]
Chinchilla, M., M. Alfaro & O.M. Guerrero. 1981. Adaptación natural de la rata blanca a Toxoplasma gondii. Rev. Biol. Trop. 29: 273-282. [ Links ]
Chinchilla, M. & J. Frenkel. 1984. Resistencia a la infección por Toxoplasma in vitro inducida por mediadores linfocitarios en células no fagocíticas de ratón y hámster. Inmunología. 3: 144-150. [ Links ]
Chinchilla, M., L. Reyes & O. Guerrero. 1995. Resistance to intracellular parasites correlates with species differences in ability of macrophages to inhibit parasite replication. Immunol. Infect. Dis. 5: 83-87. [ Links ]
Chinchilla, M., O.M. Guerrero, L. Reyes & E. Abrahams. 1996. Susceptibilidad de la rata Sigmodon hispidus (Rodentia: Cricetidae) al Toxoplasma gondii (Eucoccidia: Sarcocystidae). Rev. Biol. Trop. 44: 265-268. [ Links ]
Corte-Real, S., C.B. Santos & M.N. Meirelles. 1995. Differential expression of the plasma membrane Mg2 + ATPase and Ca2+ ATPase activity during adhesion and interiorization of Leishmania amazonensis in fibroblasts in vitro. J. Submicrosc. Cytol. Pathol. 27: 359-366. [ Links ]
Grimaldi, G. & R. Tesh. 1993. Leishmaniasis of the new world: current concepts and implications for future research. Clin. Microbiol. Rev. 6: 230-250. [ Links ]
Guerbouj, S., I.Gizani, K. Victoir D. Le Ray & J.C. Dujardin. 2000. Parasite candidate vaccines: a warning from polimorphic Leishmania populations. Parasitol. Today. 16: 265. [ Links ]
Guerrero, O., M. Chinchilla & E. Abrahams. 1997. Increasing of Toxoplasma gondii (Coccidia, Sarcocystidae) infections by Trypanosoma lewisi (Kinetoplastida, Trypanosomatidae) in white rats. Rev. Biol. Trop. 45: 887-882. [ Links ]
Hernández, F. & R. Guillén. 2000. Microwave processing for scanning electron microscopy. Eur. J. Morphol. 38: 109-111. [ Links ]
Hervás-Rodríguez, J., E. Mozos, A. Méndez, J. Pérez & J.C. Gómez-Villamandos. 1996. Leishmania infection of canine skin fibroblasts in vivo. Vet. Pathol. 33: 469-473. [ Links ]
Howood, D., G. Milne & J. Penston. 1990. A comparison of microwaves and heat alone in the preparation of tissue for electron microscopy. Histochem. J. 22: 358-364. [ Links ]
Mauel, J. 1990. Macrophage-parasite interactions in Leishmania infections. J. Leukoc. Biol. 47: 187-193. [ Links ]
Medrano, F., C. Cañavate, M. Leal, C. Rey, E. Lissen & J. Alvar. 1998. The role of serology in the diagnosis and prognosis of VL in patients infected with HIV type 1. Am. J. Trop. Med. Hyg. 59: 155-162. [ Links ]
Méndez, S., M. Nell & J. Allunda. 1996. Leishmania infantum infection of macrophages in vitro with promastigotes. Internat. J. Parasitol. 26: 619- 622. [ Links ]
Molina, S. & M. Chinchilla. 1996. Multiplicación in vitro de Leishmania mexicana en macrófagos de hámster y ratones infectados y no infectados. Parasitol. Al Día. 20: 79-85. [ Links ]
Pearson, R. & A. Queiroz-Souza. 1996. Clinical spectrum of leishmaniasis. Clin. Infect. Dis. 22: 1-13. [ Links ]
Schwartzman, J. & R. Pearson. 1985. The interaction of Leishmania donovani promastigotes and human fibroblasts in vitro. Am. J. Trop. Med. Hyg. 34: 850-855. [ Links ]
Segal, G., W. Lee, P. Arora, M. McKee, G. Downey & C.A. McBulloch. 2001. Involvement of actin filaments and integrins in collagen phagocytosis by human fibroblasts. J. Cell.Sci. 114: 119-129. [ Links ]
Troyo, A. & M. Chinchilla. 2003. In vitro multiplication of Toxoplasma gondii and Trypanosoma cruzi in mouse, rat, and hamster astrocytes. Rev. Biol. Trop. 51: 639-646. [ Links ]
Wang, R., A. Ghahary, Y. Shen, P.G. Scott & E.E. Tredget. 1996. Human dermal fibroblasts produce NO and express both cNOS and iNOS isoforms. J. Invest. Dermatol. 106: 419-427. [ Links ]
Wolday, D., N. Berhe, H. Akuffo et al. 1999. Leishmania-– HIV intercation: immunopathogenic mechanisms. Parasitol. Today. 15: 182-187. [ Links ]