Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista de Biología Tropical
On-line version ISSN 0034-7744Print version ISSN 0034-7744
Rev. biol. trop vol.49 n.1 San José Mar. 2001
Blanca Pérez-García1, Aniceto Mendoza1, Irma Reyes Jaramillo1 y Ramón Riba 1
Abstract
The development of the sexual phase of six Mexican species of Dryopteris is described and compared. Spores of all studied species are monolete, ellipsoid and have a rugose surface; the perine is folded, brown to dark brown, with a tubercled outline. Germination pattern is of the Vittaria-type and the development pattern of the prothallia is of the Aspidium-type. Gametangia are of the common type for the leptosporangiate advanced ferns. First leaves of the sporophytes appear 258-265 after sowing and apparently in Dryopteris pseudo-filix-mas the sporophyte have an apogamic origin (80 days). To make a comparative analysis of gametophytic characteristics in the twelve Mexican species and conclude of germination is of the Vittaria-type and development pattern prothallial is of the Aspidium-type, and unicelular trichomes on margin and superficial gametophytic to yield irregular aspect are characteristics to yield unit and characteristic to genera to conform Dryopteridaceae family (sensu Moran 1995) with the exception of Didymochlaena genus.
Key words: Apogamy, Dryopteris, Dryopteridaceae, gametophytes, Mexico, morphogenesis, prothallus, pteridophyta.
El género Dryopteris Adans., ha sido objeto de varias circunscripciones, por lo que es difícil precisar el número exacto de especies que lo conforman, de alrededor de 100 especies, las que crecen principalmente en regiones templadas y tropicales, preferentemente de los 300-3050 msnm. Su mayor diversidad se concentra en Asia Oriental y en el Nuevo Mundo se encuentran 25 especies, 12 de las cuales se distribuyen en México.
Las plantas de este grupo se caracterizan por ser terrestres, epipétricas o raramente epífitas, con los tallos o rizomas erectos y con escamas, las hojas monomorfas, erectas y algo arqueadas, el pecíolo generalmente escamoso de color pajizo-verdoso a pardo-rojizo, la lámina 1-pinnado-pinnatífida a 3-pinnada y tienen un número cromosómico n = 41 (Moran 1995, Riba y Pérez-García 1999).
La morfología de los gametofitos de la familia Dryopteridaceae es ampliamente conocida (Kny 1895; Momose 1937, 1938, 1939; Duncan 1943; Nakazawa 1960; Nakazawa y Ootaki 1962). Por lo que respecta al estudio de la fase sexual del género Dryopteris, se han hecho varios trabajos principalmente con especies del Viejo Mundo y de algunos géneros relacionados (Arachniodes, Cyrtomium, Diacalpe, Didymochlaena, Lithostegia, Peranema y Polystichum) con este grupo de plantas (Chandra y Nayar 1970, Cousens 1975, Kaur 1977, Mendoza et al. 1999a, Mendoza et al. 1999b, Pérez-García et al. 1999, Stokey y Atkinson 1954).
En este trabajo se presenta la descripción y la comparación de la morfogénesis de seis especies del género Dryopteris, recolectadas en México: D. arguta (Kaulf.) Watt., D. futura A.R. Sm., D. nubigena Maxon & C.V. Morton, D. patula (Sw.) Underw., D. pseudo-filix-mas (Fée) Rothm. y D. rosea (Fourn.) Mickel & Beitel, así como un análisis comparativo con otras especies ya estudiadas anteriormente (Pérez-García et al. 1999).
Materiales y métodos
El material estudiado fue recolectado en distintas localidades de la República Mexicana (Cuadro 1). Los ejemplares de respaldo se encuentran depositados en el Herbario Metropolitano UAMIZ.
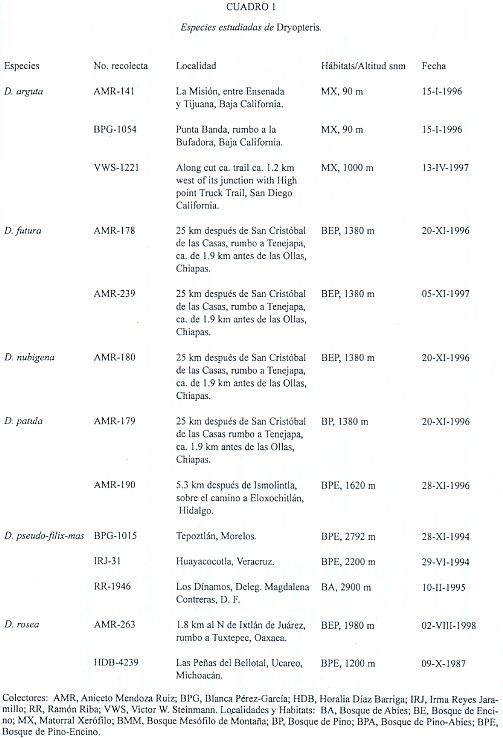
Las esporas se obtuvieron de hojas fértiles de diferentes individuos, las cuales se colocaron en sobres de papel para liberarlas a temperatura ambiente. El material fue tamizado en una malla metálica con poros de 0.074 mm de diámetro. Las esporas de cada especie fueron sembradas sin previa esterilización, en 25 cajas de Petri de 5 cm de diámetro (3 réplicas), que contenían medio de cultivo de Thompson (Klekowski 1969, Pérez-García 1989) en condiciones asépticas. Fueron esparcidas con un pincel de pocas cerdas sobre la superficie del medio. La densidad de esporas sembradas fue de 150-200 por cm2.
Los cultivos se mantuvieron en condiciones de laboratorio dentro de bolsas de polietileno transparente, para evitar contaminación y desecación, con un fotoperíodo de 12 hr luz-oscuridad con luz artificial (Solar 75 Watts, luz de día) y a una temperatura de 23-28 °C. El 10% de las cajas se mantuvieron en obscuridad para determinar fotoblastismo. También se sembraron esporas de las seis especies en suelo en pequeñas macetas (2) de 5 cm de diámetro, fotomicrografías se obtuvieron de gametofitos y de esporofitos vivos.
Resultados
Esporas: homospóricas y aclorofílicas (Kramer y Green 1990, Tryon y Lugardon 1991), son monoletes, bilaterales, elipsoidales de color pardo a pardo oscuro, superficie rugosa de contorno tuberculado y perina con prominentes pliegues largos o cortos, cristada a equinada; las esporas más pequeñas fueron las de D. rosea que miden (34) 40 (48) m por (25) 29 (31)
m y las más grandes las de D. pseudo-filix-mas que miden (53) 58 (64)
m por (35) 40 (44)
m (Figs. 1-3). La variación en el tamaño de las esporas de las seis especies estudiadas se presentan en el cuadro 2.
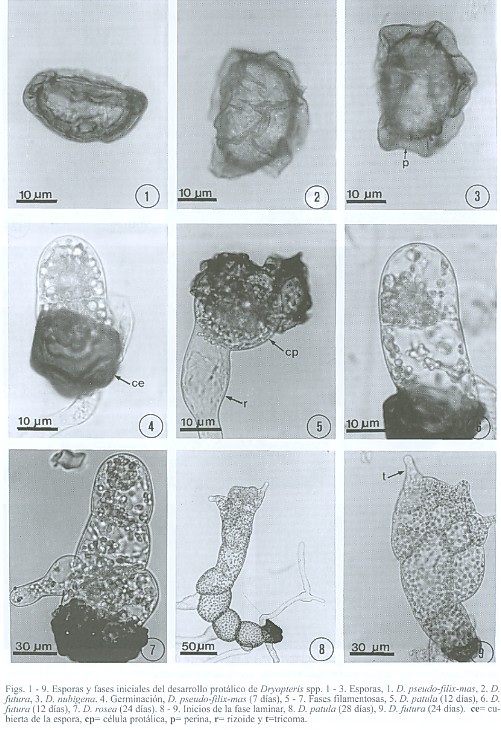
Germinación: el patrón de germinación está basado en los planos de división de la célula en relación con la polaridad de la misma y la dirección de crecimiento de la célula rizoidal primaria y la protálica. Con base en lo anterior el patrón de germinación para las seis especies estudiadas es del tipo Vittaria ya que la primera división celular en la germinación de la espora se produce por una pared paralela al plano ecuatorial de la misma y el alargamiento de la célula rizoidal primaria y el filamento germinativo joven es paralelo al eje polar de la espora (Nayar y Kaur 1971). En general el proceso de germinación se inicia entre 7 y los 12 días después de sembradas las esporas. Se desarrolla primero la célula rizoidal, que es hialina y unicelular y posteriormente emerge la célula protálica, la cual presenta abundantes cloroplastos (Figs.4, 5).
En los cultivos que se mantuvieron en la obscuridad no se observó germinación después de 100 días, por lo que se considera que las esporas de las seis especies en estudio son fotoblásticas positivas, se obtuvo un porcentaje de germinación del 95 %.
Fase filamentosa: la germinación de la espora origina un filamento germinal delgado, uniseriado y corto, de 2 a 5 células protálicas, en forma de barril y con numerosos cloroplastos y glóbulos de grasa, ésta fase se presenta entre los 10 y los 20 primeros días en promedio, en las seis especies (Figs. 6, 7, 8).
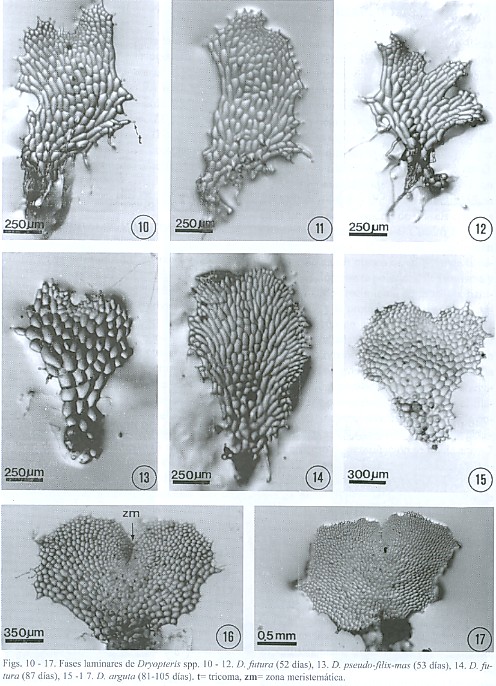
Fase laminar: la secuencia de divisiones celulares y el desarrollo del protalo joven están condicionados por la formación temprana de pelos en el mismo, por lo que el desarrollo protálico que presentan las seis especies en estudio es tipo Aspidium (Nayar y Kaur 1969, 1971). La germinación de la espora forma un filamento germinal de unas cuantas células, cuya célula terminal produce un pelo en su ápice. Una de las células hijas de la penúltima célula se diferencia tempranamente en una célula obcónica y se desarrolla lateralmente en el gametofito y la formación de la lámina se inicia a partir de las células que están por detrás de la célula terminal, las cuales se dividen longitudinalmente. La lámina protálica es asimétrica con un lado mayor que el otro. El protalo crece por la actividad de la célula inicial y después la región meristemática adquiere una muesca poco profunda y se vuelve apical por el crecimiento unilateral del gametofito (Figs. 9 -15). La forma asimétrica del mismo se pierde muy pronto. En los cultivos de las seis especies ésta se forma entre los 20 y los 90 días. En todas las fases se conserva la cubierta de la espora y los rizoides no son profusos (Figs.16 - 17).
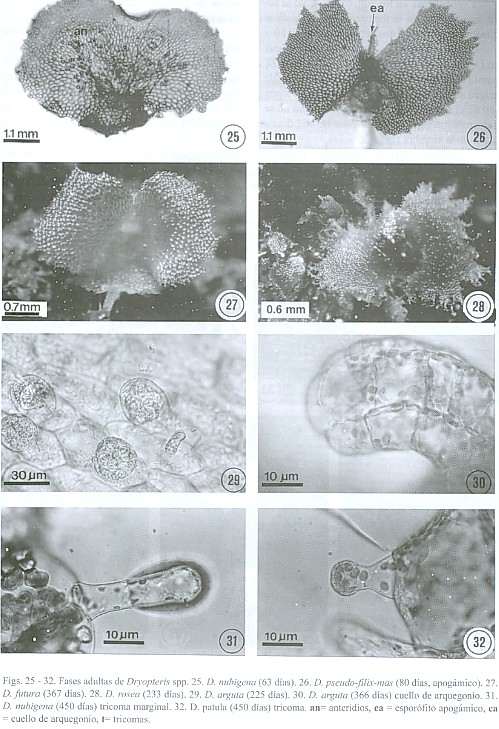
Fase adulta: entre los 50 y los 233 días posteriores a la siembra, los gametofitos adultos son cordiforme-espatulados, cordados, espatulados u ocasionalmente reniformes. Como es característico del género Dryopteris presentan numerosos tricomas marginales y superficiales, dándole al gametofito un aspecto irregular (Figs. 18 - 24).
Dryopteris arguta: los gametofitos son cordiforme-espatulados con un meristemo central pluricelular formando una muesca, las alas son isodiamétricas y amplias y su contorno es irregular debido a los tricomas unicelulares, capitados, que se desarrollan en el margen y en la superficie; presentan un cojinete definido en la región media central, donde se forman los gametangios, los rizoides son hialinos y basales (Figs. 18-21). Se desarrollaron tanto gametofitos masculinos como femeninos (88-173 días).
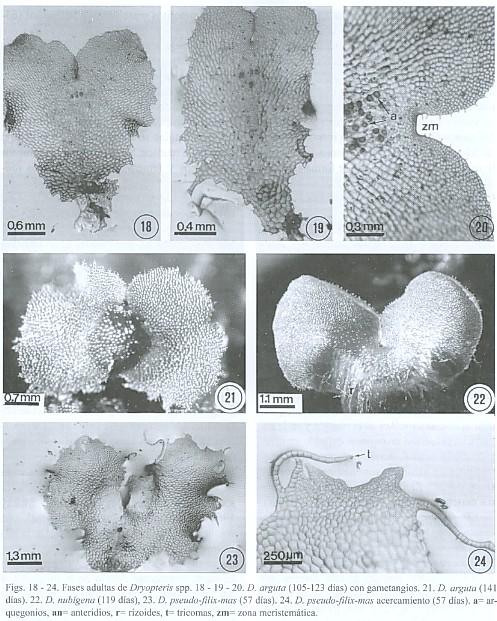
D. futura: los gametofitos son cordiforme-espatulados, con alas simétricas estrechas, con márgenes de aspecto irregular, la muesca meristemática es central, presentan tricomas marginales y superficiales, cojinete no bien definido, los gametangios se forman en la parte ventral cerca de la muesca (Fig. 27). Los gametofitos son masculinos y femeninos (51-68 días).
D. nubigena: los gametofitos son espatulado-cordiformes u ocasionalmente reniformes, con abundantes tricomas unicelulares y capitados en el margen y en la superficie, con un cojinete en la región media central, en donde se desarrollan los gametangios ventralmente cerca de la muesca (Figs. 22, 25, 31), se forman gametofitos masculinos y femeninos (63-186 días).
D. patula: los gametofitos son espatulados y reniformes, con abundantes tricomas unicelulares, capitados marginal y superficialmente (Fig. 32), la muesca es central, las alas dependiendo de la forma del protalo pueden ser estrechas o amplias, el cojinete es inconspicuo, los gametangios se forman en la parte ventral cerca de la muesca. Se observaron gametofitos masculinos y femeninos en los cultivos (50-126 días).
D. pseudo-filix-mas: los gametofitos son cordiformes a reniformes con alas amplias, con la muesca central profunda y separando las alas isodiamétricas, presenta tricomas unicelulares marginales y superficiales dándoles aspecto irregular, el cojinete es inconspicuo (Figs. 23 - 24). Los esporofitos formados fueron de origen apogámico, no se formaron arquegonios y en la misma población se forman gametofitos anteridiados (119-233 días).
D. rosea: los gametofitos son cordiformes, con alas isodiamétricas amplias y una muesca central, con abundantes tricomas marginales y superficiales dándoles el típico aspecto irregular, el cojinete es inconspicuo y sobre el se desarrollan los gametangios (Fig. 28). Observamos en los cultivos tanto gametofitos masculinos como femeninos (233 días).
En lo que se refiere a su expresión sexual se presentan gametofitos dioicos en D. arguta, D. futura, D. patula y D. rosea; en D. pseudo-filix-mas sólamente se desarrollan protalos monoicos y en D. nubigena no se formaron gametangios después de 462 días de la siembra.
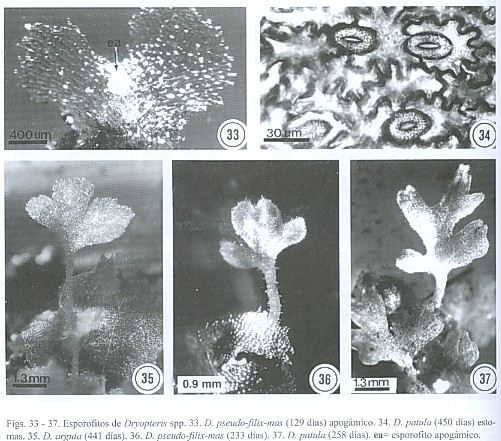
Esporofitos: en los cultivos en suelo se tuvo mayor éxito en la formación de esporofitos que en los de agar. Éstos se formaron a los 80 y los 441 días después de sembradas las esporas en D. arguta (441 días), D. futura (400 días), D. patula (258 días) y D. rosea (265 días) y son de origen sexual, solamente en D. pseudo-filix-mas (80 días) son apogámico y en D. nubigena no se desarrollaron esporofitos después de 462 días a partir de la siembra (Figs. 35 - 37).
La primera hoja del esporofito presenta pecíolo y una lámina entera bi-a trilobulada, con venación dicotómica abierta. Toda la plántula joven presenta tricomas uni o bicelulares secretores y estomas anomocíticos y las células de las paredes laterales son típicamente onduladas (Fig. 34).
Solamente D. pseudo-filix-mas presenta esporofitos de origen apogámico y estos se desarrollaron a los (80-233) días, el embrión apogámico se formó a partir de un grupo de células iniciales y superficiales en el lado ventral del gametofito, sobre el cojinete y cerca de la muesca del mismo, el joven esporofito formó el tallo y la raíz simultáneamente y posteriormente la hoja, lo que confirma lo ya mencionado por Duncan (1943) en el sentido de que la célula inicial apical del tallo es formada en los estadíos tempranos de desarrollo del embrión (Figs. 23, 26, 33, 36).
Dryopteris arguta, D. futura, D. nubigena, D. patula, D. pseudo-filix-mas y D. rosea presentan el mismo tipo de esporas, patrón de germinación y desarrollo protálico, gametangios leptosporangiados y difieren en su expresión sexual y en el origen de sus esporofitos como ya lo citaron para otras especies mexicanas Pérez-García et al. (1999).
El desarrollo gametofítico de las 12 especies de este género que existen en México es bastante homogéneo y presenta cierto grado de variación en cuanto a la forma adulta del gametofito, expresión sexual y origen del esporofito.
Es interesante hacer una comparación de las diferencias y semejanzas presentes en las doce especies de Dryopteris estudiadas.
Las similitudes que podemos encontrar entre las doce especies (cuadro 3) son: Esporas monoletes de color pardo a pardo obscuro, siendo las más pequeñas las de D. rossii (28) 40 (44) m x (24) 29 (32)
m y las más grandes las de D. karwinskiana (52) 59 (68)
m x (40) 42 (48)
m, el resto de las especies presentan un tamaño intermedio, esta variación en tamaño de esporas ya habia sido citado por Kanamori (1969).
En cuanto al tipo de germinación Vittaria y al desarrollo protálico Aspidium, ambos estan presentes en las 12 especies estudiadas.
La fase filamentosa presenta una ligera variación durante su desarrollo, presentándose los filamentos más cortos en D. pseudo-filix-mas con 2 células y los más largos en D. wallichiana con 2-9 células. Todas las especies presentan gametangios del tipo de los helechos leptosporangiado.
Las diferencias que podemos percibir en el cuadro 3 son: En la forma de la fase adulta, la mas frecuente es la cordiforme manifestandose en D. arguta, D. cinnamomea, D. munchii, D. patula, D. pseudo-filix-mas, D. rosea y D. rossii; mientras que D. futura, D. karwinskiana y D. maxonii la presentan cordiforme-espatulada; y D. karwinskiana y D. wallichiana presentan forma cordiforme a acintada; solamente D. nubigena lo presenta espatulado-cordiforme, esta variación en forma se debe probablemente a la gran plasticidad de los gametofitos.
En la expresión sexual sí observamos una variación significativa: Se registraron gametofitos dioicos en D. arguta, D. futura, D. maxonii, D. nubigena, D. patula y D. rosea; gametofitos monoicos y dioicos en las mismas poblaciones en D. cinnamomea, D. karwinskiana y D. rossii y gametofitos exclusivamente con anteridios y asexuados en las mismas poblaciones en D. munchii, D. pseudo-filix-mas y D. wallichiana.
El origen del esporofito en la mayoría de las especies estudiadas es sexual, con excepción D. munchii, D. pseudo-filix-mas y D. wallichiana en que fueron de origen apogámico (Loyal 1959), el desarrollo de los esporofitos fue más rápido en los cultivos en suelo que en los de agar.
La apogamia es frecuente en el género Dryopteris y varias de sus especies tiene apogamia obligada, este fenómeno ha sido estudiado en el complejo Dryopteris pseudo-mas Woll, D. hirtipes (Blume) O. Kuntze, D. mollis Underw., por Duncan (1943), en D. chinensis (Baker) Koidzumi por Kanamori (1967), en D. dilatata (Hofm.) A. Gray y D. filix-mas (L.) Schott por Manton y Walker (1954).
En cuanto a la expresión sexual de los gametofitos en los representantes del género se cuenta con los estudios de Cousens y Horner (1970) para Dryopteris ludoviciana (Kunze) Small; y el de Korpelainen (1994) para D. campyloptera (Kunze) Clarkson, D. excelsa (Desv.) C. Chr., D. clintoniana Wherry, D. filix-mas (L.) Schott, D. goldiana (Hook.) Gray, D. intermedia (O.F. Müll. ex Willd.), D. marginalis (L.) Gray y D. spinulosa (Müll.) O. Kuntze.
Los diversos patrones de expresión sexual que se presentan en las especies de Dryopteris pueden interpretarse como adaptaciones para facilitar el entrecruzamiento intra e intergametofítico en los diferentes ambientes en que las especies se desarrollan.
Las ventajas evolutivas que representan estos patrones de expresión sexual permiten la acumulación de heterocigosidad y hacen posible la hibridización entre las diversas especies la cual puede incrementarse como resultado de la unisexualidad en gametofitos, de este modo la expresión variable del sexo en el género permite procesos de evolución divergente y reticulada (Cousens 1975).
Por último, si seguimos el criterio de Moran (1995) establecido en Flora Mesoamericana para la familia Dryopteridaceae, la misma está conformada por 10 géneros, de los cuales en México se presentan Arachniodes, Dryopteris, Olfersia, Phanerophlebia, Polystichum, Polybotrya y Stigmatopteris. Todos ellos presentan gametofitos con pelos de tamaño distinto, lo que les da un aspecto eroso- fimbriado, con excepción de Didymochlaena cuyos gametofitos son glabros. Nuestros resultados refuerzan las ideas planteadas por Atkinson (1973), Atkinson y Stokey (1964) y Stokey (1951) quién afirman que podemos encontrar información útil que nos sugiera posibles relaciones, algunas veces a nivel de familia pero probablemente de manera más frecuente, entre géneros y especies, como observamos en la familia Dryopteridaceae y sus correspondientes géneros excepto Didymochlaena (Mendoza et al. 1999a, 1999b, Pérez-García et al. 1999). En el caso particular de esta familia, el patrón de germinación tipo Vittaria y el desarrollo tipo Aspidium son específicos útiles para caracterizarla.
Agradecimientos
Los autores agradecen a Ana Rosa López-Ferrari y Adolfo Espejo Serna la revisión del manuscrito y a los árbitros anónimos sus valiosas sugerencias.
Resumen
Se describe y se compara la morfogénesis de la fase sexual de seis especies mexicanas de Dryopteris. Las esporas de todas las especies estudiadas son monoletes y elipsoidales, la perina es plegada, de color pardo claro a pardo obscuro, su superficie es rugosa y de contornos tuberculados. El patrón de germinación es tipo Vittaria y el desarrollo protálico es tipo Aspidium. Los gametangios son del tipo característicos de los helechos leptosporangiados. Se desarrollaron esporofitos en cinco de las seis especies y solamente en D. pseudo-filix-mas es de origen apogámico (80 días). Se hace un análisis comparativo de las características gametofíticas presentes en las 12 especies mexicanas del género y se concluye que el tipo de germinación Vittaria y el patrón de desarrollo protálico tipo Aspidium y gametofitos con tricomas unicelulares, capitados marginales y superficiales, de aspecto irregular, son características que le dan unidad y caracterizan a los géneros que conforman la familia Dryopteridaceae (Moran, 1995) a excepción del género Didymochlaena.
Referencias
Atkinson, L.R. 1973. The gametophyte and family relationships. p. 73-90. In: A.C. Jermy, J.A. Crabbe & B.A. Thomas (eds.). The phylogeny and clasification of the ferns. Academic. Nueva York.
Atkinson, L.R. & A.G. Stokey. 1964. Comparative morphology of the gametophyte of homosporous ferns. Phytomorphology 14: 51-70. [ Links ]
Cousens, M.I. 1975. Gametophyte sex expression in some species of Dryopteris. Amer. Fern J. 65: 39-42. [ Links ]
Cousens, M.I. & H.T. Horner. Jr. 1970. Gametophyte ontogeny and sex expression in Dryopteris ludoviciana. Amer. Fern J. 60: 13-17. [ Links ]
Chandra, P. & B. K. Nayar. 1970. Morphology of some polystichoid ferns. I. The gametophytes of Arachniodes, Cyrtomium and Polystichum. J. Linn. Soc. Bot. 63: 265-276. [ Links ]
Duncan, R.E. 1943. Origin and development of embryos in certain apogamous forms of Dryopteris. Bot. Gaz. (Crawfordsville) 105: 202-211. [ Links ]
Kanamori, K. 1967. Origin and early development of apogamous embryos in the protallia of Dryopteris chinensis. J. Jap. Bot. 42: 111-118. [ Links ]
Kanamori, K. 1969. Studies on the sterility and size variation of spores in some species of japanese Dryopteris. Journ. Jap. Bot. 44: 207-217. [ Links ]
Kaur, S. 1977. Morphology of the prothallus and juvenile sporophytes of some species of Dryopteris. Proc. Indian Acad. Sci. 85b: 48-50. [ Links ]
Klekowski, E.J. Jr. 1969. Reproductive biology of the Pteridophyta. III. A study of the Blechnaceae. Bot. J. Linn. Soc. 62: 361-377. [ Links ]
Kny, L. 1895. Entwickelung von Aspidium filix-mas Sw. Bot. Wandt. 9: 411-438. [ Links ]
Korpelainen, H. 1994. Growth, sex determination and reproduction of Dryopteris filix-mas (L.) Schott gametophytes under varying nutritional conditions. Bot. Jour. Linnean Soc. 114: 357-366. [ Links ]
Kramer, K. U. & P. S. Green. 1990. I. Pteridophytes and Gymnosperms pp.110-112. In: K. Kubitzki (ed). The Families and Genera of Vascular Plants. Springer-Verlag, Berlín. [ Links ]
Loyal, D.S. 1959. Some observations on the cytology and apogamy of Himalayan Dryopteris paleacea (Don.) Hand-Mazz. J. Indian Bot. Soc. 39: 608-613. [ Links ]
Manton, I. & S. Walker. 1954. Induced apogamy in Dryopteris dilatata (Hoffm.) A. Gray and D. filix-mas (L.) Schott emend. and its significance for the interpretation of the two species. Ann. Bot. (London) 18: 377-383. [ Links ]
Mendoza, A., B. Pérez-García & R. Riba. 1999a. Morfología y anatomía del gametofito de Didymochlaena truncatula (Dryopteridaceae). Rev. Biol. Trop. 47: 87-93. [ Links ]
Mendoza, A., B. Pérez-García & R. Riba. 1999b. Morfogénesis de la fase sexual del helecho Arachniodes denticulata (Dryopteridaceae). Rev. Biol. Trop. 47(4): (en prensa).. [ Links ]
Momose, S. 1937. Studies on the gametophyte of ferns. On the prothallial development and prothallium of Dryopteris varia O. Kuntze. J. Jap. Bot. 13: 113-120. [ Links ]
Momose, S. 1938. Studies on the gametophytes of ferns: On the prothallium of eudryopteroid ferns. J. Jap. Bot. 14: 445-453. [ Links ]
Momose, S. 1939. Studies on the gametophytes of ferns: Further observations on the prothallium of eudryopteroid ferns. J. Jap. Bot. 15: 280-292. [ Links ]
Moran, R.C. 1995. Dryopteridaceae, p. 210-226. In: R.C. Moran. y R. Riba (eds.). Flora Mesoamericana. Instituto de Biología, Jardín Botánico de Missouri y Museo de Historia Natural de Londres.
Nayar, B.K. & S. Kaur. 1969. Types of prothallial development in homosporous ferns. Phytomorphology 19: 179-188. [ Links ]
Nayar, B.K. & S. Kaur. 1971. Gametophytes of homosporous ferns. Bot. Rev. 37: 295?396. [ Links ]
Nakazawa, S. 1960. Cytodifferentiation patterns of Dryopteris protonema modified by some chemical agents. Cytologia 25: 352-361. [ Links ]
Nakazawa, S. & T. Ootaki. 1962. A prepattern to the papilla diferentiation in Dryopteris gametophyte. Phtyton (Buenos Aires)18: 113-120. [ Links ]
Pérez-García, B. 1989. Morfogénesis de gametofitos de Cyatheaceae (Pterophyta: Filicales). Tesis Doctoral. Fac. Ciencias, Universidad Nacional Autónoma de México, México, D. F. [ Links ]
Pérez-García, B., A. Mendoza, I. Reyes Jaramillo & R. Riba. 1999. Morfogénesis de la fase sexual de seis especies mexicanas del género Dryopteris (Dryopteridaceae). Rev. Biol. Trop. 47: 63-75. [ Links ]
Riba, R. & B. Pérez-García. 1999. Dryopteridaceae. In Flora de México 6(4): 1-48. Consejo Nacional de la Flora de México, A. C. México, D. F. [ Links ]
Stokey, A. G. 1951. The contribution by the gametophyte to classification of the homosporous ferns. Phytomorphology 1: 39-58. [ Links ]
Stokey, A.G. & L.R. Atkinson. 1954. The gametophyte of Didymochlaena sinuata Desv. Phytomorphology 4: 310-315. [ Links ]
Tryon, A.F. & B. Lugardon. 1991. Spores of the Pteridophyta: surface, wall structure, and diversity based on electron microscope studies: i-x. Springer-Verlag, Nueva York. pp. 440 -441. [ Links ]
1 Depto. de Biología, Área de Botánica Estructural y Sistemática, Universidad Autónoma Metropolitana-Iztapalapa, Apartado Postal 55-535, 09340, México, D. F., Fax: (52) 5 804 4688, e-mail: bpg@xanum.uam.mx














