Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Acta Médica Costarricense
On-line version ISSN 0001-6002Print version ISSN 0001-6012
Acta méd. costarric vol.49 n.1 San José Jan. 2007
Glucemia postcarga en diabetes gestacional
Leonardo Orozco- Saborío, Fiorella Moya- Moya
Resumen
Objetivo: Determinar el valor umbral de glucosa postcarga más sensible y con mayor valor predictivo positivo para el diagnóstico de diabetes gestacional en pacientes con embarazos de 24 -28 semanas.
Métodos: Estudio observacional. Se identificó a partir de los archivos del Servicio de Laboratorio del hospital, a toda mujer embarazada a la que se le realizó la curva de tolerancia oral a la glucosa (100g glucosa), la cual se indicó a partir de valores de glucosa postcarga (50g glucosa) de 130 mg/dl. La cuantificación de los niveles de glucosa se efectúo con el sistema SYNCHRON CX (glucosa oxidasa), y se utilizaron los criterios de The National Diabetes Data Group para los valores de las pruebas. Se hizo un análisis estadístico univariado y multivariado con modelo de regresión logístico y construcción de curva ROC (Receiver Operating Characteristic: curvas en las que se presenta la sensibilidad en función de los falsos positivos para distintos puntos de corte) para la determinación de sensibilidad y especificidad. Se utilizó el paquete estadístico STATA, versión 7, 2000.
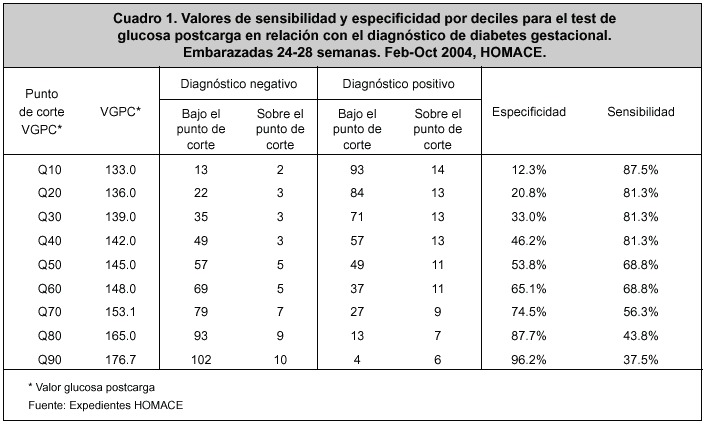
Resultados: Se revisaron 137 casos, de los cuales 123 cumplieron con los criterios de inclusión. La situación más favorable para la población en estudio se encontró en el percentil 60 (Q 60), para un valor de 148 mg/dl con una sensibilidad del 68.8% y una especificidad del 65.1%. Un valor de glucosa postcarga de 177 mg/dl, tiene una sensibilidad del 37.5 % y una especificidad del 96.2%, y un valor de 133 mg/dl, tiene una sensibilidad del 87.5% y una especificidad del 12.3%.
Conclusiones : Un valor de 140 mg/dl de glicemia postcarga puede ser mantenido como valor umbral del test de tamizaje glucosa postcarga, si el objetivo del tamizaje es reconocer pacientes con una curva de tolerancia a la glucosa positiva. Valores mayores a 177mg/d en la glucosa postcarga comprometen la indicación de la curva de tolerancia a la glucosa para diagnosticar diabetes gestacional, por su alta especificidad.
Descriptores: Diabetes gestacional, tamizaje, valor umbral
Key words: Gestational diabetes, challenge screening test, cut-off value
Recibido: 16 de enero de 2006 Aceptado: 17 de octubre de 2006
La diabetes gestacional (DG) se define como la intolerancia a los carbohidratos en diferentes grados de severidad, que inicia o se reconoce por primera vez durante el embarazo.1,2
La DG significa un riesgo para la embarazada y su feto. Mujeres con DG tienen a corto plazo un aumento en la incidencia de preeclampsia, operación cesárea y parto traumático3; a largo plazo, aproximadamente un tercio desarrollará Diabetes Mellitus no insulino dependiente.4
Los hijos de madres con diabetes gestacional presentan de 3 a 4 veces mayor riesgo de macrosomía fetal.5 Consecuencias neonatales tempranas incluyen desórdenes metabólicos como hipoglicemia, hiperbilirrubinemia, hipocalcemia e hipertrofia cardiaca.6
La conducta usual para detectar la DG es someter a la mujer embarazada a la medición de su glicemia plasmática después de una carga de 50 g de glucosa oral, entre las 24 y 28 semanas de gestación.7 Cousins discute que el umbral de la prueba de tamizaje (glucosa postcarga) no debe ser mayor a 140 mg/dl, o una inaceptable pérdida de sensibilidad ocurriría.8
Las recomendaciones actuales para el tamizaje de la diabetes gestacional son controversiales.9 Carpenter, Cowstan et al, y Cowstan, han aconsejado utilizar un valor de 130 mg/dl como umbral para considerar la prueba positiva. Estos autores reportaron que al menos el 10% de pacientes con DG no serán diagnosticadas si se usa 140 mg/ dl como umbral del test.10-13
Taylor et al, usando un valor límite de 130 mg/dl en mujeres con factores de riesgo (edad, índice masa corporal, raza), describen una detección del 82.6%, en comparación con el 78.3%, usando el límite usual de 140 mg/dl.7
Bonomo et al, en un estudio multicéntrico realizado en 1992 por la Sociedad Italiana de Diabetología, llegaron a la conclusión de que para prevenir riesgos perinatales, un valor límite de 136 mg /dl podría ser utilizado con el fin mejorar la sensibilidad del test.14
La meta para un test de tamizaje es detectar la enfermedad en un estado que permita curar o aminorar su morbilidad y mortalidad, por lo que un valor umbral más adecuado, según el caso, sería recomendable.9
Por lo tanto, el objetivo es definir el valor o rango de valores de la prueba de tamizaje (glucosa postcarga), más sensible y con mayor valor predictivo positivo para una curva de tolerancia a la glucosa diagnóstica de DG en la población, y demostrar la asociación de las características clínicas: edad, peso, talla, índice de masa corporal, antecedentes heredofamiliares y grupo étnico con el diagnóstico.
Métodos
Se realizó un estudio retrospectivo, no comparativo, no aleatorio, tomando como población a toda mujer embarazada que tuvo el control prenatal en el Hospital de las Mujeres "Dr. Adolfo Carit Eva" (HOMACE), entre enero y noviembre de 2004.
En la consulta de control prenatal se realizó la prueba de tamizaje de DG con glucosa postcarga de 50 g de glucosa entre las 24 y 28 semanas de gestación.
A aquellas pacientes cuya prueba fue mayor o igual a 130 mg/dl, se les realizó la curva de tolerancia a la glucosa con 100 g de glucosa.
Las embarazadas con DG se identificaron con los criterios de The National Diabetes Data Group.15
La cuantificación de la glucosa se realizó con el método del sistema SYNCHRON CX (glucosa oxidasa), disponible en el Servicio de Laboratorio del Hospital
A partir de los archivos del Servicio de Laboratorio del Hospital, se identificó a toda embarazada a la que se le realizó la curva de tolerancia a la glucosa para diagnóstico de DG en el período establecido.
Una vez seleccionado el grupo de estudio, se revisaron los expedientes clínicos para recolectar las siguientes variables: valor de la glucosa en el test de tamizaje distribuido según la cifra absoluta y las siguientes variables sociodemográficas: edad menor de 25 años, igual o mayor a 25 años. Antecedentes heredofamiliares de Diabetes Mellitus, tomado como negativa la ausencia de historia de diabetes en abuelos, padres, hermanos o hijos de la mujer en estudio.
Índice de masa corporal: se definió peso normal de acuerdo con la Organización Mundial de la Salud, como un índice de masa corporal < 25 kilogramo/metro cuadrado, siendo kilogramo, el peso preconcepcional, reportado por la mujer embarazada el primer día de su control prenatal, y metro, la estatura de la mujer medida en metros.
Grupo étnico: descendencia hispana y que habite en el país. Se excluyeron los casos de pacientes conocidas diabéticas, hipertensas crónicas o con alguna enfermedad crónica asociada, embarazo múltiple y con patología obstétrica vinculada. Se utilizó un análisis estadístico univariado y multivariado con modelo de regresión logístico y construcción de curva ROC (Receiver Operating Characteristic) para el análisis de sensibilidad y especificidad (curvas ROC son curvas en las que se presenta la sensibilidad en función de los falsos positivos para distintos puntos de corte).
Se analizaron los datos con el paquete estadístico STATA, versión 7, 2000.
Resultados
Se revisaron 137 casos, de los cuales 123 cumplieron con los criterios de inclusión para el estudio.
Se excluyeron catorce casos debido a: ausencia del informe del valor de la glucosa postcarga en el expediente (n:2), curva de tolerancia a la glucosa realizada a pacientes no embarazadas (n:6), y pacientes que vomitaron y no completaron la curva de tolerancia a la glucosa (n:6).
El promedio de edad de las pacientes fue de 30 ± 6.85 años; el 50% de las edades centrales se encontró entre 24 y 36 años. El promedio del peso fue de 68.57±17.51 Kg, y de un 27.51±6.48 Kg/m2 para el índice de masa corporal. El 66% de mujeres presentaban problemas de sobrepeso al iniciar el embarazo.
Se obtuvo una proporción de 17 pacientes con el diagnóstico de DG para un 13.82%.
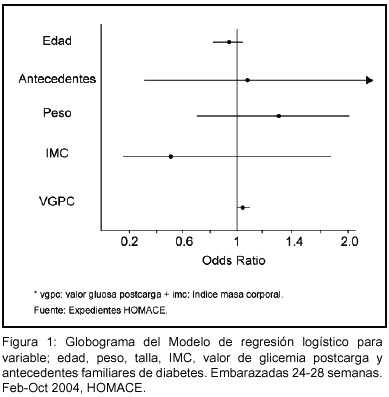
Se comprobó que por cada unidad que aumente el valor de glicemia postcarga existe un 6% más de probabilidad de presentar el diagnóstico de diabetes gestacional OR: 1.06 (IC: 1.0275-1.1030) P 0,001 (Figura 1).
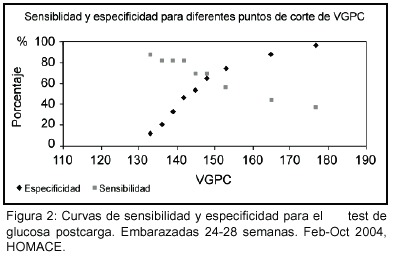
El valor de glicemia postcarga más favorable para el diagnóstico de DG en la población estudiada fue de 148 mg/ dl, con una especificidad del 65.1% y una sensibilidad del 68.8% (Cuadro 1). En este punto, que corresponde al percentil 60 (Q60) se produjo la intersección de ambas curvas (sensibilidad y especificidad) (Figura 2).
Un valor de glucosa postcarga de 177 mg/dl tiene una especificidad del 96%, y un valor de 133 mg/dl tiene una sensibilidad del 87.5% y una especificidad del 12.3 % (Cuadro 1). La variable etnia no se incluyó, pues todas las pacientes fueron del grupo étnico hispano.
Discusión
Se encuentran pruebas concluyentes de una asociación entre los valores de glucosa postcarga mayores de 130 mg/ dl y el desarrollo de DG.
Este resultado podría intuirse lógicamente, ya que el diagnóstico de dicha patología se realiza con base en los niveles de la glucemia. No es así el caso de las demás variables sociodemográficas: antecedentes heredofamiliares, peso, talla, índice de masa corporal y edad.
La situación de la variable edad, con un OR: 0,95 (IC 0.4-1.07), muestra la tendencia de la edad como factor protector para el desarrollo de DG. Se podría explicar esta discrepancia con los criterios emitidos por el Comité de Expertos de Diabetes en 1997(3), debido a que 91 pacientes (74%) se encontraban en el grupo de menores de 25 años, y 32 (26%) en el grupo de 25 años o más, siendo una población mayoritariamente joven.
En términos generales, se requiere que el test tenga una alta sensibilidad para detectar verdaderos positivos, es decir, mujeres que verdaderamente estén desarrollando la enfermedad (diabetes) durante el período del embarazo pero también que al mismo tiempo la prueba pueda detectar con alta probabilidad los verdaderos negativos (especificidad), es decir, mujeres que no desarrollaran la enfermedad durante el período del embarazo.
Dado que el interés es maximizar la probabilidad de verdaderos positivos y verdaderos negativos, se debió establecer diferentes puntos de corte y analizar el comportamiento de las curvas individuales de especificidad y sensibilidad para cumplir con este requisito.
Con el valor obtenido de 148 mg/dl como punto de cruce de sensibilidad y especificidad (68,8% y 65,1%), respectivamente (Gráfico 2), se concluye que un valor de 140mg/dl de glucemia postcarga puede ser mantenido como valor umbral del test de tamizaje glucosa postcarga, si el objetivo del tamizaje es reconocer pacientes con una curva de tolerancia a la glucosa positiva.
Se puede observar la similitud con estudios anteriores de Bonomo, donde se obtuvieron valores de 142 mg/dl y 141 mg/dl de glicemia postcarga.13Sin embargo, se podría proponer un valor de 135mg/dl para aumentar la captación de embarazadas con DG (sensibilidad >80%), a expensas de una pérdida de especificidad. Habría que analizar costo beneficio de esta recomendación en futuros estudios.
Se debería considerar no indicar la curva de tolerancia a la glucosa con valores de glucosa postcarga mayores de 170 mg/dl, ya que se demostró una alta especificidad (>87,4%) para el diagnóstico de DG, evitando así someter a la paciente al estrés fisiológico y psicológico de la prueba.
Las variables sociodemográficas no se relacionan con el diagnóstico de DG en este estudio. Se podría ampliar la población del estudio para observar el comportamiento del intervalo de confianza en investigaciones venideras.
Dentro de las limitaciones, se halló la dificultad para localizar expedientes en el archivo del Hospital, debido a la no concordancia del número de expediente reportado en el Laboratorio con el original (n: 22). Por otra parte, se envió la curva de tolerancia a la glucosa a mujeres no embarazadas (n: 6), en dos casos se envió la curva de tolerancia a la glucosa sin previa glucosa postcarga, y en 6 casos la paciente no la completó, pero todos estos casos fueron excluidos.
Abstract
Objective: To determine the most sensitive and positive predictive cut-off value for the oral glucose challenge screening test for the diagnosis of gestational Diabetes Mellitus in women with pregnacies between the 24-28 weeks.
Methods: Observational study. From the files of the hospitals laboratory service, every pregnant woman who had an oral glucose tolerance (100g of glucose) test; this test was had been indicated because values of more or equal to 130 mg/dl during of oral glucose challenge screening test (50g of glucose). The glucose levels were quantified by the SYNCHRON CX system. The National Diabetes Data Group criteria were used. Logistic regression model was utilized, and ROC (Receiver Operating Characteristic) curve analysis was done to determine the sensitivity and specificity. The STATA statistical program, version 7, 2000 was used.
Results: 123 cases were included in the analysis. The cut-off value of the oral glucose challenge screening test for our population was 148 mg/dl.
A value of the oral glucose challenge screening test of 177 mg/dl has a sensitivity of 37.5% and a specificity of 96.2%. A value of 133 mg/dl has a sensitivity of 87.5% and a specificity of 12.3%.
Conclusion: An oral glucose challenge screening test of 140 mg/dl can be kept as the cut-off value, if the goal of the screening test is to recognize patients with a positive oral glucose tolerance test. Values greater than 177 mg/dl after the oral glucose challenge screening test, determine the need of the oral glucose tolerance test to diagnose gestational diabetes for its high specificity.
Referencias
1. Metzger BE, the organizing committee: summary and recommendations of the third international workshop-conference on gestational Diabetes Mellitus. Diabetes 1991; 40 (Suppl. 2):197–201. [ Links ]
2. Expert Committee on the Diagnosis and Classification of Diabetes Mellitus: Report of the expert committee on the diagnosis and classification of Diabetes Mellitus. Diabetes Care 1997; 20: 1183- 1197. [ Links ]
3. O`Sullivan JB: Diabetes Mellitus after GDM. Diabetes 1991; 29 (Suppl 2):131-135. [ Links ]
4. Peters RK, Kjos SL, Xiang A, Buchanan TA. Long term diabetogenic effect of single pregnancy women with previous gestational diabetes mellitus. Lancet 1996; 347:227-30. [ Links ]
5. Landon M, Catalano P, Gabbe S. Diabetes mellitus. In: Gabbe S, Niebyl J, Simpson J, editors. Obstetrics normal and problem pregnancies. Philadelphia: Churchill Livingstone, 2002: 1081-116. [ Links ]
6. Moore T. Diabetes in pregnancy. In: Creasy R, Resnik R, editors. Maternal-Fetal medicine. Philadelphia: Saunders, 2004: 1023-061. [ Links ]
7. Naylor D, Sermer M, Chen E, Farine D. Selective screening for gestational diabetes mellitus. N Engl J Med 1997; 337:1591-6. [ Links ]
8. Cousins L: pregnancy complications among diabetic women: review 1965-1985. Obstet Gynecol Surv 1987; 42: 140-49. [ Links ]
9. Lemen PM, Wigton TR, Miller-McCarthey AJ, Cruikshank DP. Screening for gestational diabetes mellitus in adolescent pregnancies. Am J Obstet Gynecol 1998; 178: 1251-56. [ Links ]
10. Carpenter MW. Rationale and performance of test for gestational diabetes. Clin Obstet Gynecol 1991; 34: 544-57. [ Links ]
11. Coustan DR, Nelson C, Carpenter MW, Carr SR, Rotondo L, Widness JA. Maternal age and screening for gestational diabetes: a population-based study. Obstet Gynecol 1989; 73: 557-61. [ Links ]
12. Coustan DR. Methods of screening for and diagnosing of gestational diabetes. Clin Perinatol 1993; 20: 593-602. [ Links ]
13. Coustan DR. Screening and diagnosis of gestational diabetes. Semin Perinatol 1994; 18: 407-13. [ Links ]
14. Bonomo M, Gandini ML, Mastropasqua A, Begher C, Valentini U, Faden D, et al. Which cutoff level should be used in screening for glucose intolerance in pregnancy? Am J Obstet Gynecol 1998; 179: 179-85. [ Links ]
15. National Diabetes Data Group: Classification and diagnosis of diabetes mellitus and other categories of glucose intolerance. Diabetes 1979; 28: 1039-57. [ Links ]
Servicio de Obstetricia, Hospital de las Mujeres "Dr. Adolfo Carit Eva", Caja Costarricense de Seguro Social
Abreviaturas: DG, diabetes gestacional; HOMACE, Hospital de las Mujeres "Dr. Adolfo Carit Eva"
Correspondencia: Leonardo Orozco S. Apartado 11619- 1000 San José.