Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Acta Médica Costarricense
versión On-line ISSN 0001-6002versión impresa ISSN 0001-6012
Acta méd. costarric vol.44 no.4 San José dic. 2002
Justificación: El cáncer de cérvix es la patología neoplásica más frecuente entre la población femenina. En casos de invasión localizada, la histerectomía radical puede considerarse un tratamiento curativo, sin embargo, el sangrado transoperatorio significativo hace necesaria la transfusión en muchos casos, con todas las complicaciones que esta conlleva. Hasta donde sabemos, no hay ningún estudio publicado en la bibliografía nacional, acerca de la técnica de hemodilución isovolémica para reducir los requerimientos transfusionales en estas pacientes.
Objetivos:a) Hacer experiencia clínica con la Hemodilución isovolémica en pacientes sometidas a histerectomía radical por cáncer de cérvix; b) Evaluar la utilidad de la Hemodilución isovolémica como un método para reducir la necesidad de transfusión de sangre alogénica.
Materiales y métodos: El estudio fue prospectivo. Se seleccionó en forma consecutiva a todas las pacientes sometidas a histerectomía radical por cáncer de cérvix, del Servicio de Ginecología Oncológica del Hospital Dr. Rafael Ángel Calderón Guardia, entre los meses de enero de 2000 a enero de 2001. Se realizó sangría, a través de una línea arterial, un volumen hemático calculado con base en el peso y el hematocrito de la paciente. La sangre autóloga fue retransfundida al término de la cirugía.
Resultados: Un total de 12 pacientes fueron incluidas en el estudio. La edad promedio fue de 55,5 ± 10,4 años. La mayoría tuvo el cáncer de cérvix en estadío I-B1 (n = 10), el resto, en el estadío I-B2 (n = 1) y I-A2 (n = 1). Se obtuvo un promedio de 1208 ml de sangre autóloga por paciente. El procedimiento fue bien tolerado, excepto en una, quien presentó compromiso hemodinámico atribuible a la sangría. Al comparar los valores basales con los obtenidos antes de la retransfusión, se observó un descenso promedio de la hemoglobina, hematocrito y plaquetas de 4,2 g/dl, un 14,4% y 52.000/µl, respectivamente. Ninguna de las pacientes ameritó transfusión de sangre alogénica.
Conclusiones: La hemodilución isovolémica preoperatoria es una técnica sencilla y eficaz para reducir la necesidad de transfusión de sangre alogénica en pacientes sometidas a histerectomía radical por cáncer de cérvix. Se asocia con una baja incidencia de complicaciones, pero es recomendable la vigilancia estrecha del estado hemodinámico transoperatorio, en especial durante el momento de la sangría.
Descriptores: Anemia, hemodilución, sangrado, cáncer, complicaciones, transfusión alogénica. Recibido: 02 de abril, 2002
Aceptado: 08 de octubre, 2002
Abreviaturas: HDIV (hemodilución isovolémica)
El cáncer de cérvix ocupa el primer lugar entre las neoplasias que afectan a la población femenina. 1 ,2 En etapas tempranas (carcinoma in sit u), la conización o histerectomía simple
puede ser suficiente, sin embargo, cuando el tumor se extiende más profundamente, pero sin invasión extrauterina, amerita de histerectomía total con linfadenectomía pélvica, procedimiento conocido como histerectomía radical. 2 ,3 Este tipo de cirugía se asocia con pérdida sanguínea importante, que explica la necesidad de transfusión sanguínea en muchos casos. 4-6
Si bien el uso clínico de las transfusiones sanguíneas ha abierto nuevas perspectivas en la cirugía, pronto se empezó a evidenciar que se asocian con riesgos significativos que incluyen: a) reacciones hemolíticas, b) alergia, c) anafilaxis, d) reacciones debidas a pirógenos, e) sobrecarga circulatoria, f) hemosiderosis, g) sensibilización inmunológica y g) transmisión de enfermedades infecciosas. 7 ,8 En un inicio la trans-misión de enfermedades infecciosas fue la principal preocu-pación. Ésta ha disminuido marcadamente con las pruebas sofisticadas de tamizaje, aunque no se ha podido erradicar por completo (p.ej., el riesgo de transmisión de hepatitis C es de 1:1000 y de HIV de 1:400.000). 9-11 La transfusión de sangre alogénica es un trasplante de células extrañas, que causa reacciones inmunológicas. 3 Medawar, en 1946, propuso por primera vez los efectos inmunomoduladores inducidos por la transfusión, siendo corroborados en estudios subsiguientes, al observar una mayor incidencia de infecciones postoperatorias y recurrencia tumoral posterior a una resección curativa, cuando se compararon grupos de pacientes transfundidos y no transfundidos. 12 Otro punto por considerar en la terapia transfusional es que en la actualidad los médicos deben establecer tratamientos que sean económicamente justificables y ventajosos para el paciente, debido a que los hemoderivados son recursos escasos y sumamente costosos.13 ,14
La transfusión a pacientes con anemia perioperatoria es motivo de controversia. 15 La simple transfusión de glóbulos rojos no siempre necesariamente mejora el resultado de los pacientes anémicos. 16-19 Los valores marcadamente bajos de hemoglobina pueden ser bien tolerados en pacientes quirúr-gicos, aún en aquellos que tienen cierto grado de compromiso de la función cardiovascular. 20 ,21 La hemodilución es una técnica que consiste en extraer sangre del paciente, la cual se conserva en la sala de operaciones y es retransfundida al término de la cirugía. Con el fin de evitar compromiso hemodinámico por la hipovolemia aguda, se infunde cristaloides a razón de 3 ml por cada 1 ml de sangre extraída, o coloides a razón de 1 ml por cada 1 ml de sangre extraída. 22-25
Materiales y métodos
El estudio fue aprobado por el Comité de Bioética e Investigación para el Proyecto de Investigación del Hospital Dr. Rafael Angel Calderón Guardia, y se obtuvo el consentimiento firmado de las pacientes. Se seleccionó en forma prospectiva y consecutiva a todas las pacientes sometidas a histerectomía radical por cáncer de cérvix en estadíos I-A y I-B, del Servicio de Ginecología Oncológica del Hospital Dr. Rafael Ángel Calderón Guardia, entre los meses de enero de 2000 y enero de 2001. Los criterios de exclusión fueron: shock ó inestabilidad hemodinámica, cardiopatía isquémica, hemoglobina pre-operatoria <9 g/dl, neumopatía, coagulopatía, enfermedad cerebrovascular y rechazo del método por parte de la paciente. Se siguieron las pacientes durante toda su estancia hospitalaria.
El día previo a la cirugía se realizó la valoración preanestésica y todas las pacientes fueron premedicadas con lorazepam 2 mg la noche anterior, y 2 mg la mañana de la cirugía. Al llegar a sala de operaciones se administró midazolam 3 mg IV STAT y se tomaron accesos vasculares (2 vías venosas periféricas #18 y una línea arterial radial #20). Se procedió luego a la monitorización (electrocardiografía continua, presión arterial no invasiva cada 2,5 minutos, temperatura esofágica y diuresis a través de una sonda de Foley). La inducción anestésica se realizó con pentotal 4-7 mg/kg IV, fentanil 1 µg/kg IV y atracurio 0,5 mg/kg IV. El mantenimiento de la anestesia se efectuó con enfluorano, fentanil 1 µg/kg IV c/20-30 minutos, según necesidades, y atracurio 0,1-0,2 mg/kg IV c/20-30 minutos. Inmediatamente antes de la incisión quirúrgica, se inició la sangría a través de la línea arterial, hacia una bolsa que contiene una solución anticoagulante con citrato, fosfato, dextrosa y adenina (CPDA-1) (véase Figura 1 ).
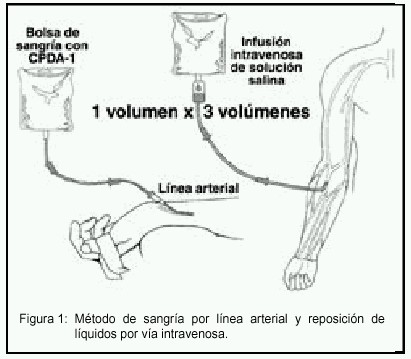
El volumen de sangría permisible se calculó mediante la fórmula: 23 ,26
Volumen de sangría permisible = Volemia X Hematocrito de la paciente-hematocrito mínimo permitido
La volemia se estimó mediante la fórmula: 70 ml x peso de la paciente en kilogramos. El hematocrito mínimo permitido fue establecido en 28%, con base en la literatura. 24 Para determinar el volumen de la sangría se utilizó una balanza, sabiendo que 1 ml de sangre equivale a aproximadamente 1 gramo de peso. En el brazo contralateral se administró a chorro, de forma simultánea cristaloide (solución salina 0,9%) a un volumen equivalente a 3 veces el volumen de la sangría. En caso de presentar inestabilidad hemodinámica, se detuvo de inmediato la sangría. Las bolsas de sangre obtenidas fueron rotuladas con los datos de la paciente y enumeradas según el orden en que fueron recolectadas, y se guardaron en la sala de operaciones a temperatura ambiental. Se administró solución salina con un 0,9% de mantenimiento, a una tasa de 12 ml/kg/h. Se inició la retransfusión de la sangre autóloga inmediatamente posterior al cierre de la incisión quirúrgica, o cuando hay compromiso hemodinámico atribuido a la pérdida hemática. La retransfusión se hizo en orden inverso a como fueron obtenidas las bolsas de sangre autóloga. Se tomaron muestras sanguíneas para gases arteriales, hemograma y pruebas de coagulación (tiempo de protrombina y tiempo de tromboplastina parcial), antes de la inducción anestésica, antes de la retransfusión autóloga y en el postoperatorio, a las 6 y 24 horas. Se transfundió sangre alogénica en caso de presentarse anemia aguda (hemoglobina <9 g/dl) asociada a inestabilidad hemodinámica. 27 Se estimaron las pérdidas sanguíneas por medio de la observación del estado del campo quirúrgico, la comparación de la diferencia entre los pesos seco vs húmedo de las gasas, cuadros y paños utilizados y la medición del volumen recolectado a través de los aspiradores y drenos.
Resultados
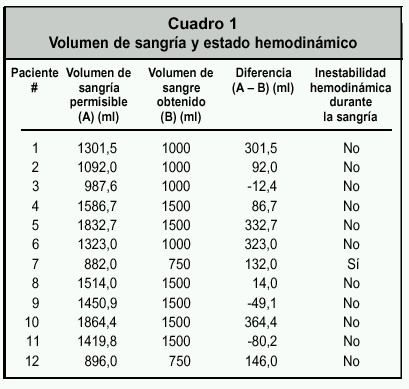
Un total de 12 pacientes fueron incluidas en el estudio. Una paciente fue excluida debido a que presentaba anemia de base. La edad promedio fue de 55,5 ± 10,4 años (rango de 40 a 71 años). La estancia hospitalaria promedio fue de 5,5 ± 1,1 días (rango de 3 a 7 días). La tasa de mortalidad intrahospitalaria fue de un 0%. El peso promedio fue de 63,6 ± 8,5 kg (rango de 50 a 84 kg). La talla promedio fue de 155,7 ± 8,7 cm (rango de 148 a 174 cm). El índice de masa corporal promedio fue de 26,3 ± 3,2 kg/cm 2 (rango de 20,3 a 28,4 kg/cm 2). Cinco pacientes fueron de la categoría ASA I y el resto de ASA II. Nueve fueron de la categoría Goldman I y tres de la categoría Goldman II. Hubo cinco pacientes hipertensas y una diabética. La mayoría tuvo el cáncer de cérvix en estadío I-B1 (n = 10), el resto fueron de estadío I-B2 (n = 1) y I-A2 (n = 1). El tiempo anestésico promedio fue de 172,1 ± 45,6 minutos, mientras que el tiempo quirúrgico promedio fue de 138,3 ± 42,4 minutos. Se obtuvo un promedio de 1208 ml de sangre autóloga por paciente. A nueve se les realizó una sangría de un volumen menor que el permisible, mientras que en tres el volumen de sangría fue apenas superior al permisible (véase Cuadro 1 ). El procedimiento fue bien tolerado, excepto en una paciente, quien presentó compromiso hemodinámico atribuible a la sangría, que, fue pronto, resuelto deteniendo la extracción hemática.
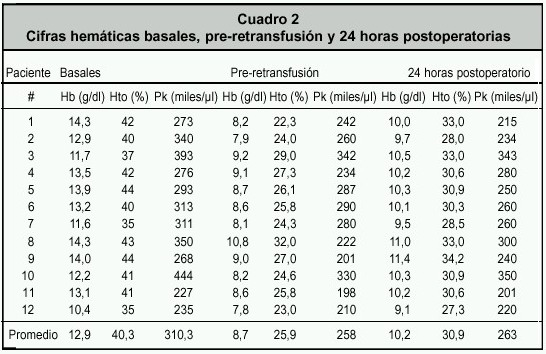
Las cifras basales promedio de hemoglobina (Hb), hematocrito (Hto) y plaquetas (Pk) fueron de 12,9 g/dl, 40,3% y 310.300/µl, respectivamente (véase Cuadro 2 ). El tiempo parcial de tromboplastina (TPT) y el tiempo de protrombina (TP) basales fue de 31,8 segundos y un 90,9%, respectiva-mente. Al comparar los valores basales con los obtenidos antes de la retransfusión, se observó un descenso promedio de la hemoglobina, hematocrito y plaquetas de 4,2 g/dl, un 14,4% y 52.000/µl, respectivamente. A las 24 horas, luego de la retransfusión autóloga y tomando en cuenta las pérdidas sanguíneas postoperatorias por los drenos, el descenso promedio de las cifras de hemoglobina, hematocrito y plaquetas con respecto a las cifras basales fue de 2,7 g/dl, un 9,4% y 47.500/µl, respectivamente. El volumen estimado de pérdida hemática transoperatoria fue de 765 ml, mientras que el volumen promedio de sangre recolectada en los drenos en el primer día postoperatorio fue de 340 ml. Ninguna de las pacientes ameritó de transfusión de sangre alogénica. Una presentó complicaciones asociadas con la cirugía (laceración vesical exitosamente reparada). Se observó cambios mínimos en el pH al comparar los gases arteriales tomados en el período de pre inducción vs pre-retransfusión (7,35 vs 7,32). También se observó un ligero descenso del bicarbonato (22,0 vs 17,3 mEq/l) y un incremento en el exceso de base (– 4,3 vs – 6,4 mEq/l). Todas las pacientes mantuvieron un intercambio gaseoso dentro de límites normales.
Discusión
La hemodilución isovolémica es una técnica de hemoconservación que aprovecha las facilidades del monitoreo intraoperatorio para recolectar sangre fresca antes del inicio de la cirugía, con el fin de ser retransfundida al término. 28-32 Aplicamos esta técnica a las pacientes sometidas a histerectomía radical, por ser un grupo con sangrado intra y postoperatorio importante. Sin el uso de técnicas de hemoconservación, muchas de ellas terminan siendo transfundidas con sangre alogénica, ya sea en sala de operaciones o en el periodo postoperatorio. 6 ,33 ,34 En un informe de Spirtos et al, que incluyó 504 pacientes sometidas a histerectomía radical por cáncer de cérvix, en donde no se utilizó ninguna técnica de hemoconservación, hubo necesidad de transfusión alogénica en el 77,6% de los casos. 35 La técnica en general fue bien tolerada, con mínimos cambios hemodinámicos durante la sangría. Solo una de las pacientes presentó compromiso hemodinámico significativo, que obligó a detener la recolección. A ella se le logró recolectar 750 ml de sangre autóloga y no hubo necesidad de transfusión de sangre alogénica. Aún así, su volumen de sangría de esta paciente se aproximó al máximo permisible.
Como es de esperar, luego de la hemodilución hubo descenso de los valores de la hemoglobina, hematocrito y plaquetas, con respecto a las cifras basales; sin embargo, no se asoció con efectos adversos, probablemente porque la disminución fue discreta. Es interesante observar que aún cuando hubo cifras bajas de hemoglobina en el transoperatorio, ninguna de ellas presentó inestabilidad hemodinámica. Lo anterior se apoya también los mínimos cambios gasométricos, antes y después de la retransfusión autóloga. Estos hallazgos se sustentan por el hecho de que al infundir un volumen de cristaloides en una relación de 3:1, se logra prevenir la hipovolemia, que en última instancia sería la causante de las alteraciones hemodinámicas.
24 ,36-38
Este método de hemoconservación fue efectivo, debido a que ninguna de nuestras pacientes ameritó transfusión alogénica. Lo anterior se explica al comparar el volumen promedio de sangría obtenido (1208 ml), el cual fue muy semejante igual al volumen promedio estimado de pérdida sanguínea en el trans y postoperatorio (1105 ml). Estos datos concuerdan con los reportados por Mirhashemi et al. 6
Como la sangría remueve también factores de coagulación y hubo a la hemodilución con cristaloides, sus niveles (aunque no fueron determinados en nuestro estudio) deben descender. 39 Esta disminución no se reflejó clínicamente (ninguna de las pacientes presentó evidencia macroscópica de coagulopatía) ni en las pruebas de coagulación. Lo anterior se explica por el hecho de que las alteraciones en la hemostasia solo se presentan cuando la actividad de los factores de coagulación hayan descendido a menos de un 30% con respecto a los valores normales. 7 Algunos autores encontraron que la hemodilución mejora la coagulación, debido a que también se diluyen los factores anticoagulantes endógenos, tales como la antitrombina III, la proteína C y S, entre otros. 12 Si bien hubo un descenso promedio de un 16,7% del conteo plaquetario (basal = 310.000/µl vs pre-retransfusión = 258.000/µl), no fue lo suficientemente severo para causar coagulopatía. Lo anterior concuerda con informes de la bibliografía, en los que se observó sangrado por trombocitopenia, solo cuando el conteo plaquetario descendido a menos de 50.000/µl. 23 Pese al tamaño relativamente pequeño de la muestra, los resultados del estudio demuestran que la hemodilución isovolémica preoperatoria es un método eficaz para reducir la exposición a la sangre alogénica. Dado que el seguimiento de las pacientes se dio solo durante su estancia intrahospitalaria, no se puede concluir acerca del efecto sobre el riesgo de la recidiva tumoral a largo plazo. Se requiere de más estudios prospectivos y controlados, que incluyan un número mayor de pacientes para poder hacer una recomendación definitiva de la técnica de la hemodilución isovolémica preoperatoria.
Abstract
Justification: Cervical cancer is the most frequent neoplasic pathology among the feminine population. In cases of localized invasion, radical hysterectomy should be considered a curative treatment. However a significative transoperative bleeding makes a transfusion necessary in many cases, with all the complications that this endures. As far as we know there is not a published study about the isovolemic hemodilution technique to reduce the transfusional requirements in these patients in the national literature.
Objective: Demonstrate that the isovolemic hemodilution reduces the necessity of allogeneic blood transfusion in patients who have undergone radical hysterectomy.
Materials and methods: The study was prospective. All of the chosen patients, were selected in consecutive order and they received radical hysterectomy due to cervical cancer in stage I-B1 (n=10), the rest of the patients were in stage I-B2 (n-1) and I-A2 (n=1). Attaining an average of 1208 ml of autologous blood per patient. The procedure was well toler-ated, except one case where the patient presented hemodynamic compromise attributable to the blood withdrawing. Comparing the basal values with the ones obtained before retransfusion, we observed an average decrease of the hemoglobin, hematocrit and platelets of 4.2 g/dl, 14.4% and 52.000/µl respectively. None of the patients required allogeneic blood transfusion.
Referencias
1 Odicino F, Favalli G, Zigliani L, Pecorelli S. Staging of gynecologic malignancies. Surg Clin North Am 2001; 81:753-79 [ Links ]2 Abu-Rustum NR, Hoskins WJ. Radical abdominal hysterectomy. Surg Clin North Am 2001; 81:815-28 [ Links ]
3 Averette HE, Wrennick A, Angioli R. History of gynecologic oncology subspecialty. Surg Clin North Am 2001; 81:747-52 [ Links ]
4 Tomacruz RS, Bristow RE, Montz FJ. Management of pelvic hemorrhage. Surg Clin North Am 2001; 81:925-48 [ Links ]
5 Kanter MH, Van Maanen D, Anders KH, Castro F. Perioperative autologous blood donations before elective hysterectomy. JAMA 1996; 276:798-801 [ Links ]
6 Mirhashemi R, Averette HE, Deepika K. The impact of intraoperative autologous blood transfusion during type III radical hysterectomy for early-stage cervical cancer. Am J Obstet Gynecol 1999; 181:1310-5 [ Links ]
7 Algora-Weber M, Fernández-Montoya A, Gómez-Villagran JL. Guía sobre la indicación de la transfusión de glóbulos rojos, plaquetas y pro-ductos plasmáticos lábiles. Junta Directiva de la Sociedad Española de Transfusión Sanguínea. Med Clin 1999; 113:471-4 [ Links ]
8 Blumberg N, Heal JM. Immunomodulation by blood transfusion: an evolving scientific and clinical challege. Am J Med 1996; 101:299-308 [ Links ]
9 Donahue JG, Muñoz A, Ness PM. The declining risk of post transfusion hepatitis C virus infection. N Engl J Med 1992; 327:369 -75 [ Links ]
10 Heiss MM. Risk of allogeneic transfusions. Br J Anaesth 1998; 81(suppl. 1):16-19 [ Links ]
11 Dodd RY. The risk of transfusion-transmitted infection. N Engl J Med 1992; 327:419-24 [ Links ]
12 Spahn DR, Casutt M. Eliminating blood transfusions: new aspects and perspectives. Anesthesiology 2000; 93:242-55 [ Links ]
13 Mercuriali F, Inghillieri. Management of preoperative anaemia. Br J Anaesth 1998; 81(suppl. 1):56-61 [ Links ]
14 Faust RJ. Perioperative indications for red blood cell transfusion: has the pendulum swung too far?. Mayo Clin Proceedings 1993; 68:512-4 [ Links ]
15 Carson JL. Duff A, Berlin JA, Lawrence VA. Perioperative blood transfusion and postoperative mortality. JAMA1998; 279:199-205 [ Links ]
16 Carson JL, Poses RM, Spence RK, Bonavita G. Anaemia and surgery: the relationship between the severity of anaemia and surgical mortality and morbidity. Lancet 1988; 1:727-9 [ Links ]
17 Chen AY, Carson JL. Perioperative management of anaemia. Br J Anaesth 1998; 81(suppl. 1):20-4 [ Links ]
18 Viele MK, Weiskopf RB. What can we learn about the need for transfusion from patients who refuse blood?. The experience with Jehovah´s Whitnesses. Transfusion 1994; 34:396-401 [ Links ]
19 Wahr JA. Myocardial ischaemia in anaemic patients. Br J Anaesth 1998; 81(suppl. 1):10-5 [ Links ]
20 Díaz-Espallardo C, Moral-García V. Cost-effectiveness analysis of an autotransfusion program in primary knee and hip replacement surgery. Rev Esp Anestesiol Reanim 1999; 46:396-403 [ Links ]
21 Ness PM, Bourke DL, Walsh PC. A randomized trial of perioperative hemodilution versus transfusion of preoperatively deposited autologous blood in elective surgery.Transfusion 1992; 32:226-34 [ Links ]
22 Kafer ER, Isley MR, Hansen T.Automatic acute normovolemic hemodilution reduces blood transfusion for spinal fusion. Anesth Analg 1986; 65:S86-93 [ Links ]
23 Stehling L, Zauder HL. Acute normovolemic hemodilution. Transfusion 1991; 31:857-64 [ Links ]
24 Trouwborst A, Van Bommel J, Ince C, Penny CP. Monitoring normovolaemic haemodilution. Br J Anaesth 1998; 81(suppl. 1):73-8 [ Links ]
25 Karakaya D, Ustun E, Tur A. Acute normovolemic hemodilution and nitroglycerin-induced hypotension: comparative effects on tissue oxygenation and allogeneic blood transfusion requirement in total hip arthroplasty. J Clin Anesth 1999; 11:368-74 [ Links ]
26 Spence RK. Preoperative packed cell volume necessary for patients undergoind elective surgery. Br J Anaesth 1998; 81(suppl. 1):50-5 [ Links ]
27 Practice guidelines for blood component therapy: a report of the American Society of Anesthesiologist Task Force on Blood Component Therapy. Anesthesiology 1996; 84:732-47 [ Links ]
28 Weiskopf RB. More on the changing indications for transfusion of blood and blood components during anesthesia. Anesthesiology 1996; 84:498-501 [ Links ]
29 Speiss BD, Sassetti R, McCarthy RJ. Autologous blood donation: hemodynamics in a high-risk patient population. Transfusion 1992; 32:17-23 [ Links ]
30 Gombotz H, Metzler H, List WF. Methods for reduction of perioperative bleeding. Br J Anaesth 1998; 81(suppl. 1):62-6 [ Links ]
31 Goodnough LT. Controversies in autologous blood procurement. Br J Anaesth 1998; 81(suppl. 1):67-72 [ Links ]
32 Schmied H, Schiferer A, Sessler DI, Meznik C. The effects of red cell scavenging, hemodilution, and active warming on allogeneic blood requirements in patients undergoind hip or knee arthrosplasty. Anesth Analg 1998; 36:387-91 [ Links ]
33 Combs CA, Murphy EL, Laros RK. Cost-benefit analysis of autologous blood donation in obstetrics. Obstet Gynecol 1992; 80:621-9 [ Links ]
34 Thomas MJ, Desmond M, Gillon J. Preoperative autologous donation: what was the impact of the 1995 consensus statement?. Transfus Med 1999; 9:241-57 [ Links ]
35 Spirtos M, Westby CM, Averette HE, Soper JT. Blood transfusion and the risk of recurrence in squamous cell carcinoma of the cervix: a Gynecologic Oncology Group Study. URL:
http://www.women-scancercenter.com/resource/research/gogtrans.html 2001
36 Toy P, Ahn D, Bachetti P. When should the first of two autologous donations be made?. Transfusion 1994; 34:S14-9 [ Links ]
37 Habler O, Mebmer K. Hyperoxaemia in extreme haemodiution. Br J Anaesth 1998; 81(suppl. 1):79-82 [ Links ]
38 Van Iperen CE, Biesma DH, Van de Wiel A, Marx JJM. Erythropoietic response to acute and chronic anaemia: focus on postoperative anaemia. Br J Anaesth 1998; 81(suppl. 1):2-5 [ Links ]
39 Herbert WNP, Owen HG, Collins ML. Autologous blood storage in obstetrics. Obstet Gynecol 1988; 72:166-72 [ Links ]
1 Residente de Anestesiología y Recuperación.
2 Jefe de Servicio de Ginecología Oncológica).
3 Asistente de Hematología.
Institución: Hospital Dr. Rafael Ángel Calderón Guardia.
Correspondencia: kwokho123@hotmail.com














