Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Acta Médica Costarricense
On-line version ISSN 0001-6002Print version ISSN 0001-6012
Acta méd. costarric vol.43 n.4 San José Oct. 2001
Justificación: La oclusión trombótica de las venas cerebrales o senos durales es una causa menos frecuente de enfermedad cerebrovascular que la trombosis arterial. Sin embargo; los estudios epidemiológicos indican que esta entidad no es tan inusual como o ser pensaba previamente. Hasta donde sabemos, no hay ningún estudio publicando al respecto en la literatura nacional, siendo precisamente el motivo del presente trabajo.
Objetivos: Identificar las características demográficas, clínicas y diagnósticas de los pacientes que sufrieron una trombosis de senos venosos durales. Describir los métodos terapéuticos empleados y la evolución que tuvieron estos pacientes.
Materiales y métodos: Se revisaron los expedientes clínicos de 11 casos diagnosticados de trombosis de senos durales en el Hospital Dr. Rafael Ángel Calderón Guardia, en el período comprendido entre enero de 1996 a enero de 1999. Se analizaron los posibles factores de riego, formas de presentación clínica, estudios de radio imagen y tratamiento empleado.
Resultados: El promedio de edad fue de 32,6 años. Un 18,2% fueron varones, mientras que el 81,8% correspondió a mujeres. Las manifestaciones más frecuentes fueron: cefalea (100%), vómito (91%), déficit motor 882%), alteración del sensorio (73%), papiledema (54,5%), crisis convulsiva (54,5%) y datos de irritación meníngea (36,4%): el signo del delta vacío se documentó en 27,3% de los estudios tomográficos. El seno sagital superior fue el más frecuentemente afectado (91%). Se anticoaguló con heparina intravenosa al 54, 5% de los casos.
Conclusiones: Aunque somos conscientes de las limitaciones de nuestra serie, nuestra intención ha sido llamar la atención sobre una patología vascular cerebral, que aunque no es tan frecuente como su contraparte arterial, debe tenerse en consideración por sus potenciales efectos sobre la salud del paciente. El conocimiento adecuado de esta condición es importante, debido a que aún cuando los síntomas son severos, la reversibilidad puede ser completa.
Descriptores: Trombosis, seno dural, diagnóstico, anticoagulación.
Recibido: 19 de julio de 2001.
Aceptado: 23 de octubre de 2001.
Introducción
El primer caso de TSD fue reportado en 1825 por Ribes, de un paciente masculino de 45 años con trombosis del seno sagital superior, en asociación con una nepolasia de fondo.1 desde entonces ha sido reportada en virtualmente todo tipo de pacientes, en especial la población obstétrica.2,3 La primera desccripción clinicopatológica de una TSD durante el post-parto fue por John Abercrombie, en 1828.4 Es una entidad clínica tradicionalmente considerada como poco frecuente; sin embargo, los datos epidemilógicos indican que no es tan inusual como se pensaba. 2,3,5 Es menos común que la trombosis arterial; sin embargo, su diagnóstico es frecuentemente pasado por alto. Los estudios patológicos revelan signos de TSD en más de 9% de los casos de autopsia no seleccionados, lo cual sugiere que muchos nunca fueron diagnosticados antemortem. 6,7
El flujo sanguíneo cerebral es drenado por varias venas principales, las cuales, llevan la sangre hacia los senos durales. Los principales senos son el sagital superior, sagital inferior, recto, laterales, cavernoso y sigmoideos. La obstrucción del flujo venoso produce un cuadro clínico de hipertensión intracraneana (trastorno del sensorio, cefalea, náusea, vómito, etc) asociado con paresia o alteraciones sensitivas y con frecuencia crisis convulsivas. 1,4 Se puede observar disminución del nivel de conciencia y papiledema. No obstante, son posibles muchas otras presentaciones clínicas. Fisiopatológicamente se caracteriza por una alteración del equilibrio entre los factores trombogénicos y fibrinolíticos endógenos. Aún cuando los síntomas neurológicos son severos, la reversibilidad puede ser completa, debido a que son regiones cerebrales funcional o metabólicamente trastornadas, pero que todavía pueden ser recuperadas (análogo al concepto de la penumbra en la isquemia cerebral por oclusión arterial). 4 La mortalidad general se sitúa en el 10-30% según diferentes series. 2,5,8 En el diagnóstico, la tomografía cerebral es útil y suele mostrar lesiones hipodensas o hemorrágicas y signos indirectos de TSD. 9 La angiografía en la fase venosa es la prueba diagnóstica definitiva. 10,11 La RMN ny en especial la angio-RMN tiene una elevada especificidad diagnóstica. 12,14 Otro método de diagnóstico cada vez más utilizado y con resultados prometedores es el ultrasonido Doppler transcraneano. 15-18 El tratamiento con antibióticos ha mejorado de forma notable la evolución de las trombosis sépticas, mientras que al administración de anticoagulantes (heparina intravenosa) se ha mostrado útil en las series más recientes. 3, 19-21 en casos seleccionados, se ha utilizado trombolisis in situ con buenos resultados. 22-27
Materiales y Métodos
Se revisaron los expedientes clínicos de todos los casos de TSD en el Hospital Dr. Rafael Angel Calderón Guardia, en el período comprendido entre enero de 1996 a enero de 1999. Un total de 11 casos de TSD fueron diagnosticados en el período de estudio. Se consideró diagnóstico de TSD cuando hubo un cuadro clínico y hallazgos compatibles en los estudios de neuroimagen (TAC, RMN, angio-RMN ó RMN fueron reportados por un neuroradiólogo, mientras que las angiografías cerebrales fueron interpretadas por el neurocirujano que realizó el procedimiento. Se analizaron los posibles factores de riesgo para trombosis en general, así como los factores de riesgo para trombosis en general, así como los factores de riesgo más específicos para la TSD o venosa sistémica previa y la posible coexistencia de factores hematológicos. Se dividió el modo de presentación en agudo ( < 48 hora) ó insidioso ( > 48 horas) y la progresión clínica en temprana (> 10 días) o tardía (< 10 días). Se tomaron datos de examen físico general y neurológico completo, así como los resultados del hemograma, bioquímica completa y coagulación. Los resultados del TAC de cráneo se clasificaron en : 1) examen normal, 2) signos directos de trombosis: signo de delta vacío, signo de la cuerda y signo del triángulo denso, 3) signos directos de trombosis: reforzamiento por el medio de contraste del falx cerebral y el tentorio cerebelar, disminución del tamaño verticular asociado a edema cerebral y 4) presencia de infartos venosos o arteriales asociados.
Resultados
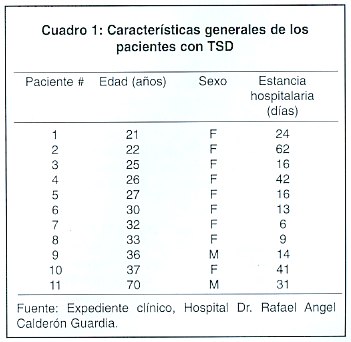
El promedio de edad fue de 32,6 + 13,5 años, siendo el rango de 21-70 años (Cuadro 1). Un 18,2% de los pacientes fueron varones, mientras que el 81,8% restante correspondió a mujeres (relación varón: mujer = 1:4,5). El promedio de estancia intrahospitalaria fue de 17,3 + 17,3 días, con un rango de 6-62 días.
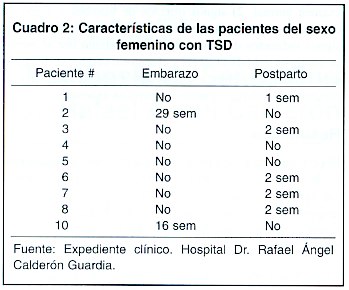
De las 9 pacientes incluidas en el estudio, 2 estaban cursando un embarazo y 5 en el período puerperal. La totalidad de los casos de TSD puerperal ocurrieron en las primeras dos semanas postparto (Cuadro 2). Ninguna de ellas fue después de un aborto. El promedio de embarazos fue de 2,3 gestas al momento de la aparición de la trombosis. La única paciente nulípara estaba en planificación con gestágenos orales. Ninguna de las pacientes estaba en terapia hormonal sustitutiva.
Se planteó al momento de ingreso el diagnóstico de TSD en 27,3% de los pacientes (n=3). Otros diagnósticos fueron: hemorragia subraracnoidea (n=2), meningoencefalitis (n=2), hiperemesis gravídica (n=1), malformación arteriovenosa (n=1), endometritis puerperal (n=1) y crisis convulsiva en estudio (n=1.e l tiempo promedio transcurrido desde el momento de la consulta al Servicio de Emergencias hasta la sospecha del diagnóstico fue de 3,5 días (rango 1 a 13 días).
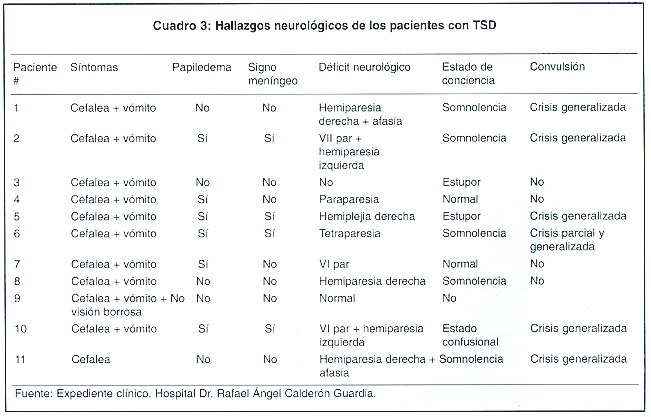
La presentación aguda de los síntomas ocurrió en el 54,5% de los casos (n=6), mientras que la forma insidiosa fue en el 45,5% de los casos (n=5). Todos los pacientes tuvieron deterioro clínico durante su internamiento, el cual sucedió en término de 10 días en el 63,6% de los casos (n=7) y luego de < 10 días o más en el 63;4% de los casos (n=4). Los síntomas más frecuentes fueron: la cefalea (100% de los casos) y el vómito, que se presentó en 10/11 (91%), Cuadro 3. Seis pacientes presentaron en algún momento de la evaluación uno o más episodios de crisis convulsiva, siendo más frecuente la forma generalizada. Un total de 8 pacientes (73%) tuvo alguna alteración del estado y/o contenido de la conciencia, distribuido de la siguiente manera: somnolencia en 8/11 (73%) estado confusional en 1/11 (9,1%) y estupor en 2/11 (18,2%). En 9/11 (82%) de los pacientes hubo manifestaciones de compromiso motor. Entre los pacientes que presentaron déficit motores 8/9 (89%) tuvieron plejia o paresia de extremidades, mientras que 2/9 (22%) cursaron con parálisis del VI. Un paciente presentó un VII par acompañado de hemiparesia. En 6/11 (54,5%) se presentaron papiledema. En 4/11 (36,4%) de los pacientes se encontró datos de irritación meníngea.
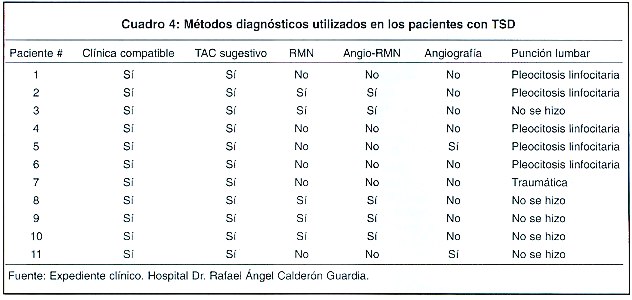
Se realizó un TAC sin medio de contraste a todos los pacientes (Cuadro 4). A 9 pacientes (825) se les realizó adicionalmente un TAC con medio de contraste. A 7 pacientes (63,6%) se les realizaron estudios conformatorios de la TSD [angio-RMN (n=5) y angiografía cerebral convencional (n=2)] a 6 pacientes más frecuente del líquido cefalorraquídeo fue un patrón de pleocitosis linfocitaria (n=5). El tiempo transcurrido desde el momento de la sospecha clínica hasta al confirmación con un método de radioimagen fue de 2,1 días (rango 1 a 8 días).
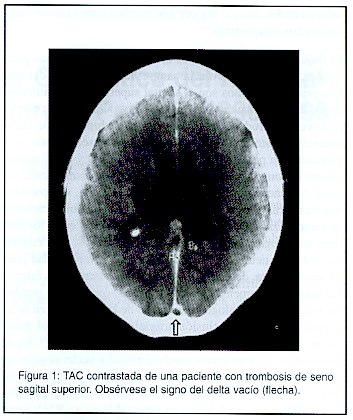
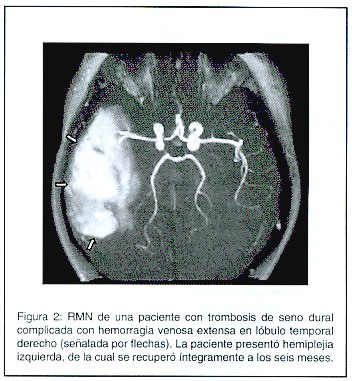
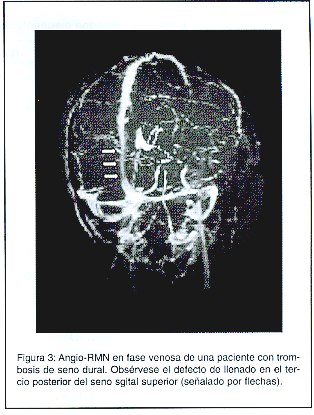
El signo del delta vacío se documentó en 27,3% (n=3) de los estudios tomográficos (Figura 1). Uno de los estudios mostró el signo de la cuerda. Los ventrículos fueron catalogados como pequeños en el 54,5% de los casos (n=6). Ninguno tuvo ventriculomegalia por TAC. Se presentí edema cerebral en 4 pacientes. Tres de los pacientes tuvieron infartos venosos hemorrágicos (figura 2). El SSS fue comprometido en 10 de los pacientes (91%) (Figura 3). En 2 de estos pacientes hubo compromiso concomitante de otro territorio [SSI + seno recto (n=1), seno transverso bilateral + seno recto (n=1)] . Uno de los pacientes tuvo una trombosis del SSI.
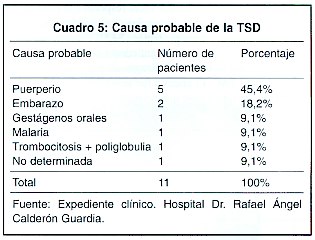
La condición clínica más frecuentemente relacionada con TSD fue el embarazo y puerperio, siendo responsable en el 63;6% de los casos (n=7) (Cuadro 5). Los únicos 3 pacientes a quienes se les realizaron estudios por estados de hipercoagulabilidad (proteína C, proteína S, antitrombina III, anticoagulante lúpico,a nticuerpos anticardiolipina y factor V de Leiden) fueron negativos.
Con respecto al manejo, 10 pacientes fueron ingresados inicialmente a Gineco-Obstetrica ó Neurología (5 pacientes cada servicio). Uno de los pacientes ingresó a Neurocirugía. Ningún paciente ingresó directamente a la Unidad de Cuidados Intensivos, sin embargo el 54,5% de los pacientes ameritó de traslado a este último servicio (n=6). Dos pacientes que ingresaron inicialmente al Servicio de Gineco-Obstetricia fueron valoradas por psiquiatría, debido al planteamiento de un cuadro psiquiátrico. Todos los pacientes desde el momento de su ingreso recibieron heparina sódica subcutánea. Seis pacientes (54,5%) fueron manejados luego con anticoagulación intravenosa (heparina sódica). Se necesitó de un promedio de 5,3 días (rango 1 a 15 días) para que el paciente recibiera tratamiento definitivo desde el momento de la consulta al hospital. Se requirió de un promedio de 2,5 días para lograr una anticoagulación terapéutica (tiempo parcial de tromboplastina 2-2,5 veces respecto a la cifra basal). No hubo complicaciones hemorrágicas asociadas con la terapia anticoagulante. Seis pacientes (54,5%) recibieron manitol intravenoso como medida antiedema ó edema cerebral en el TAC. El epamín fue administrado a 10 pacientes (91%) .El epamín fue administrado a 10 pacientes (91%). El único caso que no recibió anticonvulsivante no presentó crisis convulsivas generalizadas ni focales. Cinco pacientes (45,4%) recibieron nimodipina. Dos pacientes (18,2%) recibieron dexametasona intravenosa. De los pacientes, 6/11 (54,5%) se egresaron con terapia anticoagulante a largo plazo. De éstos, 5 fueron con warfarina oral por espacio de seis meses. Una paciente fue anticoagulada con heparina de bajo peso molecular durante el tercer trimestre del embarazo y posterior al parto se continuó con warfarina oral por seis meses.
La recuperación total se presentó en el 72,7% de los pacientes. Tres pacientes (27,3%) tuvieron secuelas neurológicas [tetraparesia espástica + demencia + epilepsia (n=1), hemiparesia derecha (n=1) y VI para derecha (n=1)]. La montalidad en nuestro estudio fue de 0%.
Discusión
Se logró recopilar 11 casos de TSD, en un período de cinco años, lo que no permiten establecer una incidencia de manera apropiada. Esto no es diferente de lo reportado en la literatura mundial. Ameri et al también establece que la misma es totalmente desconocida. 1 Otros autores como Towbin 7 encontró TSD en 9% de 192 autopsias y Averback 28 en una serie de 7 casos insiste en que la TSD es una enfermedad frecuentemente sub-reconocida, lo que probablemente sea cierta en nuestra casuística, dado que a la fecha, no hay ningún reporte orecio de esta paltolgía en nuestro país. Dos reportes nos sugieren que la incidencia es mucho más alta de aquella reportada en serie de autopsias, dada la baja mortalidad de los casos menos severos de la patología, que obviamente no llegan a sumarse a las incidencias establecidas por medio de necropsia. 2,8 En cuanto a la distribución por género, encontramos que hay predominio de mujeres (81,(%), lo que concuerda con otras series de casos y en particular con un reporte reciente de Morales – Ortiz et al,20 quienes encontraron un 91,7% de mujeres en su casuística y que también había sido encontrado de previo por Estanol et al. 29 En nuestra serie de casos, encontramos una edad promedio de 32,6 + 13,5 años, que se explica por el hecho del predominio de mujeres en edad fértil. A pesar de que se menciona en la literatura mundial una lista significativa de condiciones que pueden causar o predisponer a TSD y que incluyen patologías quirúrgicas, médicas y ginecobstétricas, en nuestra serie es evidente que el embarazo y el puerperio son las causas predominantes (63,6%) y de éstos dos, el puerperio la más común, lo que ya había sido descrito. 2,29,30 Del grupo de pacientes de sexo femenino, la gran mayoría estaban cursando un embarazo (n=2) o en período puerperal (n=7), lo cual concuerda con varios reportes recientes Encontramos que todos los casos de TSD puerperal ocurrieron en las primeras dos semanas postparto. El uso de gestágenos orales fue el factor más evidente en una de las 9 pacientes y esta relación ha sido demostrada en estudios controlados. 31 uno de los problemas de la TSD es la presentación clínica inespecífica. 4,32.
Esto se reflejó e n el presente estudio, ya que se planteó al momento de ingreso el diagnóstico de TSD solo en el 2,3% de los casos. A dos pacientes durante su internamiento se les planteó erróneamente un cuadro conversivo. Se observó un retardo importante en el planteamiento del diagnóstico, cuyo promedio fue de hasta los 3,5 días. Se necesitó un total de 5,3 días para que el paciente recibiera tratamiento definitivo desde el momento de la consulta al hospital. Si partimos del hecho de que la respuesta al tratamiento anticoagulante es tiempo-dependiente, entonces esta demora es evidente inaceptable. 33 La forma de presentación de los síntomas mostró similitud con los datos descritos en la serie de Bousser et al, 2 llamando la atención de que todos los pacientes tuvieron empeoramiento quizás sea el reflejo del retardo en el diagnóstico e inicio de la terapia anticoagulante. Encontramos en nuestra serie una mayor alteración del estado de la conciencia (73%) con respecto a otros reportes. Probablemente se puede atribuir a que nuestros pacientes fueron un grupo con enfermedad más grave, como se reflejó también en la mayor frecuencia de crisis convulsivas (54,5%) y déficit focal (89%) contra la serie de pacientes de Morales – Ortiz et al (33,3%) y 50% respectivamente). 20 El papiledema se presentó con más frecuencia (54,5%) en comparación con el 25% de los casos de la serie de Morales – Ortiz. 20 A todos los pacientes se les realizaron uno o más estudios de TAC; sin embargo este método no es confirmatorio. Prueba de ello es que se requirió en 7 pacientes un estudio adicional (5 RMN con angio-RMN fue diagnóstica en todos los casos en que se realizó, lo cual confirma la opinión actual de que el diagnóstico de TSD hoy en día ha de realizarse con RMN, 34 sobre todo si ésta se realiza precozmente ( en las primeras 2 semanas), d la angiografía convencional solamente para aquellos casos dudosos. La punción lumbar no fue útil en el diagnóstico sino para descartar otras patologías. El signo del delta vacío se documentó en 27,3% de los estudios, lo cual concuerda con la cifra (30%) del reporte de Virapongse. 9 A excepción del signo anterior y el de la cuerda (n=1), no encontramos otros signos indirectos de TSD. Los infartos venosos hemorrágicos fueron tan frecuentes (n=3) como el signo del delta vacío. Esto tiene importantes implicaciones terapéuticas, debido a dos dactores. Primero, puede confundir al clínico con otros diagnósticos tales como la hemorragia subaracnoidea y malformación arteriovenosa. Segundo, puede desalentar el uso de anticoagulantes; que sin embargo, cada día hay más estudios que evidencian la utilidad de la heparina y baja incidencia de complicaciones hemorrágicas. El SSS fue el más comprometido (91%), lo cual concuerda con otras series de casos. 35-40 Tuvimos limitaciones para describir la importancia de los estados de hipercoagulabilidad, debido a que únicamente se envió 3 pacientes para estos estudios, todos con resultados negativos. En un paciente se le asoció con una trombocitosis y poliglobulia. Cabe destacar que esta condición ha sido reportada también en la literatura. 41 El uso de epamín fue común, debido a que más de la mitad de los pacientes tuvieron uno o más episodios de crisis convulsiva. Tanto la nimodipina como los esteroides demostraron ser inefectivos en esta patología; 1 sin embargo, se usaron en algunos de nuestros pacientes (45,4% y 18,2% respectivamente). En referencia al tratamiento empleado, en nuestros casos se optó por manera prioritaria por la anticoagulación, como han recomendado en los últimos años múltiples autores, con buenos resultados en la mayoría de la veces. 2,4,5,19 No hubo complicaciones hemorrágicas asociadas con la terapia anticoagulante, aún cuando se utilizó en pacientes con infartos venosos hemorrágicos. Otros autores, incluso han usado trombolíticos en este grupo de pacientes, sin aparentes complicaciones. 43 La recuperación total se presentó en el 72,7% de los pacientes. Similares hallazgos fueron reportados en un estudio reciente. 43 Solo una paciente tuvo una secuela neurológica invalidante.
Abstract
Justification: The thrombotic occlusiom of the cerebral veins or dural sinuses is a less frequent cause of stroke than arterial thrombosis. However; the epidemiologic studies indicate that this entity is not as unusual as it has been thougth previously. Up to where we know, there is no study published in the national literature being this, in fact, the reason of the present work.
Aim: To identify the demographic, clinical and diagnostic characteristics of patients that suffered dural sinuses thrombosis. To describe the therapeutic methods used and the evolution of these patients.
Materials and methods: Clinical files of 11 diagnosed cases of dural sinues thrombosis in the Hospital Dr. Rafael Angel Calderon Guardia were revised, in the period between January of 1996 to January of 1999. The possible risk factors, clinical presentation, radiologic studies and treatment used were analyzed.
Results: The average age was of 32,6 years. 18,2% were male, while 81,8% corresponded to women. The most frequent manifestations were: headache (100%), vomit (91%), focal deficit (82%), alteration of the mental status (73%), papilledema (54,5%) seizures (54,5%) and data of meningeal irritation (36,4%). The sing of the empty delta was documented in 27,3% of the tomographic studies. The superior sagittal sinus was the most frequently affected (91%). Anticoagulation with intravenous heparin was used in 54,5% of the cases.
Conclusions: Although we are aware of the limitations of our report, our intention has been to cal the attention on a cerebral vscular disease that although it is not as frequent as arterial thrombosis, it should be taken into consideration because of its potential effects on the patient´s health. The appropriate knowledge of this condition is important, because even when the symptoms are severe, the reversiblity can be complete.
Abreviaturas: RMN, renonancia magnética nuclear; SSS, seno sagital superior, SSI, seno sagital inferior; TAC, tomografía axial computarizada; TSD, thrombosis de senos durales
Referencias
1. Ameri A, Bousser MG. Cerebral venous thrombosis. Neurol Clin 1992; 110:87-111. [ Links ]
2.Bousser MG, Chiras J, Sauron B. Cerebral venous thrombosis: a review of 38 cases. Stroke 1985; 16:199-213. [ Links ]
3. Cantú C. Cerebral venous thrombosis associated with pregnancy and puerperium: review of 67 cases. Stroke 1993; 24:1880-4. [ Links ]
4. Villringer A, Einhaupl KM. Dural sinus and cerebral venous thrombosis. New Horizons 1997; 5:332-41. [ Links ]
5. Daif A, Amada E, AI-Rajeh S. Cerebral venous thrombosis in adults: a study of 40 cases from Saudi Arabia. Stroke 1995; 26: 1193-5.
6. Jacobs K. The stroke syndrome of cortical vein thrombosis. Neurology 1996; 47:376-82. [ Links ]
7. Towbin A. The syndrome of latent cerebral venous thrombosis: its frequency and relation to age and congestive heart failure. Stroke 1973; 4:419-30. [ Links ]
8. Krayenbuhl H. Cerebral venous and sinus thrombosis. Clin Neurosurg 1997; 14:1-24.
9. Virapongse C, Cazanave C, Quisling R. The empty delta sign: frequency and significance in 76 cases of dural sinus thrombosis. Radiology 1987; 162:779-85.
10. Ruggieri PM, Masaryk TI, Ross JS. Magnetic resonance angiography: cerebrovascular applications. Stroke 1992; 23:774-80. [ Links ]
11. Casey SO, Alberico RA, Patel M. Cerebral CT venography. Radiology 1996; 198:163-70. [ Links ]
12. Vogl TI, Bergman C, Villringer A. Dural sinus thrombosis: value of venous MR angiography for diagnosis and follow-up. AJR 1994; 162: 1191-8.
13. Isensee Ch, Reul J, Thron A. Magnetic resonance imaging of thrombosed dural sinuses. Stroke 1994; 25:29-34. [ Links ]
14. Dormont D, Anxionnat C, Evrard S. MRI in cerebral venous thrombosis. J Neuroradiol 1994; 21:81-99. [ Links ]
15. Ries S, Steinke W, Neff KW. Echocontrast-enhanced transcranial colorcoded sonography for the diagnosis of transverse sinus venous thrombosis. Stroke 1997; 28:696-700. [ Links ]
16. Wardlaw JM. Transcranial Doppler ultrasound findings in cerebral venous sinus thrombosis. J Neurosurg 1994; 80:332-5.
17. Valdueza JM. Monitoring of venous hemodynamics in patients with cerebral venous thrombosis by transcranial Doppler ultrasound. Arch Neurol 1999; 56:229-34. [ Links ]
18. Canhao P, Batista P, Ferro JM. Venous transcranial Doppler in acute dural sinus thrombosis. J Neurol 1998; 245:276-9. [ Links ]
19. Einhaupl KM, Villringer A, Meister W. Heparin treatment in sinus venous thrombosis. Lancet 1991; 338:597-600. [ Links ]
20. Morales-Ortiz A. Trombosis venosa cerebral en la región de Murcia. Rev Neurol 1998; 26:748-51. [ Links ]
21. Levine SR, Twyman RE, Gilman S. The role of anticoagulation in cavernous sinus thrombosis. Neurology 1988; 38:517-22. [ Links ]
22. Gerszten PC, Welch WC, Spearman MP. Isolated deep cerebral venous thrombosis treated by direct endovascular thrombolysis. Surg Neurol 1997; 48:261-6.
23. Hacke W, Kaste M, Fieschi. Intravenous thrombolysis with recombinant tissue plasminogen activator for acute hemispheric stroke. JAMA 1995; 274: 1017-25. [ Links ]
24. Holder CA. Isolated straight sinus and deep cerebral venous thrombosis: successful treatment and local infusion of urokinase. J Neurosurg 1997; 86:704-7. [ Links ]
25. Horowitz M, Purdy P, Unwin H. Treatment of dural sinus thrombosis using selective catheterization and urokinase. Ann Neurol 1995; 38:5867. [ Links ]
26. Niwa J. Treatment of acute superior sagittal sinus thrombosis by t-PA infusion via venography-direct thrombolytic therapy in the acute phase. Surg Neurol 1998; 49:425-9.
27. D'Alise MD, Fitchel F, Horowitz M. Sagittal sinus thrombosis following minor head injury treated with continuous urokinase infusion. Surg Neurol 1998; 49:430-5. [ Links ]
28. Averback P. Primary cerebral venous thrombosis in young adults: the diverse manifestations of an underrecognized disease. Ann Neurol 1978; 3:81-6. [ Links ]
29. Estanol B, Rodríguez A, Conte G. Intracranial venous thrombosis in young women. Stroke 1979; 10:680-4. [ Links ]
30. Borum SE, Naul LG, McLeskey CH. Postpartum dural venous sinus thrombosis after postdural puncture headache and epidural blood patch. Anesthesiology 1997; 68:487-90.
31. Cerebral Venous Sinus Thrombosis Study Group. Case-control study of risk of cerebral sinus thrombosis in oral contraceptive users who are carriers of hereditary prothrombotic conditions. BMJ 1998; 316:589-92. [ Links ]
32. De Bruijn SF, Stam J, Kappelle LJ. Thunderdap headache as first symptom of cerebral sinus thrombosis. Lancet 1996; 348:1623-5. [ Links ]
33. Minadeo JP, Karaman BA. Headache: cortical vein thrombosis and response to anticoagulation. J Emerg Med 1999; 17:449-53. [ Links ]
34. Ozsvath RR, Casey SO, Lustrin ES. Cerebral venography: comparison of CT and MR projection venography. AJR Am J Roentgenol 1997; 169:1699-707. [ Links ]
35. McLean BN. Dural sinus thrombosis. Br J Hosp Med 1991; 45:226-30. [ Links ]
36. Meder JF, Chiras J, Roland J. Venous territories of the brain. J Neuro radiolog 1994; 21:118-33. [ Links ]
37. Stephens PH, Lennox G, Hirsch N. Superior sagittal sinus thrombosis after internaljugular vein cannulation. Br J Anaesthe 1991; 67:476-9. [ Links ]
38. Cros D, Comp PC, Beltran G. Superior sagittal sinus thrombosis in a patient with protein S deficiency. Stroke 1990; 21:633-6. [ Links ]
39. Rosendaal FR. Venous thrombosis: a multicausal disease. Lancet 1993; 353: 1167-73. [ Links ]
40. Crawford SC, Digre KB, Palmer CA. Thrombosis of the deep venous drainage of the brain in adults: analysis of seven cases with review of the literature. Arch Neurol 1995; 52:1101-8. [ Links ]
41. Walther EU, Tiecks FP, Haber! RL. Cranial sinus thrombosis associated with essential thrombocythemia followed by heparin-associated thrombocytopenia. Neurology 1996; 47:300.
42. Hanley DF, Feldman E, Borel CO. Treatment of sagittal sinus thrombosis associated with cerebral hemorrhage and intracranial hypertension. Stroke 1988; 19:903-9.
43. Preter M, Tzourio C, Ameri A. Long-term prognosis in cerebral venous thrombosis: follow-up of 77 patients. Stroke 1996; 27:243-6.
1. Asistente Especialista en Medicina Crítica y Terapia Intensiva, Hospital Dr. Rafael A. Calderón Guardia.
2. Asistente Especialista en Neurología, Hospital Dr. Rafael A. Calderón Guardia.
Correspondencia: Kwok Ho Sánchez Suen. Unidad de Cuidados Intensivos, Hospital Rafael A. Calderón Guardia. Correo electrónico: kwokho@medicos.sa.cr














