Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista de Biología Tropical
On-line version ISSN 0034-7744Print version ISSN 0034-7744
Rev. biol. trop vol.49 n.3-4 San José Dec. 2001
asociado con Saccostrea palmula (Bivalvia: Ostreidae), Costa Rica
Jorge Cabrera Peña, Maurizio Protti Quesada, Mario Urriola Hernández, Osvaldo Sáenz Vargas y Rebeca Alfaro Hidalgo
Laboratorio de Recursos Naturales y Vida Silvestre, Escuela de Ciencias Biológicas, Universidad Nacional, Heredia 863000, Costa Rica. Fax: (506) 2376427, corel: jcabrer@samara.una.ac.cr o mprotti@samara.una.ac.cr.
Recibido 01-XI-2000. Corregido 30-111-200 1. Aceptado 06-IV-2001.
Abstract
Size and fecundity observations of pea crab (Juxtafabia muliniarum) from the paleal cavity of!he oyster Saccostrea palmula were made from May 1998 to May 1999. Infestation frequency was 18.52 % in a sample of 540 oysters. Of 136 pea crabs, 36 % were couples, 60 % were single females and 4 % were single males.The mean caparace length of J. muliniarum was 5.6 + 0.74 mm (range 4.0 to 7.6 mm) for females and 2.7 + 0.60 mm (range 1.6 to 4.0 mm) for males. The mean weight was 0.180 + 0.084 g (range 0.06 to 0.4g) for females and 0.011 + 0.003 g (range 0.01 to 0.02 g) for males. Ovigerous females (43.75 % of all females) were found in all months. The caparace length - fecundity relationship was F = 3904.6 Ln (Lc) -4651.1. The caparace length-weight relationship was P = 6 X 10-4 Lc3.2122. The mean sex-ratio was 1.0 male: 2.4 females. Saccostrea palmula infected only by females was the dominant group (60.78 %). This mollusk is a new host record for the crab.Key words: Juxtafabia muliniarum, feeundity, pea crab, size, Saccostrea palmula. sex ratio.
La familia Pinnotheridae está representada por un grupo diverso de pequeños cangrejos simbiontes de moluscos (almejas, ostras, mejillones, ostiones y otros bivalvos), poliquetos, equinodermos, holoturoideos y urocordados (Schmitt et al. 1973, Werding y Sánchez 1989. Stevens 1992, Soong 1997, Hamel et al. 1999).
Green (1995) sinonimizó a Pinnotheres jamesi con P. reticulatus. Posteriormente Campos (1993), nominó el género Juxtafabia para incluir en él a P. muliniarum Rathbun, 1918 y reconoció a P. jamesi y P. reticulatus como sinónimos de Juxtafabia muliniarum (Rathbun, 1918).
Juxtafabia muliniarum se caracteriza, en ambos sexos, por presentar el tercer maxilípedo con el carpo y propodo de igual tamaño; el extremo distal de propodo suboblongo es redondeado oblicuamente y con el dactilo amplio y lunado en posición próximoventral. En los machos el tercer somito abdominal es más ancho que el resto; el 4 y 5 somito están fusionadas y el telson es más largo que ancho; el tercer maxilípedo presenta palpas más cortos que el isquio-mero; el cuarto par de patas caminadoras es más corto que el resto y el cuarto dactilo es más corto y menos curvado que los otros. En las hembras los somitos abdominales son libres, más anchos y largos que el caparazón; el primer par de patas caminadoras es el más corto y, el dactilo 4 es más largo que los anteriores y que su propodo (Campos 1993)
Juxtafabia muliniarum se encuentra desde el Golfo de California a Costa Rica y ha sido registrada como simbionte en los bivalvos: Polymesoda inflata (Castaing et al. 1980, Green 1985). Chione pulicaria. C. fructifaga. C. califomiensis. C. tumens. Protothaca grata y Tagelus affines (Campos 1993, Campos et al. 1996).
En este trabajo se informa, por primera vez para el Pacífico de Costa Rica, las tallas, proporción de sexos, fecundidad y la relación longitud del caparazón con el peso total de J. muliniarum (Brachyura: Pinnotheridae) asociado a Saccostrea palmula (Bivalvia: Ostreidae).
Materiales y métodos
Se trabajó con 136 ejemplares de J. muliniarum, obtenidos de la cavidad paleal de 100 ejemplares de S. palmula, de un total de 540 ostras (n mensual entre 36 y 52 ostras) extraídas según el método bimuestreal de Stein (Azorín 1972) entre mayo 1998 y mayo de 1999, en el manglar del estero Morales, Puntarenas, Costa Rica (10° 4' N y 85° 58' O). Para la detección y extracción de los cangrejos en el hospedero se utilizó un estereomicroscopio 10x/40x. Los espécimenes fueron fijados en una solución de formaldehído al 5 % y clasificados según Campos (1993). A cada ejemplar se le midió: la longitud del caparazón (Lc) y ancho del caparazón (Ac) (+ 0.01 mm) y el peso total (Pt) (+ 0.05 g) (Rodríguez 1980). El sexo se determinó según Campos (1993). Los individuos fueron agrupados arbitrariamente en nueve clases de tallas: 1 (< 1.6 mm), 2 (1.7-2.4 mm), 3 (2.5-3.2 mm), 4 (3.3-4.0 mm), 5 (4.1-4.8 mm), 6 (4.9-5.6 mm), 7 (5.7-6.4 mm), 8 (6.5-7.2 mm) y 9 (7.3-8.0 mm), con el fin de determinar la relación talla-sexo.
A los datos se le aplicó un análisis de estadística descriptiva y se graficó la distribución de tallas y sexos. Se determinó mediante pruebas de correlación la relación longitud del caparazón-peso total (Pt = a Lc b) según Ricker (1975). La fecundidad (F) se determinó por el conteo directo de huevos de hembras ovígeras según Díaz et al. (1983). Se calculó la relación entre el número de huevos y la longitud del caparazón mediante la ecuación F = b Ln(Lc) - a (Díaz et al. 1983, Villalejo-Fuerte et al. 1998)
Los ejemplares tipos de esta investigación han sido depositados en Laboratorio de Recursos Naturales y Vida Silvestre, Escuela de Ciencias Biológicas, Universidad Nacional.
Resultados
De los 136 ejemplares de J. muliniarum, el 29.5 % fueron machos y 70.5 % hembras, para una proporción sexual de 1 macho: 2.4 hembras.
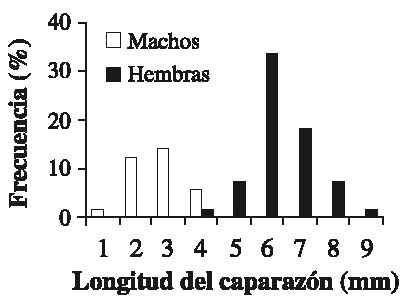
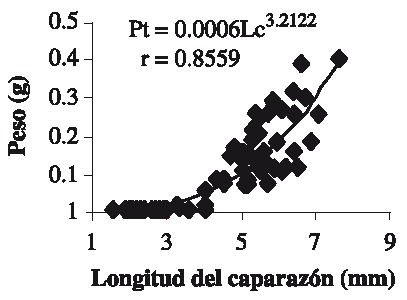
En promedio, las hembras presentaron valores más altos en todas las variables medidas con respecto a los machos (Cuadro 1). Las clases más frecuentes en machos y hembras fueron la 3 y 6 respectivamente (Fig. 1). La relación entre Lc-Pt se rigió por la ecuación Pt = 6 X 10-4 Lc3.2122 (r = 0.8559; p < 0.05) para la población total (Fig. 2).
Morales, Puntarenas, Costa Rica.
Table 1
estuary, Puntarenas, Costa Rica.
| Sexo | Variables | Promedio | S | Máximo | Mínimo | |
| Hembras (n = 96) | Lc | (mm) | 5.60 | 0.74 | 7.60 | 4.00 |
| Ac | (mm) | 6.87 | 0.90 | 9.40 | 4.90 | |
| Pt | (g) | 0.18 | 0.08 | 0.40 | 0.06 | |
| Machos (n = 40) | Lc | (mm) | 2.71 | 0.60 | 4.00 | 1.60 |
| Ac | (mm) | 3.18 | 0.79 | 5.10 | 2.00 | |
| Pt | (g) | 0.01 | 0.003 | 0.02 | 0.01 | |
Fig. 1. Distribución por tallas y sexos de una población de J. muliniarum (n = 136) asociada a S. palmula.
Fig. 1. Size and sex distribution in a population of J. muliniarum (n = 136) associated to S. palmula.
Fig. 2. Caparace length-weight relationship in a population of J. muliniarum associated to S. palmula.
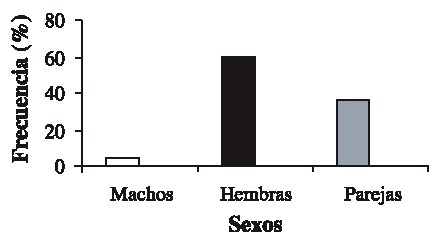
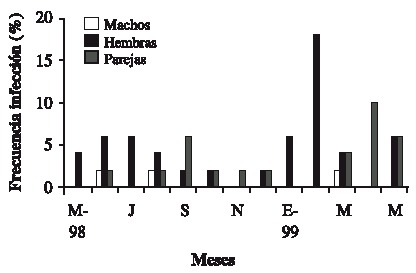
Del total de cangrejos recolectados, las hembras solas, fueron las que presentaron el mayor porcentaje de incidencia sobre S. palmula (60 %), mientras que los machos solos aparecieron en 4 % durante el periodo de estudio (Fig. 3). Las hembras solas fueron las más frecuentes en cuanto a infestación mensual, alcanzando su máxima expresión en febrero de 1999 (18 %), mientras que los machos solamente aparecieron en junio (2 %) y agosto (2 %) de 1998 (Fig. 4).
Fig. 3. Frecuencia de infección de una población de S. palmula por J. muliniarum.
Fig. 3. Frequency of infestation in a population of S. palmula by J. muliniarum.
Fig. 4. Monthly frequency of males, females and couples of J. muliniarum associated to S. palmula.
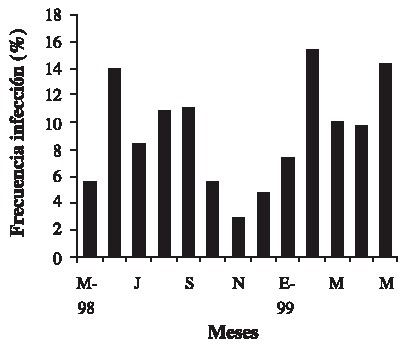
Se detectaron dos máximos de infestación mensual del cangrejo sobre las ostras, uno en febrero (18 %) y el otro en mayo de 1999 (12 %) (Fig. 5).
Fig. 5. Frecuencia de infección mensual de S. palmula (n = 100) por J. muliniarum.
Fig. 5. Frequency of monthly infestation in S. palmula (n = 100) by J. muliniarum.
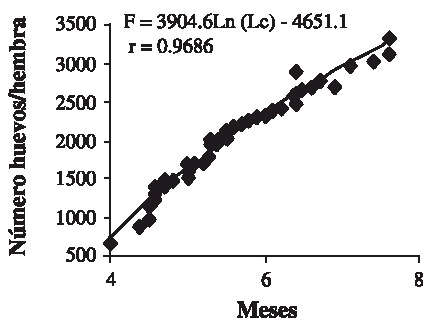
Durante todos los meses de muestreo se presentaron hembras ovígeras con huevos en diferentes etapas de desarrollo, representando el 43.75 % del total de hembras, siendo febrero de 1999 el de mayor incidencia. El promedio de huevos por hembra para el periodo de estudio fue de 2032.36 + 569.23 y la relación Lc-F se rigió por la ecuación F = 3904.6 Ln (Lc) 4651.1 (r = 0.9686; p < 0,05) (Fig. 6).
Fig. 6. Relación longitud caparazón-fecundidad en una población de J. muliniarum (n = 42) asociada a S. palmula.
Fig. 6. Caparace length-fecundity relationship in a population of J. muliniarum (n = 42) associated to S. palmula.
Discusión
Las hembras presentaron, en promedio, una longitud de caparazón aproximadamente el doble de los machos, lo cual coincide con lo informado por McDermott (1981) y Bell y Stancyck (1983) para la mayoría de los pinnotéridos simbiontes de moluscos, equinodermos y otros invertebrados marinos. La Lc de J. muliniarum, en ambos sexos, se encuentra entre los ámbitos mínimos y máximos de especies del género Pinnotheres. El valor máximo encontrado en este estudio fue inferior al informado por Wicksten (1982) para P. margarita (12.3 mm). El ancho de caparazón promedio de J. muliniarum, del estero Morales, se encontró dentro de los ámbitos informados por Wicksten (1982) (3.3-14.1 mm en P. margarita) y por Pohle y Marques (1988) para varias especies de Pinnotheres; sin embargo P. novaezelandiae y P. pilumnoides alcanzan tallas superiores a las registradas en este estudio (15.2 y 14.0 mm respectivamente).Los resultados de esta investigación sugieren que los machos de J. muliniarum infectan a S. palmula a un ancho de caparazón (2.0 mm) menor que la informada para algunas especies de Pinnotheres, tales como: P. novaezelandiae (9.8 mm) P. pilumnoides (14.0 mm) P. angelicus (5.9 mm), P. modiolicola (6.3 mm), P pisum (6.3 mm) y P. taylori (2.6 mm), así como otras especies de la familia Pinnotheridae como: Fabia concharum (12.1 mm), F. subcuadrata (5.5 mm), Pinnaxodes chilensis (17.7 mm) (Pohle y Marques 1988), lo cual puede ser atribuido a la condición amensal de los cangrejos pinnotéridos con el hospedero; ya que según Haines et al. (1994) los machos pueden vivir fuera del bivalvo, mientras que las hembras establecen una relación más dependiente con el hospedero luego de su definitivo establecimiento. Por otra parte, este hecho puede ser explicado por la dominancia intraespecífica agresiva de las hembras sobre los machos, lo cual induce una permanencia estacional de estos, tal como señaló Hipeau-Jacquotte (1974b) para los camarones de la subfamilia Pontoniinae. Esta hipótesis se refuerza por la mayor incidencia de hembras solas (60 %) durante el periodo de estudio.
Las hembras de J. muliniarum alcanzaron pesos y tallas promedio superiores a los machos coincidiendo con Haines et al. (1994). A nivel poblacional, la curva de crecimiento Lc- Pt establece una relación alométrica positiva, tal como sucede en la mayoría de los crustáceos decápodos, particularmente en los cangrejos braquiuros (Gould 1971, Hartnoll1977).
La proporción sexual es muy variable dentro y entre las especies de la familia Pinnotheridae (Dos Santos y Pezzuto 1997). En el presente trabajo la relación sexual fue de 1 macho: 2.4 hembras, mientras que la mayoría de los trabajos realizados para otras especies de pinnotéridos asociados a moluscos bivalvos (Pearce 1964, 1966), a galerías de camarones excavadores (Dos Santos y Pezzuto 1997) y equinodermos (Bell y Stancyck 1983) indican relaciones sexuales de 1: 1. Coincide con lo informado para pinnotéridos hospederos en tubos de poliquetos (McDermott 1981), donde dominan las hembras. Además, esta relación es contraria a la registrada por Ambariyanto y Seed (1991) para P. pisum (1.4: 1) y por Kruczynski (1973) para P. maculatus (1.6: 1), ambos hospederos en Mytilus edulis, donde los machos fueron los dominantes.
La presencia de pinnotéridos en moluscos bivalvos es muy variable temporalmente (Dos Santos y Pezzuto 1997), situación que coincidió con J. muliniarum asociado a S. palmula, donde el porcentaje de infestación fue variable mensualmente y las mayores variaciones obtenidas pueden ser atribuidas a fluctuaciones ambientales locales producto de las influencia de corrientes, salinidad, temperatura del agua, exposición de las ostras a la infestación y competencia eventual entre el número de organismos infestantes y el número de hospederos en lugarar, coincidiendo con lo señalado por Hipeau-Jacquotte (1974a).
Durante todos los meses de muestreo se presentaron hembras ovígeras con huevos en distintas etapas de desarrollo, lo que demuestra la adaptabilidad de J. muliniarum al estilo de vida asociada (Hipeau-Jacquotte 1973). Esta situación, acompañada de los diferentes estados de mudas en que se encontraron las hembras, sugiere periodos continuos de reprodución para esta especie, tal como lo informó Dowds (1978) para varias especies de Pinnixa en un estuario de Carolina del Norte, USA.
EI ámbito del número de huevos encontraJen J muliniarum (entre 680 a 3 300 huevos/hembra) es superior a los valores informados por Dos Santos y Pezzuto (1997) para Pinixa patagoniensis (830-2 472) y se encuentra
dentro de los ámbitos informados para el género Pinnotheres y Pinnixa, sin llegar a alcanzar los máximos de 8 000 y 9 546 huevos por hembra informados por Pearce (1966), Christensen y McDermott (1958) respectivamente.
La ecuación para la relación Lc-F, permite explicar en forma satisfactoria (r = 0.9686) el incremento en el número de huevos en función del crecimiento de las hembras.
Resumen
Se determinaron las tallas, frecuencia de infección y fecundidad de Juxtafabia muliniarum de la cavidad paleal de Saccostrea palmula de mayo de 1998 a mayo de 1999, la frecuencia de infestación fue de un 18.52 % en una muestra de 540 ostras. De los 136 cangrejos, el 36 % fueron parejas, el 60 % hembras solas y el 4 % machos solos. El promedio de la longitud del caparazón fue de 5.6 + 0.74 mm (ámbito entre 4.0 y 7.6 mm) para hembras y 2.71 + 0.60 mm (ámbito entre 1.6 y 4.0 mm) para machos. El peso promedio fue de 0.180 + 0.084 g (ámbito entre 0.06 y 0.4 g) para hembras y 0.011 + 0.003 g (ámbito entre 0.01 y 0.02 g) para machos. La fecundidad de J. muliniarum se rigió por la ecuación F = 3904.6 Ln (Lc) -4651.1. En todos los meses se encontraron hembras ovígeras. La relación longitud del caparazón-peso total para machos y hembras se rigió porla ecuación Pt = 6 X 10-4 Lc3.2122. La proporción sexual fue de 1.0 macho: 2.04 hembras. Se registra a S. palmula como huésped de J. muliniarum
Agradecimientos
Se agradece a Tatiana Láscaris, Universidad Nacional por el apoyo brindado para realizar este trabajo en la Estación de Ciencias Marinas de Punta Morales (ECMAR), así como a los revisores anónimos por las correcciones y sugerencias al manuscrito.
Referencias
Ambariyanto, H. & R. Seed. 1991. The infestation of Mytilus edulis Linnaeus by Polydora ciliata (Johnston) in the Conwy Estuary, North Wales. J. Moll. Stud. 57: 413-424. [ Links ]
Azorín, P.F. 1972. Curso de muestreo y aplicaciones. Aguilar, D.F. México. 375 p. [ Links ]
Bell, J.L & S.E. Stancyck 1983. Population dynamic and reproduction of Dissodactylus mellitae (Brachyura: Pinnotheridae) on its sand dollar host Mellita quinquiesperforata (Echinodermata). Mar. Ecol. Prog. Ser. 13: 141-149. [ Links ]
Campos, E. 1993. Systematic and taxonomic remarks on Pinnotheres muliniarum Rathbun,1918 (Crustacea: Brachyura: Pinnotheridae). Proc. Biol. Soc. Wash. 106: 92-101. [ Links ]Campos, E., R. Mejía-Cruz & A.R. Campos. 1996. Bivalvos (Molusca) y sus crustáceos simbiontes en el alto Golfo de California. VII Congreso Asoc. Invest. Del Mar de Cortés, A. C., México. LR-2. [ Links ]
Castaing, A., J.M. Jiménez & C.R. Villalobos. 1980. Observaciones sobre la ecología de manglares de la costa Pacífica de Costa Rica y su relación con la distribución del molusco Geloina inflata (Phillippi) (Pelecypoda: Corbiculidae). Rev. Biol. Trop. 28: 323- 339. [ Links ]
Christensen, A.M. & J.J. McDermott. 1958. Lifehistory and biology of the oyster crab, Pinnotheres ostreum Say. Biol. Bull. Mar. Biol. Lab., Woods Hole 114: 146-179. [ Links ]Díaz, H.J., E. Conde & M. Bevilacqua. 1983. Avolumetric method for estimating fecundity in decapoda. Mar. Ecol. Progr. Ser. 10: 203-206. [ Links ]
Dos Santos, A.E. & P.R. Pezzuto. 1997. Population dynamics of Pinnixa patagoniensis Rathbun, 1918(Brachyura: Pinnotheridae) a symbiotic crab of Sergio mirim (Thalassinidea: Callianassidae) in Cassino Beach, Southern Brazil. Mar. Ecol. 19: 37-51. [ Links ]
Dowds, R.E. 1978. Distribution and reproduction of four species of Pinnixa (Crustacea: Brachyura) in a NorthCarolina Estuary. Amer. Zool. 18: 599. [ Links ]
Green, T.M. 1985. Pinnotheres jamesi synonymized with J. muliniarum (Decapoda: Brachyura). Proc. Biol. Soc. Wash. 98: 611-614. [ Links ]
Gould, S.J. 1971. Geometric similarity in allometric growth: Contribution to the problem of scalinh in the evolution of size. Am. Natur. 105: 113-136. [ Links ]
Haines, C. M. C., M. Edmunds & A.R. Pewsey. 1994. The pea crab, Pinnotheres pissum (Linnaeus, 1767), and its association with the common mussel Mytilus edulis (Linnaeus, 1758), in the Solent (UK). J. Shellfish Res. 13: 5-10. [ Links ]Hamel, J.F., K.L. Peter & A. Mercier. 1999. Life cycle of the pea crab Pinnotheres halingi sp. nov., an obligate symbiont of the sea cucumber Holothuria scabra Jaeger. Ophelia 50: 149-175. [ Links ]
Harnoll, R.G. 1977. The determination of relative growth in crustacea. Crustaceana 34: 281-293 [ Links ]
Hipeau-Jacquotte, R. 1973. Manifestation dun comportment territorial chez crevettes Pontoniinae (Palaemonidae) associées aux mollusques Pinnidae a Tuléar (Madagascar). J. Exp. Mar. Biol. Ecol. 13: 63-71. [ Links ]
Hipeau-Jacquotte, R. 1974a. Etude des crevettes Pontoniinae (Palaemonidae) associées aux mollusques Pinnidae a Tuléar (Madagascar). 5. Linfestation dans les conditions naturelles. Téthys. Suppl. 5: 383-402. [ Links ]
Hipeau-Jacquotte, R. 1974b. Etude des crevettes Pontoniinae (Palaemonidae) associées aux mollusques Pinnidae a Tuléar (Madagascar). 6. Comportement sexuel. Téthys. Suppl. 5: 403-408. [ Links ]
Kruczynski, W.L. 1973. Distribution and abundance of Pinnotheres maculatus Say in Bogue Sound, North Carolina. Biol. Bull. Mar. Biol. Lab. Woods Hole 145: 482-491. [ Links ]McDermott, J.J. 1981. Biology of the symbiotic crab Pinnixa cylindrica (Say) (Decapoda: Pinnotheridae). Proc. Pennsylvania Acad. Sci. 55: 23-27. [ Links ]
Pearce, J.B. 1964. On reproduction in Pinnotheres maculatus (Decapoda: Pinnotheridae). Biol. Bull. Mar. Biol. Lab. Woods Hole 127: 384. [ Links ]
Pearce, J.B. 1966. On Pinnixa faba and Pinnixa littoralis (Decapoda: Pinnotheridae) symbiotic with the clam Tresus capax (Pelecypoda: Mactridae), p. 565-589. In H. Barnes (ed.). Some contemporary studies in marine science. Allen Unwin, Londres. [ Links ]
Pohle, G & F. Marques. 1998. Phylogeny of the Pinnotheridae: Larval and adult evidence, with emphasis on the evolution of gills. Invert. Reprod. Develop. 33: 229-239. [ Links ]Ricker, W.E. 1975. Computation and interpretation of biological statistic of fish population. Bull. Fish. Res.Bd., Canada. 382 p. [ Links ]
Rodríguez, G. 1980. Los Crustáceos decápodos de Venezuela. Instituto Venezolano de Investigaciones Científicas, Caracas. Venezuela. 444 p. [ Links ]
Schmitt, W.L., J.C. McCain & E.S. Davidson. 1973. Decapoda I. Brachyura I. Family Pinnotheridae, Vol. 3: 1-160. In H.E. Gruner & L.B. Holthuis (eds.). Crustaceorum Catalogus. W. Junk, La Haya, Holanda. [ Links ]Soong, K. 1997. Some lifehistory observations on the pea crab, Pinnotheres tsingtaoensis, symbiotic with the bivalve mollusk, Sanguinolaria acuta. Crustaceana 70: 855-866. [ Links ]
Stevens, P. 1992. New host record for pea crabs (Pinnotheres ssp) symbiotic with bivalve mollusks in New Zealand (Decapoda: Brachyura). Crustaceana 63: 216-220 [ Links ]
Villalejo-Fuerte, M., M. Arellano-Martínez & B.P. Ceballos-Vázquez. 1998. Fecundity of the panamic spidercrab Maiopsis panamensis Faxon, 1893 (Brachyura: Majidae) in the Gulf of California, Mexico. J. Shellfish Res. 17: 299-301. [ Links ]
Wicksten, M.K. 1982. New records of pinnotherid crabs from the gulf of California (Brachyura: Pinnotheridae). Proc. Biol. Soc. Wash. 95: 354-357. [ Links ]
Werding, B. & H. Sánchez.1989. Pinnotherid crabs of the genus Dissodactylus Smith, 1870, associated with irregular sea urchins at the Caribbean of Colombia (Crustacea: Decapoda: Pinnotheres) Zool. Medel. 63: 35-42. [ Links ]