Revista Costarricense de Cardiología
ISSN 1409-4142
Infarto Agudo de Miocardio: Certezas e Incertidumbres con las Nuevas Estrategias de Reperfusión
Dr. Ricardo Mario Iglesiasa, Dr. Adrian Lescanob
a. Fellow American College of Cardiology, Director de Docencia e Investigación del Departamento Cardiovascular, Sanatorio de la Trinidad, Virrey del Pino 2458. 4º piso. Belgrano, Buenos Aires Buenos Aires, Argentina. Fax 011-4788-2566; e-mail: ricardoiglesias@fibertel.com.ar
b. Coordinador Docente, Sociedad Argentina de Cardiología, médico asistente del Servicio de Cardiología. Sanatorio de la Trinidad, Palermo, Buenos Aires, Argentina.
Abreviaturas: IAM: infarto agudo de miocardio. ACV: accidente cerebrovascular. LDL: lipoproteína de baja densidad. ACT:
Resumen
Las enfermedades cardiovasculares representan la primera causa de morbimortalidad a nivel mundial.
El infarto agudo de miocardio es la expresión más dramática dentro del síndrome coronario agudo y el accidente de placa coronario, el mecanismo fisiopatológico involucrado con mayor frecuencia.
El objetivo del tratamiento ha variado en los últimos años, desde obtener permeabilidad en las arterias epicárdicas hasta alcanzar un decuado nivel e perfusión n el ircuito microvascular.
La optimización de la estrategia terapéutica se obtiene a través de una reperfusión precoz y efectiva (fibrinolíticos y/o angioplastia) y la selección adecuada de múltiples fármacos coadyuvantes (B bloqueantes, aspirina, clopidogrel, anticoagulantes) que han demostrado beneficios clínicos en diversos ensayos clínicos.
Palabras clave: Infarto agudo del miocardio, reperfusión, fibrinolíticos, angioplastía.
Abstract
The first cause of morbidity-mortality all over the world is represented by the cardiovascular diseases.
The acute infarct of myocardium is the most dramatic expression within the acute coronary syndrome and the coronary plaque rupture, the most frequently physiopathology mechanism involved. In the last few years the objective of the treatment has changed, from obtaining permeability in the epicardial arteries to reaching a suitable level of perfusion in the microvascular circuit.
The optimization of the therapeutic strategy obtains through a precocious and effective reperfusion (fibrinolytic and/or angioplasty) and the suitable helping drug selection (aspirin, clopidogrel and anticoagulants) that has demonstrated clinical benefits in clinical trials
Keywords: Acute myocardial infartion, reperfusion, fibrinolitics, angioplasty.
Introducción
Las enfermedades cardiovasculares constituyen la primera causa de mortalidad en pacientes adultos en la mayoría de los países desarrollados, incluido nuestro país, donde ocasiona más de 90.000 muertes por año. Los síndromes coronarios agudos conforman un conjunto de entidades clínicas de alta prevalencia en la población (35% de las internaciones en Unidad Coronaria). Agrupan diferentes cuadros clínicos que tienen en común el dolor precordial de reposo o a mínimos esfuerzos, que aparece en un tiempo reciente o que se agrava en un corto lapso (< a 3 meses). El mecanismo fisiopatológico involucrado es el accidente de placa, que comprende una cascada de reacciones fisiopatológicas que interactúan entre si y cuyo producto final es el trombo. Las manifestaciones clínicas de la ruptura de la placa de ateroma y la trombosis pueden variar de acuerdo a la magnitud de esta, la localización y la falla en el sistema de fibrinolisis endógena. Un trombo relativamente estable y oclusivo tiende a causar un infarto agudo del miocardio (IAM) tipo Q, mientras que uno suboclusivo tiene mas posibilidades de provocar un cuadro de angina inestable o IAM no Q.
El electrocardiograma (ECG) es la herramienta que guía la conducta inicial en los cuadros isquémicos agudos. Las decisiones terapéuticas al ingreso en la unidad coronaria,son seleccionadas de acuerdo a los cambios de la repolarización eléctrica ventricular.Los pacientes con elevación persistente del segmento ST o bloqueo de rama izquierda son considerados infartos transmurales o tipo Q y se deben tratar con estrategias de reperfusión, fibrinolíticos o angioplastia.
Los pacientes sin elevación del segmento ST, se consideran infarto tipo no Q si presentan elevación enzimática o angina inestable si los marcadores de necrosis miocárdica son negativos. En estas circunstancias clínicas se requiere implementar una conducta terapéutica escalonada. Es importante remarcar, que en la evolución, la mayoría de los infartos con onda Q provienen del grupo con elevación del segmento ST, sin embargo el 20 % de los infartos con elevación del ST no desarrollan ondas Q. A su vez, el 10 % de los infartos con depresión del segmento ST desarrollan ondas Q en su evolución.
Por tales motivos, es inadecuado denominar infartos Q o no Q a los cuadros de ingreso y es aconsejable actuar de acuerdo con la repolarización ventricular y esperar la evolución para la clasificación definitiva. La manifestación más dramática del síndrome coronario agudo es el IAM, al que sobreviven al cabo de un año, sólo la mitad de los pacientes, muchos de los cuales no se recuperan en forma óptima. El IAM es una entidad de alta prevalencia en el mundo occidental, incluido nuestro país. Informes sanitarios estiman una cifra de 30.000 a 35.000 eventos en la República Argentina. La mortalidad prehospitalaria es alrededor del 30 %, la intrahospitalaria del 12 % y la extrahospitalaria de un 5 % anual. Los últimos 20 años fueron trascendentes para el conocimiento de la patogenia del infarto, los grandes ensayos clínicos contribuyeron de manera significativa a ampliar nuestros conocimientos, aportaron certezas para desarrollar estrategias de diagnóstico y tratamiento. Sin embargo, observamos que frecuentemente el médico se enfrenta a un número elevado de opciones que le generan incertidumbres en el óptimo manejo de los pacientes con infarto. Por esta razón es nuestro propósito sintetizar la información científica disponible de los estudios controlados y trasladarla con mesura y análisis crítico al paso individual.
¿Por qué se produce un síndrome coronario agudo?
La disfunción endotelial es la manifestación inicial de la ateroesclerosis1. Múltiples noxas alteran las propiedades normales anticoagulantes y vasodilatadoras del endotelio, entre otras las partículas de LDL oxidada, la glicosilación proteica y los probables factores infecciosos. La alteración en la permeabilidad vascular genera variaciones en los mecanismos homeostáticos con la llegada de células inflamatorias, musculares y el acúmulo de lípidos, conformando la placa de ateroma, con la consiguiente muerte celular secundaria, apoptosis y transformación celular. Esta placa con importante componente inflamatorio en su interior y una delgada capa fibrosa, desarrolla el escenario propicio para el accidente de placa. La ruptura intimal expone el tejido conectivo a las células sanguíneas, con la consecuente trombosis sobreagregada. Estos hallazgos no se limitan sólo a la arteria culpable del evento, sino que también se objetivan placas complejas e imágenes trombóticas en otras arterias coronarias. Este proceso de "pancoronaritis" expresa la manifestación global o sistémica de la enfermedad. En la actualidad, se reconoce que un porcentaje de las lesiones coronarias están en riesgo de accidentarse e indican la vulnerabilidad de los pacientes.
El sistema inflamatorio juega un papel fundamental en la génesis e inestabilidad de la enfermedad coronaria. La presencia de células inflamatorias activadas en la anatomía patológica de las aterectomías, el incremento de la temperatura local en las placas, el aumento de la agregación leucocito-plaquetaria y la elevación de los marcadores serológicos son manifestaciones objetivas de este fenómeno. Estas alteraciones sistémicas persisten varios meses, posteriores al cuadro inestable y expresan la evolución de la enfermedad más allá del proceso agudo.
En resumen, los estadios fisiopatológicos que intervienen en el síndrome coronario agudo varían entre una fase inicial, donde predominan las complicaciones resultantes del accidente de placa (trombo coronario) y una fase evolutiva donde cobra relevancia la persistencia de la placa residual, con la probabilidad de nuevas rupturas. El 75 % de los accidentes de placa se desarrollan sobre placas no críticas (obstrucciones < al 70% )
¿La ruptua de la placa ocurre de manera casual?
Datos epidemiológicos y observacionales demuestran que al menos un 30 a 50 % de los infartos están asociados con factores psicosociales o actividades condicionantes de la ruptura de estas placas vulnerables (cuadro 1). El aumento en la actividad simpática, con el consiguiente incremento de la frecuencia cardíaca, la presión arterial, la contractilidad y un aumento del tono coronario puede considerarse como posible causante de la ruptura. Además, puede estar relacionada con un estado protrombótico, generado por la hiperreactividad plaquetaria, el aumento de la viscosidad sanguínea, el aumento de los valores de cortisol y las fluctuaciones de los factores fibrinolíticos, entre otros. Es evidente que en la génesis de un infarto se deben asociar dos situaciones, una placa blanda, pequeña con posibilidades de ruptura (placa vulnerable) y un paciente con condiciones biológicas y/o emocionales inestables (paciente vulnerable).

Diagnóstico
La mayoría de las enfermedades cardiovasculares se diagnostican con simples y económicos recursos. El interrogatorio adecuado y profundo de los síntomas, el examen físico, el ECG y la radiografía de tórax son herramientas que permiten en casi un 80 % el diagnóstico de la enfermedad. El diagnóstico de IAM se sustenta con 2 de los 3 criterios (dolor, ECG y enzimas). Esta definición clásica de IAM no es práctica para decidir el tratamiento de reperfusión, porque la confirmación del infarto, en especial por los marcadores bioquímicos, supone una demora inaceptable para la eficacia terapéutica. Es así como desde los estudios pioneros con fibrinolíticos se introdujo el concepto de sospecha de IAM. Se ha demostrado que la sospecha de IAM (dolor prolongado y supradesnivel del segmento ST) se confirma el mismo en más del 90 % de los casos. Se define sospecha de IAM a la presencia de síntomas (angor o equivalentes) persistentes (más de 20 minutos) que no ceden con nitritos, asociados con supradesnivel del segmento ST o bloqueo de rama izquierda nuevo o presumiblemente nuevo, ritmo de marcapaso u otro confundidor que no permita el análisis del segmento ST dentro de las 12 horas del comienzo de los síntomas.
Estratificación de riesgo
La evaluación temprana del riesgo es indispensable para identificar la posibilidad de muerte o complicaciones de cada paciente en particular. Esta estratificación tiene una repercusión directa en la utilización de los recursos. Simples datos de observación a la cabecera del paciente nos permiten realizar la estratificación de riesgo. Los datos clínicos extraídos del estudio Fibrinolytic Therapy Trialist (FTT)2, en más de 60 000 sujetos, en los cuales se comparó la terapéutica trombolítica con grupos control o placebo, fueron una herramienta indispensable para la evaluación del paciente individual (cuadros 2 y 3).
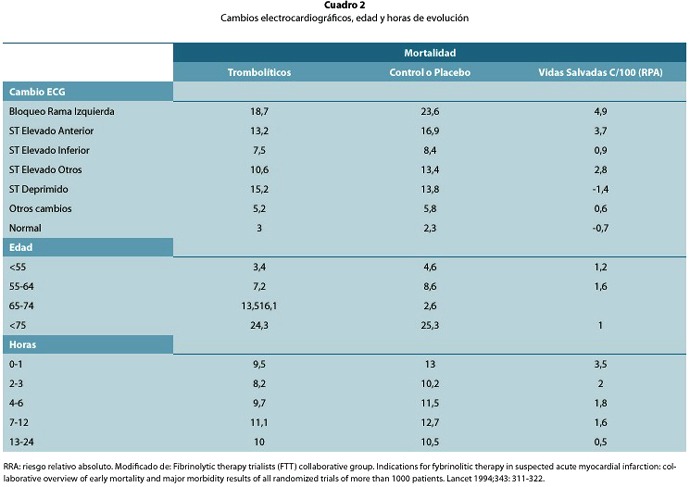
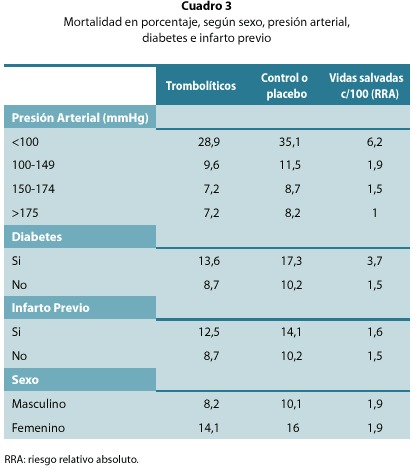
Estratedias de reperfusión
La fisura de la placa de ateroma y la consecuente formación del trombo son la base fisiopatológica fundamental para la formación del infarto agudo de miocardio. Cuando esto ocurre, el vaso se obstruye, se interrumpe el flujo coronario y los requerimientos de oxígeno celular no pueden ser satisfechos. Este es el inicio del proceso de isquemia miocárdica; si estas condiciones persisten por un tiempo prolongado, las células mueren y clínicamente se produce un infarto de miocardio. El objetivo primordial del tratamiento del IAM es la recanalización temprana y mantenimiento en el tiempo de la apertura de la arteria responsable, así como preservar la función microvascular y celular. La reperfusión exitosa salva miocardio, reduce el área de infarto, mejora la función ventricular y subsecuentemente mejora la sobrevida. Este beneficio es tiempo-dependiente dentro de las primeras 3 horas de comenzados los síntomas y menor en la ventana de 3 a 12 horas. En el período de 12 a 24 horas es menos pronunciado, aunque parece ser efectivo en pacientes que persisten con signos o síntomas de isquemia. El accidente de placa es una cascada de reacciones fisiopatológicas que interactúan entre si y cuyo producto final es el trombo. La activación sistémica de la coagulación (generación de trombina) y la mayor reactividad plaquetaria (adhesión y agregación) son los mecanismos involucrados y es allí donde debemos actuar.
Agentes trombolíticos
El tratamiento de reperfusión ha cambiado la historia natural y el pronóstico de nuestros pacientes. Los fibrinolíticos, son el de reperfusión más habitual utilizado en el mundo (43% en el registro GRACE3). Los agentes fibrinolíticos son activadores directos o indirectos del plasminógeno, que se transforma en plasmina, capaz de degradar la fibrina, el fibrinógeno, la protrombina y los factores de coagulación V y VII. La droga estándar en nuestro país es la estreptokinasa, se la utiliza en dosis fija de 1.500.000 U IV infundida en una hora. Existen otras drogas que varían en sus características, estructura, vida media y fibrinoespecificidad (duteplase, anistreplase, reteplase, alteplase y tecneteplase). Los altos costos de estos agentes y el escaso beneficio comparado con la estreptokinasa, los convierten en una alternativa de baja utilización. Independientemente del agente utilizado, cualquiera que fuere, reducen la mortalidad en un 20%. Las contraindicaciones absolutas para su utilización son poco frecuentes (cuadro 4).
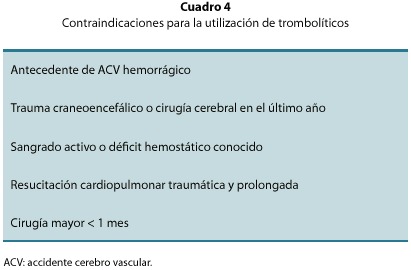
Angiplastia coronaria primaria
Durante la década del 90 varios ensayos comunicaron los beneficios del tratamiento invasivo en la resolución mecánica de la oclusión trombótica generadora del IAM. La angioplastia coronaria primaria ha demostrado índices más elevados de reperfusión que los alcanzados con el tratamiento trombolítico. Los estudios aleatorizados mostraron una restitución del flujo coronario grado en alrededor del 88 % al 95 % de los casos. Su limitación es que se debe realizar en centros especializados, con una infraestructura adecuada y un personal altamente entrenado las 24 horas del día.
Fibrinolíticos versus angiplastia coronaria primaria
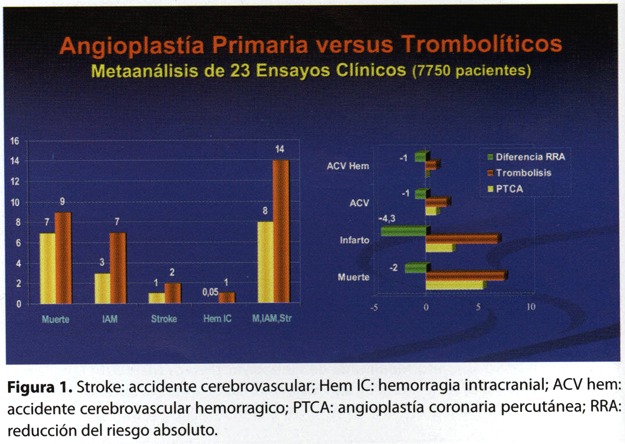
El metaánalisis de los estudios comparativos tegias confirma el beneficio brindado por la angioplastia, con una reducción del riesgo absoluto del 2 % en la mortalidad (7 versus 9%), 4% en el reinfarto (3 versus 7%), 1 % en el accidente cerebrovascular (1 versus 2%, figura 1). Estos resultados son el producto del trabajo de investigadores o centros de vasta experiencia en el manejo del IAM. Es probable que estos beneficios de la angioplastía primaria no se puedan generalizar, el éxito del procedimiento es dependiente del operador y del volumen de procedimientos del centro. La mortalidad al mes es de 8,7 % en centros con un número escaso de procedimientos por año (<15) y del 3,6 % en los centros con más de 30 al año. El Registro Norteamericano de IAM4 comprobó que no hay diferencias en la mortalidad entre el tratamiento trombolítico (5.9%) y la angioplastía primaria (6,2%) en centros con pocas intervenciones (figura 2). Cada institución deberá implementar la estrategia más conveniente en el tratamiento del IAM, dependiendo de las condiciones técnicas y humanas con las que dispone.
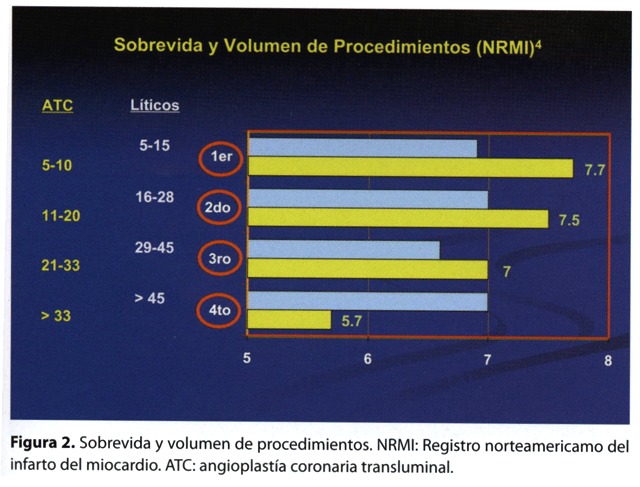
Identificar a los pacientes para cada estrategia de reperfusión
La terapia trombolítica es una estrategia sencilla, de aplicación masiva y al alcance de todos los centros de nuestro país. Sin embargo,existen condiciones clínicas que le hacen perder eficacia. El tiempo de demora en su aplicación es una de ellas, el mayor impacto sobre la mortalidad se observa en las 3 primeras horas de comenzado los síntomas (65 vidas salvadas /1000 pacientes tratados en la primera hora contra 10 vidas salvadas/1000 tratados entre las 6 y 12 horas, figura 3). Otra condición es, en pacientes añosos o en aquellos con falla de bomba, los resultados de la angioplastía primaria son superiores.
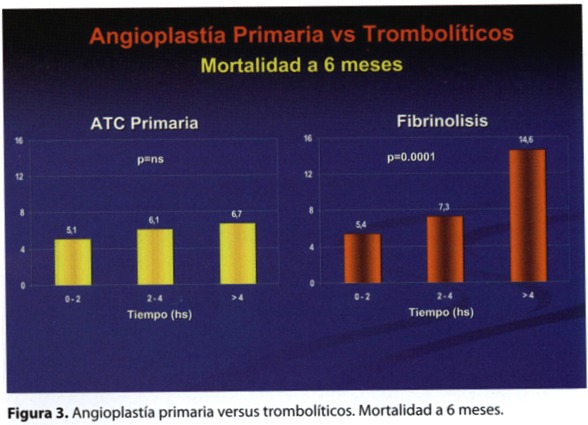
En general, en pacientes de bajo riesgo debe utilizarse fibrinolíticos ante la sospecha de IAM de menos de 12 horas de evolución, sin contraindicaciones, menores de 75 años, sin edema agudo de pulmón o shock cardiogénico. En pacientes de alto riesgo debe realizarse angioplastía primaria dentro de las 24 horas de un IAM complicado con insuficiencia cardíaca o shock cardiogénico.
Traslado de pacientes a centros con disponibilidad de ATC primaria
Los estudios PRAGUE-25, DANAMI-26 y el CAPTIM7 fueron realizados con el objetivo de responder a la pregunta ¿El traslado del paciente a un centro de alta complejidad para la realización de una angioplastía primaria puede tener ventajas con respecto a la infusión de trombolíticos in situ?
En ningún caso se pudo demostrar reducción de la mortalidad con el traslado, sí se detectó una disminución del reinfarto y del accidente cerebrovascular. Se acepta que a partir de los 90 minutos de retraso en el tiempo de derivación las diferencias a favor de la estrategia intervencionista tienden a desaparecer. El beneficio de la derivación se concentra en los IAM con más de 3 horas de evolución. Lo que demostraron claramente los ensayos es que el traslado de un paciente con infarto es factible y no se asocia con riesgos significativos. Las recomendaciones para derivar a un paciente a un centro de alta complejidad son los pacientes con amenaza de IAM extenso o con signos de insuficiencia cardiaca de menos de 12 horas de evolución, siempre y cuando el tiempo de llegada al laboratorio de hemodinamia se alcance en menos de 90 minutos. En caso de no garantizarse un traslado rápido se debe iniciar la infusión del agente trombolítico.
Debilidades del tratamiento fibrinolítico
La desventaja más notoria del tratamiento trombolítico cuando se compara con la estrategia invasiva depende fundamentalmente de la inferioridad en términos de porcentaje de reperfusión.
Aproximadamente un 45 % de los pacientes no reperfunden satisfactoriamente, incrementando al doble la mortalidad. Otro inconveniente, de gran trascendencia clínica, es el reinfarto y la recurrencia de eventos isquémicos, secundarios a la reoclusión trombótica. La administración de agentes fibrinolíticos se asocia con un estado hipercoagulable posterior, debido básicamente a la activación de la trombina. Este fenómeno se observa en la primera semana entre un 5 y 15 %, incrementando tres veces la mortalidad. El estudio GUSTO I, el cual comparó distintos agentes trombolíticos en más de 40 000 pacientes8, comprobó la importancia de la recanalización y mantenimiento en el tiempo de la apertura de la arteria responsable. La mortalidad a 30 días de los pacientes que nunca abrieron la arteria fue del 17,2%, en aquellos que inicialmente la abrieron pero al día 7 se encontraba ocluida, la mortalidad fue del 12,8%, en cambio la mortalidad de quienes se abrió precozmente y se mantuvo con buen flujo en el seguimiento fue tan solo del 4 %. El desafío de la investigación en los últimos años se concentró en el desarrollo de mejores estrategias, que aumenten la reperfusión y/o prevengan la reoclusión, sin generar incremento en el sangrado. Las drogas estudiadas en estos ensayos clínicos fueron nuevos trombolíticos o agentes que optimicen la terapéutica trombolítica clásica. Describiremos a continuación las evidencias de cada una de estas estrategias.
Nuevos agentes trombolíticos
La búsqueda del agente ideal fue el objetivo de todas las investigaciones clínicas desde los años 90 (cuadro 5). Varias drogas fueron evaluadas en forma comparativa con los clásicos trombolíticos estreptokinasa y el activador tisular del plasminógeno. El reteplase en el estudio Gusto III, el tenecteplace en el estudio Assent-2 y el lanoteplace en el estudio InTime II no pudieron evidenciar ventajas9,10,11. Una limitación clara de estos nuevos agentes ha sido la observación de que mejores niveles de reperfusión coronaria se acompañan de un riesgo muy elevado de sangrado cerebral. Drogas más potentes pero menos seguras. Por tal motivo al no poder mejorar el costo riesgo/beneficio con nuevos fármacos, se comenzó a explorar el camino de optimizar la estrategia trombolítica ya existente (figura 4)
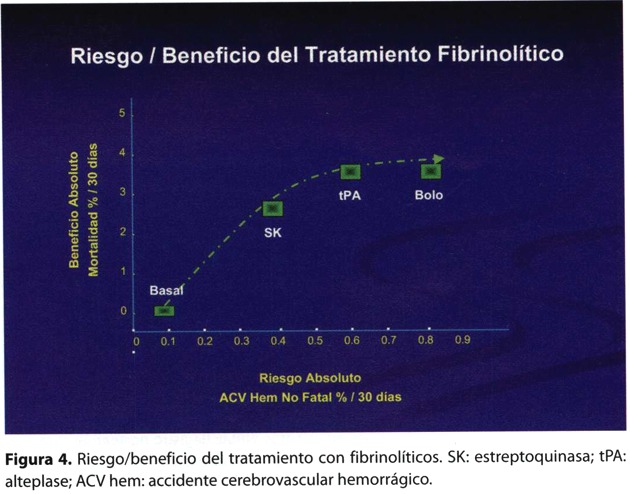
Bases racionales del tratamiento trombolítico optimizado
La administración de agentes fibrinolíticos se asocia con un estado hipercoagulable posterior, debido básicamente a la activación de la trombina, que se sabe, es un poderoso estimulante de la actividad plaquetaria. La activación y agregación plaquetaria, juegan un papel trascendental en la iniciación y propagación de la trombosis coronaria. Este proceso protrombótico es la base fisiopatológica del fracaso de la terapéutica trombolítica. La combinación de nuevos regimenes antiplaquetarios o la inhibición prolongada de la trombina pueden modificar este proceso y reducir los eventos clínicos (reinfarto y muerte).
Nuevos regimenes antiplaquetarios
La aspirina ejerce su efecto antiagregante plaquetario por bloqueo de la síntesis del tromboxano A2, poderosa sustancia proagregante, al inhibir en forma irreversible a la ciclooxigenasa plaquetaria, enzima que las plaquetas no pueden volver a sintetizar, pues carecen de núcleo celular. Los resultados del estudio ISIS-2 son concluyentes12; en más de 17.000 pacientes, la utilización de una dosis de 160 mg/ día de aspirina, en sujetos con IAM tratados con estreptokinasa, evidenciaron una reducción de la mortalidad total del 24 % y además una disminución del 50 % en la incidencia de reinfarto. La eficacia clínica de la aspirina en la cardiopatía isquémica en general y en el infarto en particular se encuentra absolutamente fuera de discusión. Sin embargo, la aspirina al actuar sobre un solo mecanismo de la agregación plaquetaria, tiene un efecto modesto como inhibidor plaquetario. El clopidogrel ejerce su acción inhibitoria sobre los receptores ADP plaquetarios y ha demostrado ser efectivo en prevenir eventos isquémicos en pacientes con enfermedad aterotrombótica sintomática. La simultánea inhibición de ambas vías de agregación, con la combinación de aspirina y clopidogrel pueden producir un mayor efecto antiplaquetario que cada uno en forma independiente. El estudio CLARITY-TIMI 28 fue diseñado para responder justamente ese interrogante13: ¿Es útil el clopidogrel para incrementar la tasa de vaso permeable tardío luego de la terapéutica trombolítica?
Este estudio incluyó 3.491 pacientes con IAM, tratados con aspirina y trombolíticos, aleatorizados a recibir clopidogrel 300 mg de carga y 75 mg de mantenimiento o placebo. La inhibición plaquetaria dual mejora la permeabilidad coronaria, al reducir un 41% el porcentaje de oclusión total, 27% la presencia de trombo endoluminal y aumentar en un 36% la incidencia de flujo TIMI 3. Adicionando clopidogrel al tratamiento trombolítico, 6 pacientes más de cada 100 tratados, quedarán con el vaso permeable luego de la primera semana de evolución del IAM. El estudio CLARITY-TIMI 28 brinda la base fisiopatológica y racional del tratamiento antiplaquetario en el IAM, aunque aún faltaba el ensayo de grandes dimensiones que pudiera demostrar beneficio sobre los eventos clínicos. Este estudio es el COMMIT14, el que incluyó un total de 45.852 pacientes con IAM de menos de 24 horas de evolución, la mitad de los cuales recibió terapia fibrinolítica, y aleatorizados a recibir 75 mg de clopidogrel o placebo. Los resultados del estudio evidencian un beneficio clínico significativo en los pacientes que recibieron clopidogrel. La mortalidad descendió un 7%, también fue significativo el descenso del reinfarto y el accidente cerebrovascular. El impacto fue más pronunciado en más de 23 000 pacientes que recibieron terapéutica fibrinolítica. La reducción absoluta de los eventos (muerte/reinfarto/accidente cerebrovascular) fue de 1,1% en los pacientes reperfundidos y de solo 0,6% en los que no recibieron terapia de reperfusión. La estrategia de reperfusión con fibrinolíticos potencia sus beneficios clínicos cuando se le adiciona un régimen de inhibición plaquetaria dual, aspirina 160 mg/día, combinada con clopidogrel 75 mg/día. Se salvan 10 vidas cada 1 000 pacientes tratados
Tratamiento anticoagulante prolongado
La eficacia de las heparinas en la angina inestable es actualmente incuestionable. Los distintos tipos de heparinas de bajo peso que se han comparado con la heparina no fraccionada han resultado tan eficaces como ésta. El tratamiento en el contexto del IAM es controvertido, existe consenso en la utilización de la heparina standard en pacientes que recibieron trombolíticos fibrinoespecíficos, aunque esta práctica esta basada sobre escasos estudios que indicaban una modesta mejoría en la permeabilidad coronaria. Los estudios ISIS-3 y GISSI-2 realizados en el inicio de la década del 90, evidenciaron una reducción en la mortalidad intrahospitalaria y en el reinfarto, cuando se la asociaba con trombolíticos fibrinoespecíficos y no fibrinoespecíficos15,16. Pero estas diferencias no se mantuvieron hasta los 30 días. Un metaanálisis de los estudios comparando enoxaparina vs. heparina no fraccionada sugiere un menor rango de reinfarto, sin impacto sobre la mortalidad pero con un incremento en el sangrado mayor y el accidente cerebrovascular14. La mayoría de los estudios no demostraron un beneficio claro con la asociación heparinas, aspirina y trombolíticos en el tratamiento del IAM. Probablemente deficiencias metodológicas en el diseño de los ensayos clínicos impidieron sacar conclusiones definitivas sobre el tema. Recientes publicaciones posicionaron, nuevamente al tratamiento con heparina.
El estudio CREATE fue diseñado, justamente, para responder la pregunta: ¿Es útil la anticoagulación prolongada por 7 días con heparina de bajo peso molecular en el IAM? Incorporó 15.570 pacientes con IAM dentro de las 12 horas de evolución y los randomizó a recibir reviparina, una heparina de bajo peso con potente actividad anti-X, versus placebo18. El tratamiento de reperfusión fue elevado (79%), en el 73 % a través de trombolíticos no fibrinoespecíficos y un 6 % con angioplastía primaria. El punto final primario (muerte/reinfarto/accidente cerebrovascular) fue significativamente reducido de 11 a 9,6%, beneficio que persiste hasta los 30 días (13,6 a 11,8 %). Se observó una clara reducción de la mortalidad a 30 días (11,3 % a 9,8 %) y del reinfarto (2,6 a 2 %). El tratamiento anticoagulante precoz incrementa los beneficios de la terapéutica fibrinolítica, utilizados dentro de las 2 primeras horas del IAM previenen 30 eventos en 1 000 tratados, dentro de las 4 horas previene 21/1000 tratados, luego de la hora 8 los beneficios no son significativos. El tratamiento anticoagulante prolongado en el IAM previene 18 muertes o reinfartos sobre 1 000 tratados. En varios países del mundo el tratamiento con trombolíticos fibrinoespecíficos es de elección, se basan en un mayor porcentaje de reperfusión, comparado al tratamiento con estreptoquinasa. Sin embargo, es bien reconocido el mayor estado protrombótico desencadenado luego de su administración. Para controlar esta situación se administra por el término de 48 horas heparina no fraccionada.
El estudio ExTRACT-TIMI 25 (Enoxaparin and Trombolisis Reperfusion for Acute Myocardial Infarction Treatment17) fue realizado para averiguar si: ¿En pacientes con indicación de heparina no fraccionada intravenosa por 48 horas, pueden obtenerse mejores resultados con un esquema alternativo de enoxaparina subcutánea por el término de 7 días?. Se incorporaron 20.506 pacientes con IAM con menos de 6 horas de evolución, todos recibieron tratamiento de reperfusión con trombolíticos, 20% con estreptoquinasa y el 80% restante con agentes fibrinoespecíficos. Se los aleatorizó a recibir heparina no fraccionada endovenosa por el término de 48 horas o enoxaparina subcutánea durante 7 días. El punto final primario a 30 días, muerte/reinfarto, fue descendido en forma significativa con la heparina de bajo peso (12% a 9,9%). El mayor impacto se concentró en una disminución del riesgo relativo de reinfarto del 33 % (4,5% con heparina estándar y 3% con enoxaparina). No hubo diferencias significativas en la mortalidad (7,5% con heparina standard y 6,9% con enoxaparina). El subgrupo de pacientes tratados con estreptoquinasa no demostró beneficios clínicos, probablemente por el escaso número de pacientes. Algunas observaciones de este ensayo son de importancia clínica; el beneficio del tratamiento anticoagulante con enoxaparina puede ser debido a 1) un superior efecto antitrombótico, 2) a la duración prolongada del tratamiento y 3) un posible efecto trombótico rebote al suspender la heparina no fraccionada. Consideramos que estas dos últimas posibilidades son más factibles, en las 48 horas iniciales no se detectaron diferencias en los eventos entre ambas heparinas (5,2 % no fraccionada y 4,7 % en bajo peso), es recién en ese momento, al suspenderse la heparina endovenosa cuando se comienzan a detectar los beneficios de la heparina de bajo peso. El tratamiento por 7 días con enoxaparina adyuvante a los trombolíticos fibrinoespecíficos previenen 15 eventos de reinfarto sobre 1000 pacientes tratados y 6 muertes.
El estudio OASIS- 6 (Organization for the Assessment of Strategies for Ischemic Síndromes19), evaluó el impacto de una nueva molécula anticoagulante, el fondaparinux. Este agente es un pentasacárido sintético, inhibidor del factor Xa, diferente a la heparina ya que no actúa a través de la antitrombina III. Este estudio incluyó 12.092 pacientes con IAM de 12 horas de evolución, los cuales fueron divididos en dos grupos, a criterio del médico tratante: el primero valoró fondaparinux versus placebo durante 7 días en pacientes que no requerían heparina no fraccionada por el uso de estreptoquinasa (78%) o por estar contraindicados los trombolíticos (22%). El segundogrupo comparó fondaparinux con heparina no fraccionada durante 7 días en pacientes con indicación de heparina no fraccionada por haber recibido trombolíticos fibrinoespecíficos (16%), por habérseles realizado angioplastía primaria (53%) o no haber recibido ningún tratamiento de reperfusión (31%). El punto final primario (mortalidad y reinfarto) a los 30 días fue reducido en forma significativa, del 11,2% versus el 9,7% con fondaparinux. De todos los escenarios que se eligieron en este estudio podemos afirmar que la anticoagulación con fondaparinux en el contexto del tratamiento trombolítico esta asociada a un descenso de la muerte y el reinfarto (fondaparinux 11,2 % y el placebo 14 %). En el marco de la angioplastía primaria se observó un incremento de los eventos en los pacientes tratados con fondaparinux (6%) comparados con el placebo (4,9 %). El hallazgo de trombosis pericatéter, hacen suponer que no se lograron niveles adecuados de anticoagulación con las dosis empleadas.
Nivel de seguridad del tratamiento trombolítico optimizado
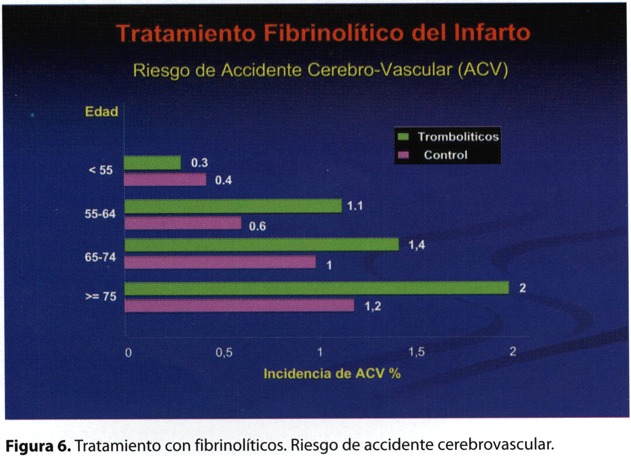
La complicación más temida del tratamiento trombolítico es la hemorragia. Existe un exceso de hemorragia mayor (necesidad de transfusión de dos o más unidades) de 0,7 % respecto del placebo. La incidencia de accidente cerebrovascular se incrementa en 4 pacientes cada 1.000 tratados (1,2% en el grupo trombolítico frente al 0,8% en el grupo control), a expensas del accidente cerebrovascular hemorrágico (0,4% vs. 0,1%); con el aumento de la edad se incrementa el riesgo de desarrollarlo: en pacientes con edades menores a los 55 años el riesgo del evento es similar entre el fibrinolítico (0,3%) y el control (0,4%), en cambio en las poblaciones mayores a los 75 años el riesgo se duplica (2% con trombolíticos y 1,2 % en el grupo control). La utilización de trombolíticos fibrinoespecíficos se asoció a un incremento del sangrado, en el estudio GUSTO I estos agentes tuvieron una incidencia de accidente cerebrovascular hemorrágico 40% mayor que con la estreptokinasa11. El antecedente de enfermedad cerebrovascular previa, el bajo peso y la hipertensión arterial al ingreso son también factores asociados con la posibilidad de sangrado cerebral. Es de suma importancia conocer de las nuevas drogas adyuvantes al tratamiento fibrinolítico, el nivel de seguridad de cada una de ellas. La incidencia de sangrado mayor con el clopidogrel en el estudio CLARITY13 no fue diferente del placebo (1,3% vs. 1,1%) y tampoco se encontraron diferencias en el estudio COMMIT14 (0,58 % vs. 0.53 %). En este último estudio, si analizamos únicamente al 50% de la población que efectivamente recibió tratamiento de reperfusión con trombolíticos, observamos que el incremento del sangrado grave es de solo 0,02 % (0,63% placebo vs. 0,65% clopidogrel). Los estudios con heparina evidenciaron un estrecho margen de seguridad, en el ensayo CREATE18 la incidencia de sangrado mayor en los pacientes reperfundidos tuvo un incremento del 0,7 % (1,1 % reviparin vs. 0.4 % placebo), y con un exceso de hemorragias intracerebrales (0,4 % vs. 0,1 %). En el estudio ExTRACT-TIMI 25 en donde el 100% de los pacientes recibieron terapia de reperfusión17, el exceso de sangrado mayor fue también del 0,7% (enoxaparina 2,1 % vs. heparina no fraccionada 1,4 %), de los cuales 0,1 % corresponde a una hemorragia cerebral. Esta incidencia es menor que en otros estudios con heparinas de bajo peso, fundamentalmente porque en este ensayo se ajustó la dosis en pacientes mayores de 75 años y en aquellos con insuficiencia renal. El OASIS- 6 evidenció que el fondaparinux fue igualmente seguro que la heparina no fraccionada (2,2% vs. 1,7%), con la misma incidencia de sangrado cerebral (0,1%, figura 5)19.
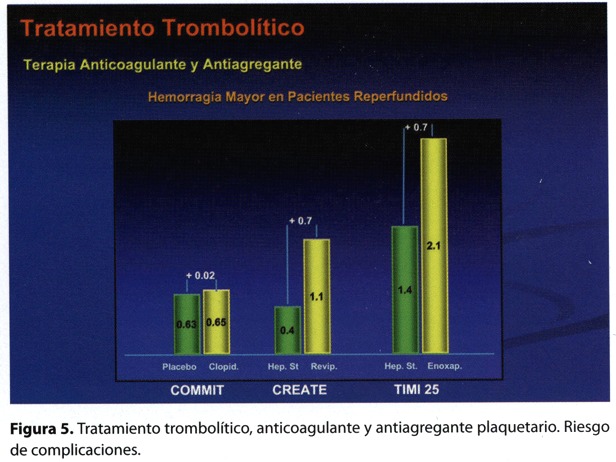
Combinación de terapia antiagregante y anticoagulante
No existe evidencia si la combinación de ambos agentes genera un efecto beneficioso aditivo. Los estudios anteriormente descriptos no estaban diseñados para responder esta pregunta. En el estudio COMMIT14 ningún paciente recibió anticoagulación prolongada, y la asociación con clopidogrel en los estudios con anticoagulantes fue muy baja. En el CREATE18 recibió clopidogrel el 55 % de los pacientes, en el ExTRACT-TIMI 2517 el 28 % y en el OASIS-6 solo el 25 %19. En el ensayo ExTRACT-TIMI 2517 el subanálisis de los 5 727 pacientes que recibieron clopidogrel, evidenció una menor incidencia de muerte y reinfarto a 30 días en el grupo de pacientes que recibieron enoxaparina (8,7 % con enoxaparina y 11,4 % con heparina no fraccionada). Sin embargo, es necesario recordar que el tratamiento clopidogrel-heparina asociado a las fibrinolíticos puede ser potencialmente peligroso por el alto riesgo de hemorragias graves, figura 6). En conclusión, la estrategia de reperfusión fibrinolítica optimizada:
- Mejoró los resultados del tratamiento trombolítico, disminuyendo las diferencias con la angioplastía primaria.
- El beneficio de la heparina de bajo peso en forma prolongada es superior al clopidogrel.
- El riesgo de hemorragia mayor es más frecuente con las heparinas de bajo peso.
- El clopidogrel tiene una mejor relación riesgo/beneficio que las heparinas de bajo peso, por lo que es la terapia adyuvante de primera elección, por su alta disponibilidad en el mercado, además de facilidad en la administración y alta seguridad.
Reflexión final
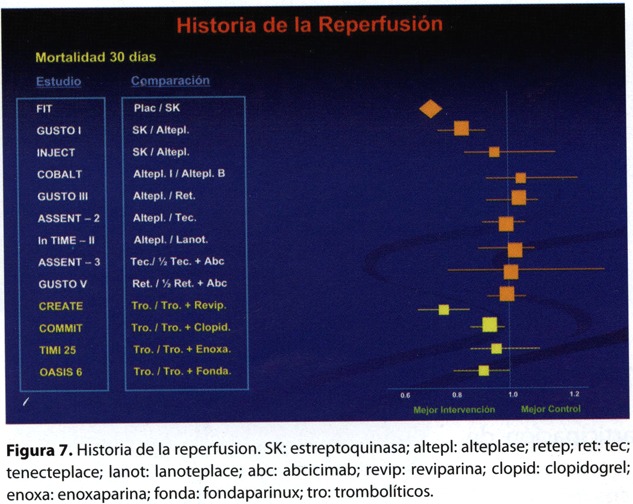
La terapéutica trombolítica es uno de los temas médicos que se han estudiado más exhaustiva y metódicamente en los últimos años. La década del 80 cambió la historia natural de la investigación clínica en el mundo, gracias al advenimiento de ensayos simples, de grandes dimensiones y fácilmente aplicables por la mayoría de los médicos que atienden a pacientes portadores de una patología de tan alta prevalencia como es el infarto. La trombolisis sistémica evidencia una importante ventaja en términos de reducción de la mortalidad, que es más marcada cuanto mas precoz es la instauración del tratamiento. En la primera hora se salvan 39 vidas por cada 1.000 pacientes tratados, gradiente que va disminuyendo a medida que aumenta el tiempo entre el inicio de los síntomas y la aplicación de los líticos, para hacerse no significativa después de las 12 horas. Podemos decir que 1,6 vidas por cada 1000 pacientes tratados se pierden por cada hora que transcurre sin la implementación de la terapéutica. En la historia de la reperfusión, el tratamiento trombolítico mas aspirina llegó a su máximo nivel de beneficio y los resultados de la mortalidad se mantuvieron sin cambios en los últimos 20 años (figura 7).
Los nuevos y potentes trombolíticos mejoraron el porcentaje de reperfusión pero lamentablemente, con un incremento de las complicaciones hemorrágicas. En los últimos tiempos ocurrieron cambios cualitativos en el tratamiento farmacológico del infarto. La inhibición dual de la agregación plaquetaria (aspirina más clopidogrel) o el tratamiento anticoagulante prolongado (7 días) mejoran los resultados obtenidos con el tratamiento trombolítico. La decisión de la mejor estrategia adyuvante a utilizar, dependerá del análisis crítico de los resultados de los estudios controlados (cuadro 6). Estos, nos aportan certezas en el tratamiento de nuestros pacientes, pero también generan incertidumbres dada la información copiosa y contradictoria. Por ello aconsejamos trasladar con mesura y cautela su aplicación al caso individual. Como final es interesante recordar las palabras de Francis Bacon: "Si un hombre empieza con certidumbres, terminará en dudas; pero si está contento de empezar con dudas terminará en certidumbres."
Referencias
1. Fuster V, Moreno PR, Fayad ZA, Corti R, Badimon JJ. Aterotrombosis and high risk plaque: part I: evolving concepts. J Am Coll Cardiol 2005; 46: 937-54. [ Links ]
2. Fibrinolytic therapy trialists (FTT)collaborative group.Indications for fybrinolitic therapy in suspected acute myocardial infarction: collaborative overview of early mortality and major morbidity results of all randomized trials of more than 1000 patients. Lancet 1994; 343: 311-322. [ Links ]
3. Fox KA, Dabbous OH, Goldberg RJ, Pieper KS, Eagle KA, Van de Werf F, Avezum A, Goodman SG, Flather MD, Anderson FA, Granger CB. Prediction of risk of death and myocardial infarction in the six months after presentation with acute coronary syndrome: prospective multinational observational study (GRACE). BMJ 2006; 25: 333- 1079. [ Links ]
4. Canto JG, Taylor HA Jr, Rogers WJ, Sanderson B, Hilbe J, Barron HV. Presenting characteristics, treatment patterns, and clinical outcomes of non-black minorities in the National Registry of Myocardial Infarction 2. Am J Cardiol 1998 Nov 1;82(9): 1013-88. [ Links ]
5. Perez de Arenaza D, Taneja AK, Flather M. Long distance transport for primary angioplasty vs immediate thrombolysis in acute myocardial infarction (PRAGUE-2 trial). Eur Heart J. 2003; 24 (19): 1798. [ Links ]
6. Andersen HR, Nielsen TT, Rasmussen K, Thuesen L, Kelbaek H, Thayssen P, Abildgaard U, Pedersen F, Madsen JK, Grande P, Villadsen AB, Krusell LR, Haghfelt T, Lomholt P, Husted SE, Vigholt E, Kjaergard HK, Mortensen LS; DANAMI-2 Investigators. A Comparison of Coronary Angioplasty with Fibrinolytic Therapy in Acute Myocardial Infarction. N Engl J Med 2003; 349(8): 733-42. [ Links ]
7. Steg PG, Bonnefoy E, Chabaud S, Lapostolle F, Dubien PY, Cristofini P, Leizorovicz A, Touboul P; Comparison of Angioplasty and Prehospital Thrombolysis In acute Myocardial infarction (CAPTIM) Investigators. Impact of time to treatment on mortality after prehospital fibrinolysis or primary angioplasty: data from the CAPTIM randomized clinical trial. Circulation. 2003; 108 (23): 2851-66. [ Links ]
8. An international randomized trial comparing four thrombolytic strategies for acute myocardial infarction. The GUSTO Investigators. N Eng J Med 1993; 329: 673-82. [ Links ]
9. A Comparison of Reteplase with Alteplase for Acute Myocardial Infarction. The Global Use of Strategies to Open Occluded Coronary Arteries (GUSTO III) Investigators. N Eng J Med 1997; 337: 1118-1123. [ Links ]
10. Assessment of the Safety and Efficacy of a New Thrombolytic (ASSENT-2) Investigators, Van De Werf F, Adgey J, Ardissino D, Armstrong PW, Aylward P, Barbash G, et al. Single-bolus tenecteplase compared with front-loaded alteplase in acute myocardial infarction: the ASSENT-2 double-blind randomised trial. Lancet 1999; 354: 716-22. [ Links ]
11. den Heijer P, Vermeer F, Ambrosioni E, Sadowski Z, López-SS von Essen R, et al. Evaluation of a weight-adjusted single-bolus plasminogen activator in patients with myocardial infarction: a double-bblind, randomized angiographic trial of lanoteplase versus alteplase. Circulation. 1998; 98 (20): 2117-25. [ Links ]
12. ISIS 2 collaborative group (Second International Study of Infarct Survival). Randomised trial of intravenous streptokinase, oral aspirin, both, or neither among 17187 cases of suspected acute myocardial infarction ISIS-2. ISIS-2 (Second International Study of Infarct Survival) Collaborative Group Lancet 1988; 2: 349. [ Links ]
13. Marc S. Sabatine, M.D., M.P.H., Christopher P. Cannon, M.D., C. Michael Gibson, M.D., Jose L. López-S M.D., Gilles Montalescot, M.D., Pierre Theroux, M.D., Marc J. Claeys, M.D., Ph.D., Frank Cools, M.D., Karen A. Hill, B.A., Allan M. Skene, Ph.D., Carolyn H. McCabe, B.S., Eugene Braunwald, M.D., for the CLARITY –TIMI 28 Investigators Addition of Clopidogrel to Aspirin and Fibrinolytic Therapy for Myocardial Infarction with ST-S Elevation. N Eng J Med 2005; 352: 1179-1189. [ Links ]
14. Chen ZM, Jiang LX, Chen YP, Xie JX, Pan HC, Peto R, Collins R, Liu LS; COMMIT (ClOpidogrel and Metoprolol in Myocardial Infarction Trial) collaborative group. Addition of clopidogrel to aspirin in 45,852 patients with acute myocardial infarction: randomised placebo-controlled trial. Lancet 2005; 366: 1607-32. [ Links ]
15. ISIS-3: a randomised comparison of streptokinase vs tissue plasminogen activator vs anistreplase and of aspirin plus heparin vs aspirin alone among 41,299 cases of suspected acute myocardial infarction. ISIS-3 (Third International Study of Infarct Survival) Collaborative Group. Lancet. 1992; 339 (8796): 753-70. [ Links ]
16. Moccetti T, Malacrida R, Pasotti E, Sessa F, Genoni M, Barlera S, Turazza F, Maggioni AP. Epidemiologic variables and outcome of 1972 young patients with acute myocardial infarction. Data from the GISSI-2 database. Investigators of the Gruppo Italiano per lo Studio della Sopravvivenza nell Infarto Miocardico (GISSI-2). Arch Intern Med. 1997; 157(8): 865-9. [ Links ]
17. Antman EM, Morrow DA, McCabe CH, Murphy SA, Ruda M, Sadowski Z, Budaj A, Lopez-S Guneri S, Jiang F, White HD, Fox KA, Braunwald E; ExTRACT-TIMI 25 Investigators. Enoxaparin versus unfractionated heparin with fibrinolysis for ST-elevation myocardial infarction. N Engl J Med. 2006; 354(14): 1477-88. [ Links ]
18. Yusuf S, Mehta SR, Xie C, Ahmed RJ, Xavier D, Pais P, Zhu J, Liu L; CREATE Trial Group Investigators. Effects of reviparin, a low-molecular-weight heparin, on mortality, reinfarction, and strokes in patients with acute myocardial infarction presenting with ST-segment elevation. JAMA 2005; 293: 427-35. [ Links ]
19. Yusuf S, Mehta SR, Chrolavicius S, Afzal R, Pogue J, Granger CB, Budaj A, Peters RJ, Bassand JP, Wallentin L, Joyner C, Fox KA; OASIS-6Trial Group. elevation myocardial infarction: the OASIS-6 randomized trial. JAMA 2006; 295: 1519-30. [ Links ]
Otras lecturas recomendadas:
Keeley EC, Boura JA, Grines CL. Primary angioplasty versus intravenous thrombolytic therapy for acute myocardial infarction: a quantitative review of 23 randomised trials. Lancet 2003; 361: 13-20.
Consenso de Sindromes Coronarios Agudos. Rev Arg Cardiol Vol 73 Supl. 3 Nov-Dic 2005; 45-62.
Doval H. Evidencias en Cardiología V. GEDIC. Buenos Aires 2005. Cap 11: 225- 270.
Fitz Maurice M. Trials de la terapéutica cardiovascular. 5ta edición, Buenos Aires 2005. 213-215.
















